Дыхательная недостаточность. Определение, причины, классификация и патофизиология хронической дыхательной недостаточности.
Раздел:
Статьи
/ Общая врачебная практика.
/ Пульмонология.
/ Дыхательная недостаточность. Определение, причины, классификация и патофизиология хронической дыхательной недостаточности.
Содержание
Определение дыхательной недостаточности
Этиология дыхательной недостаточности
Классификация и патофизиология дыхательной недостаточности
Пороговые значения pаО2 и pаСО2 могут формулироваться иначе, в частности 60 и 50 мм рт.ст. соответственно, но в таком случае не учитываются ранние стадии ДН. Кроме того, напряжение газов крови для конкретного индивидуума может зависеть от разных факторов, таких как барометрическое давление, фракция кислорода во вдыхаемом воздухе, возраст пациента (зависимость pаО2 от возраста выражается уравнением pаО2 = 104 - 0,27 × возраст (лет) и т.д..
Различают острую дыхательную недостаточность, которая развивается за короткий промежуток времени, вплоть до нескольких минут, и часто характеризуется тенденцией к стремительному прогрессированию, и хроническую ДН (ХДН), формирующуюся за продолжительное время. Иногда острая дыхательная недостаточность осложняет течение ХДН на фоне обострения приведшего к ней заболевания.
Если причина острой дыхательной недостаточности не устраняется, у пациента нарастают нарушения оксигенации крови, гиперкапния, сдвиги кислотно-основного состояния крови: респираторный ацидоз в случае вентиляционной ДН (рН <7,35 мм рт.ст.) и респираторный алкалоз при паренхиматозной ДН (рН >7,45). Напротив, при длительном существовании ДН организм обычно оказывается в состоянии скорректировать уровень рН и поддерживать его в пределах нормальных значений, используя такие механизмы, как увеличение содержания гемоглобина в крови и полицитемия. Респираторный ацидоз компенсируется задержкой почками избытка оснований, а респираторный алкалоз - дефицитом последних.
Синдром дыхательной недостаточности по характеру может иметь первичное (пульмоногенное) и вторичное (непульмоногенное) происхождение. В первом случае дыхательная недостаточность развивается при заболеваниях и повреждениях, непосредственно поражающих аппарат дыхания (легкие, воздухопроводящие пути, систему легочных сосудов, дыхательную мускулатуру и грудную клетку). При вторичной дыхательной недостаточности патологические изменения первично возникают и локализуются в органах и системах, не входящих в анатомо-физиологический комплекс аппарата внешнего дыхания, который вовлекается в патологический процесс вторично. Типичным примером вторичной дыхательной недостаточности является нарушение вентиляции легких при поражениях головного и спинного мозга.
Наиболее частыми причинами дыхательной недостаточности становятся:
• поражения бронхов и респираторных отделов легких (обструктивные заболевания легких: ХОБЛ, бронхоэктазы, муковисцидоз, гораздо реже - бронхиальная астма; интерстициальные заболевания легких, в том числе идиопатический легочный фиброз, пневмокониозы, распространенный пневмофиброз вследствие перенесенных инфекционных заболеваний (туберкулез); первичные и метастатические опухоли легких);
• деформации грудной клетки (кифосколиоз, последствия травм), морбидное ожирение;
• миопатии и мышечные дистрофии, нейромышечные заболевания;
• заболевания центральной нервной системы с дисфункцией дыхательного центра;
• нарушения кровообращения в сосудах малого круга (тромбоэмболическая легочная гипертензия, васкулиты).
Дыхательная недостаточность делится на два типа (рис. 1.1).
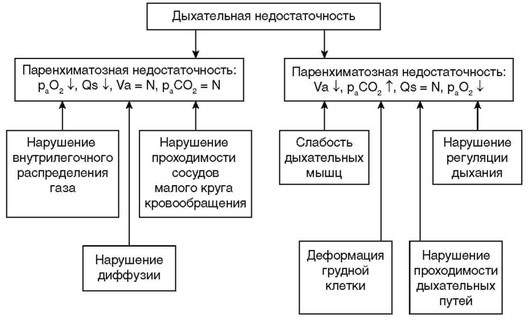
I. Хроническая дыхательная недостаточность I типа (ХДН I типа, гипоксемическая, паренхиматозная, легочная) обусловлена поражением альвеол, альвеоло-капиллярной мембраны, легочных сосудов и характеризуется артериальной гипоксемией в первую очередь в результате нарушения регионарных вентиляционно-перфузионных (Vа/Q) отношений в легких, что приводит к усилению внутрилегочного шунтирования крови. Недостаточно насыщенная кислородом кровь, поступающая из легочных зон со сниженным отношением вентиляции к кровотоку, уменьшает общее pа02 крови, оттекающей от легких. Другим механизмом развития паренхиматозной ДН является снижение диффузионной способности альвеоло-капиллярной мембраны. Утолщение мембраны происходит, в частности, у больных интерстициальным заболеванием легких.
Элиминация С02 при перенхиматозной ДН не нарушена, поскольку углекислота диффундирует через альвеолярно-капиллярную мембрану в 20 раз быстрее, чем кислород.
II. Хроническая дыхательная недостаточность II типа (ХДН II типа, гиперкапническая, вентиляционная, насосная) вызвана первичным уменьшением эффективной легочной вентиляции (альвеолярная гиповентиляция), что нарушает оксигенацию крови и выведение С02. Уровень гиперкапнии при этом пропорционален степени уменьшения альвеолярной вентиляции. Снижение альвеолярной вентиляции может возникать при нормальной и даже увеличенной общей вентиляции легких. Это связано с возрастанием мертвого пространства при изменениях отношения «вентиляция/ кровоток». Основными механизмами развития вентиляционной формы ДН являются: нарушение центральной регуляции дыхания (острые нарушения мозгового кровообращения, черепно-мозговые травмы, нейроинфекция, передозировка лекарственных препаратов, угнетающих дыхательный центр), повреждение аппарата, обеспечивающего дыхательные движения грудной клетки, в том числе периферических нервов, дыхательных мышц, грудной стенки (деформация грудной стенки, переломы ребер и позвоночника, миастения), выраженные рестриктивные расстройства (интерстициальные заболевания легких), сопровождающиеся снижением минутного объема дыхания. Хотя такой тип ХДН характерен преимущественно для больных с рестриктивной патологией легких, он может встречаться и при обструктивных заболеваниях.
При вентиляционной хронической дыхательной недостаточности гипоксемия выражена в меньшей степени, чем при ХДН I типа. Более того, поскольку у больного с ХДН II типа постепенно снижается чувствительность к повышенному уровню pаС02, назначение ему интенсивной кислородотерапии способно привести к обратному эффекту. Из-за уменьшения гипоксической стимуляции центров регуляции дыхания на систему внешнего дыхания вентиляция у пациента может значительно ухудшиться, следствием чего является значительное повышение pаС02. Еще одной причиной задержки С02 в таких случаях становится исчезновение гипоксической вазоконстрикции в участках легких, где есть плохая вентиляция, но на фоне ингаляции кислорода уровень pа02 повышается. Это приводит к увеличению кровотока в участках легких с низким вентиляционно-перфузионным отношением, что дополнительно усугубляет неравномерность вентиляционно-перфузионных отношений и способствует задержке С02.
Дыхательная недостаточность, включая хроническую дыхательную недостаточность, классифицируют также по степени тяжести. Наиболее известной клинической классификацией ДН является классификация А.Г. Дембо (1957 г.), в соответствии с которой выделяются три степени (табл. 1.1).
| Степень дыхательной недостаточности | Клиническая картина |
| 1 | Одышка только при физическом напряжении. Все показатели вентиляции и газообмена в пределах должных. Гипоксемии нет |
| 2 | Одышка при незначительном физическом напряжении. Компенсаторные механизмы включены в состоянии покоя. Функциональные показатели обнаруживают различные отклонения от должных величин. Гипоксемии, как правило, нет |
| 3 | Одышка в покое. Имеются значительные отклонения показателей вентиляции и газообмена. Артериальная гипоксемия |
Таблица 1.1. Степени тяжести дыхательной недостаточности по А.Г. Дембо
Позднее А.П. Зильбером была предложена классификация (1989 г.), которая делает упор на степень компенсации ДН (табл. 1.2).
| Степень дыхательной недостаточности | Клиническая картина |
| Декомпенсированная | Патологически измененные pаО2 и pаСО2 в покое несмотря на полное напряжение компенсаторных механизмов (гипервентиляция, ускорение кровотока с тахикардией, увеличением ударного объема и сердечного выброса, увеличение массы эритроцитов и гемоглобина, изменение диссоциации оксигемоглобина, снижение тканевого метаболизма). Требуется интенсивная терапия |
| Компенсированная | pаО2 и pаСО2 в покое за счет напряжения компенсаторных механизмов остаются в пределах допустимых значений, но на фоне физических нагрузок возможна декомпенсация. Показаны лечебные мероприятия |
| Скрытая | Газы крови нормальны, симптомов напряжения в покое нет, но функциональные дыхательные резервы ограничены: тесты с дозированной нагрузкой выявляют признаки компенсации и декомпенсации. Целесообразна реабилитационная терапия |
Таблица 1.2. Степени тяжести дыхательной недостаточности по А.П. Зильберу
Однако имеющей наибольшее практическое значение является классификация ДН, отражающая газовый состав крови (табл. 1.3), уровни pаО2 и сатурации кислородом артериальной крови (SаО2). Такая классификация позволяет стандартизировать подходы к коррекции ДН. В частности, вторая степень дыхательной недостаточности в данном случае указывает на обязательность кислородотерапии.
| Степень хронической дыхательной недостаточности | pаО2, мм рт.ст. | SаО2, % |
| Норма | ≥80 | ≥95 |
| 1 | 60-79 | 90-94 |
| 2 | 40-59 | 75-89 |
| 3 | <40 | <75 |
Таблица 1.3. Степень тяжести дыхательной недостаточности в зависимости от газового состава крови
Из нескольких хемосенсоров, контролирующих обмен газов, за обнаружение отклонений в гомеостазисе СО2 в основном отвечают центральные хеморецепторы, расположенные в продолговатом мозге вблизи вентральной поверхности, где корешки подъязычного нерва выходят из мозгового ствола (рис. 1.2).
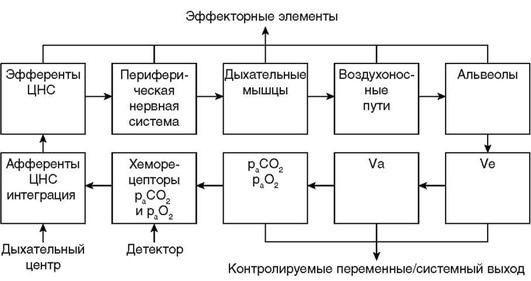
Дыхательный центр интегрирует поступающую афферентную информацию и создает центральный нервный стимул дыхания. Этот стимул преобразуется в моторную активность, которая обеспечивает обмен газа в альвеолах. Главными регулируемыми переменными являются общая минутная вентиляция (Vе), альвеолярная вентиляция (Va) и уровни pаО2 и pаСО2 в артериальной крови
Хемочувствительные клетки реагируют на отклонения в [Н+] и парциальное давление углекислого газа (pСО2) во внеклеточной жидкости внутримозгового интерстициального пространства. Когда местная [H+] увеличивается, что эквивалентно падению рН, дыхательный центр увеличивает вентиляцию по сигналу от центральных хеморецепторов. Вместе с тем отклонения во внеклеточной [H+] - не единственный стимул для центральных хеморецепторов. Рост вентиляции в ответ на изолированное повышение внеклеточной [Н+] при отсутствии изменений pСО2 (изокапнический метаболический ацидоз) происходит медленнее.
Одной из причин высокой скорости вентиляторного ответа на гиперкапнию является легкость диффузии СО2 через барьерную систему «кровь - головной мозг». Однако этот барьер относительно непроницаем для ионов [H+] и [HСО3-]. Более того, повышенное pСО2 вызывает расширение сосудов, особенно церебральных, способствуя тем самым усилению диффузии СО2 через гематоэнцефалический барьер. Диффузия СО2 представляет собой еще один важный механизм усиления связи между отклонениями кислотно-основного состояния организма и центральными хеморецепторами.
В то время как мониторинг pСО2 происходит в стволе головного мозга, отслеживание pО2 является функцией исключительно каротидных телец, расположенных у бифуркации общих сонных артерий на внутреннюю и наружную. Главной клеткой каротидного синуса является гломусная клетка (I тип). Она содержит несколько нейротрансмиттеров, включая большое количество допамина и других катехоламинов, а также серотонин, ацетил-холин и некоторые нейропептиды. Гломусные клетки образуют синапсы с афферентными волокнами нерва каротидного синуса. Чувствительная ветвь языкоглоточного нерва и нерв каротидного синуса иннервируют каротидное тельце и барорецепторы каротидного синуса. Афферентные волокна языкоглоточного нерва берут свое начало в чувствительных нейронах каменистого ганглия. В ответ на артериальную гипоксемию гломусные клетки высвобождают допамин пропорционально степени снижения pа02. Высвобождение допамина модулируется отклонениями рН, вызванными метаболическим или дыхательным ацидозом, и приводит к значительному повышению тонической активности афферентных чувствительных волокон каротидных телец. Эти афферентные волокна проявляют некоторую степень тонической активности в условиях нормоксии и даже гипероксии. 0ни «замолкают» только в присутствии выраженной артериальной гипероксии и гипокапнии. Когда pа02 падает ниже 60 мм рт.ст., активность афферентных нервов каротидного тельца возрастает экспоненциально.
Наиболее существенным фактором регулирования минутной вентиляции в состоянии покоя является уровень pаС02, отслеживаемый центральными хеморецепторами. Если артериальное содержание 02 держится на постоянном уровне, минутная вентиляция возрастает примерно на 2-3 л/мин на каждый 1 мм рт.ст. повышения pаС02. Понижение концентрации 02 во вдыхаемой смеси газов (снижающее уровень pа02) повышает не только минутную вентиляцию при заданном уровне pаС02, но также скорость нарастания минутной вентиляции с повышением pаС02 (синергическая связь). Дыхательный контроллер отслеживает изменения как pа02, так и pаС02, а сочетание гипоксии с гиперкапнией приводит к большему увеличению минутной вентиляции, чем любой из этих стимулов в отдельности.
При нормальном pаС02 минутная вентиляция не растет до тех пор, пока pа02 не упадет ниже 60 мм рт.ст. Этот эффект основан на минимальном изменении активности каротидного тельца при pа02 выше 60 мм рт.ст. Повышение pаС02 увеличивает минутную вентиляцию при любом pа02. У здоровых взрослых людей в обычных условиях гипоксия не играет важной роли в стимулировании минутной вентиляции. Однако при определенных условиях (например, при патологии легких или во время нахождения на больших высотах) вентиляторный ответ на гипоксию приобретает решающее значение в поддержании газообмена и гомеостазиса.
Для транспорта кислорода решающее значение имеют:
1) кислородная емкость крови;
2) сродство гемоглобина (Hb) к кислороду;
3) состояние центральной гемодинамики, которое зависит от сократительной способности миокарда, величины сердечного выброса, объема циркулирующей крови и величины кровяного давления в сосудах большого и малого кругов;
4) состояние кровообращения в микроциркуляторном русле.
Насыщение гемоглобина кислородом зависит от его напряжения в альвеолах и крови. Графически эту зависимость отражает кривая диссоциации оксигемоглобина (рис. 1.3). Кривая показывает, что процент оксигенации гемоглобина сохраняется на довольно высоком уровне при существенном снижении парциального давления кислорода. Так, при напряжении кислорода, равном 95-100 мм рт.ст., оксигенация гемоглобина соответствует 96-98%, при напряжении 60 мм рт.ст. - равняется 90%, а при снижении напряжения кислорода до 40 мм рт.ст., что имеет место в венозном конце капилляра, оксигенация гемоглобина равна 73%.
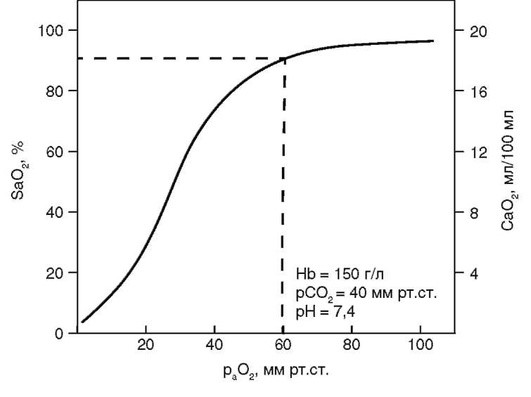
Рис. 1.3. Кривая диссоциации оксигемоглобина: pаО2 - парциальное давление кислорода в артериальной крови; SаО2 - насыщение гемоглобина артериальной крови кислородом; СаО2 - содержание кислорода в артериальной крови.
Кроме парциального давления кислорода, на процесс оксигенации гемоглобина оказывают влияние температура тела, концентрация Н+-ионов, напряжение в крови СО2, содержание в эритроцитах 2,3-дифосфоглицерата (2,3-ДФГ) и АТФ и некоторые другие факторы (рис. 1.4).
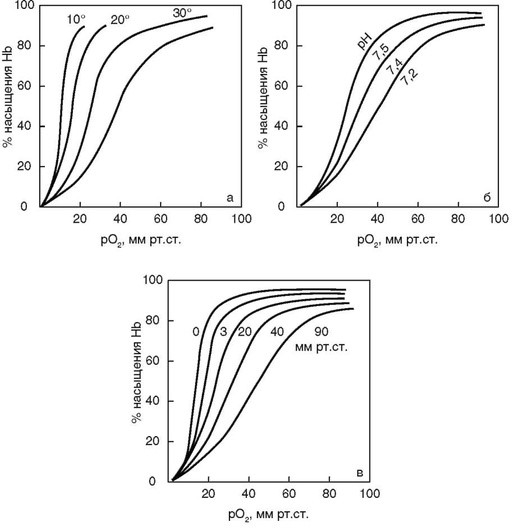
Под действием перечисленных факторов изменяется степень сродства гемоглобина к кислороду, что оказывает влияние на скорость взаимодействия между ними, прочность связи и быстроту диссоциации оксигемоглобина (НbО2) в капиллярах тканей, а это очень важно, так как в клетки тканей проникает только физически растворенный в плазме крови кислород. В зависимости от изменения степени сродства гемоглобина к кислороду происходят сдвиги кривой диссоциации оксигемоглобина. Если в норме превращение 50% гемоглобина в НbО2 происходит при pаО2, равном 26,6 мм рт.ст., то при снижении сродства между гемоглобином и кислородом это имеет место при 30-32 мм рт.ст., и кривая в результате смещается вправо. Сдвиг кривой диссоциации НbО2 вправо происходит при метаболическом и газовом (гиперкапния) ацидозе, при повышении температуры тела (лихорадке, перегревании, лихорадоподобных состояниях), при увеличении содержания АТФ и 2,3-ДФГ в эритроцитах; накопление последнего имеет место при гипоксемии, различных видах анемий (особенно при серповидноклеточной). При всех указанных состояниях увеличивается быстрота отщепления кислорода от НbО2 в капиллярах тканей и замедляется скорость оксигенации гемоглобина в капиллярах легких, что ведет к снижению содержания кислорода в артериальной крови.
Сдвиг кривой диссоциации НbО2 влево происходит при увеличении сродства гемоглобина к кислороду и наблюдается при метаболическом и газовом (гипокапния) алкалозах, при общей гипотермии и в участках местного охлаждения тканей, при понижении содержания в эритроцитах 2,3-ДФГ (например, при сахарном диабете), при отравлении окисью углерода и при метгемоглобинемии, при наличии в эритроцитах больших количеств фетального гемоглобина, что имеет место у недоношенных детей. При сдвиге влево (вследствие повышения сродства гемоглобина к кислороду) ускоряется процесс оксигенации гемоглобина в легких и вместе с тем замедляется процесс дезоксигенации НbО2 в капиллярах тканей, что ухудшает снабжение клеток кислородом, в том числе клеток центральной нервной системы. Это может вызвать ощущение тяжести в голове, головную боль и тремор.
pСО2 в артериальной крови такое же, как в альвеолах, и соответствует 4,7-6,0 кПа (35-45 мм рт.ст., в среднем - 40 мм рт.ст.).
В венозной крови pСО2 равно 6,3 кПа (47 мм рт.ст.). Количество транспортируемого СО2 в артериальной крови равняется 50 об.%, а в венозной - 55 об.%. Примерно 10% объема СО2 физически растворено в плазме крови, и именно эта часть углекислоты определяет напряжение газа в плазме. Еще 10-11% объема СО2 транспортируется в виде карбгемоглобина, при этом восстановленный гемоглобин более активно, чем оксигемоглобин, связывает углекислоту. Остальной объем СО2 переносится в составе молекул бикарбоната натрия и калия, которые образуются при участии фермента карбоангидразы эритроцитов. В капиллярах легких по причине превращения гемоглобина в оксигемоглобин связь СО2 с гемоглобином становится менее прочной и происходит его превращение в физически растворимую форму. Вместе с тем оксигемоглобин, являясь сильной кислотой, отнимает калий от бикарбонатов. Образовавшаяся при этом угольная кислота (Н2СО3) расщепляется под действием карбоангидразы на Н2О и СО2, и последний диффундирует в альвеолы.
Транспорт СО2 нарушается:
1) при замедлении кровотока;
2) при анемиях, когда уменьшается его связывание с гемоглобином и включение в бикарбонаты из-за недостатка карбоангидразы (которая содержится только в эритроцитах).
На парциальное давление СО2 в крови существенное влияние оказывает понижение или повышение вентиляции альвеол. Уже незначительное изменение парциального давления СО2 в крови влияет на мозговое кровообращение. При гиперкапнии (вследствие гиповентиляции) сосуды мозга расширяются, повышается внутричерепное давление, что сопровождается головной болью и головокружением.
Источник: Хроническая дыхательная недостаточность / под ред. О. Н. Титовой, Н. А. Кузубовой. - Москва : ГЭОТАР-Медиа, 2021.
06.12.2021 | 20:49:06