Болезнь Тея-Сакса: современные подходы к диагностике и лечению редкого наследственного заболевания. Перспективы лечения.
Раздел: Статьи
/
Общая врачебная практика.
/
Наследственные заболевания.
/
Болезнь Тея-Сакса: современные подходы к диагностике и лечению редкого наследственного заболевания. Перспективы лечения.
Содержание
Введение
- Молекулярные механизмы и генетика
- Клинические формы и симптомы
- Диагностика болезни Тея-Сакса: современные алгоритмы
- Лечение болезни Тея-Сакса: от паллиативной помощи к экспериментальной терапии
- Профилактика и генетическое консультирование
- Последние исследования и перспективы в лечении болезни Тея-Сакса (2024–2025 гг.)
Заключение
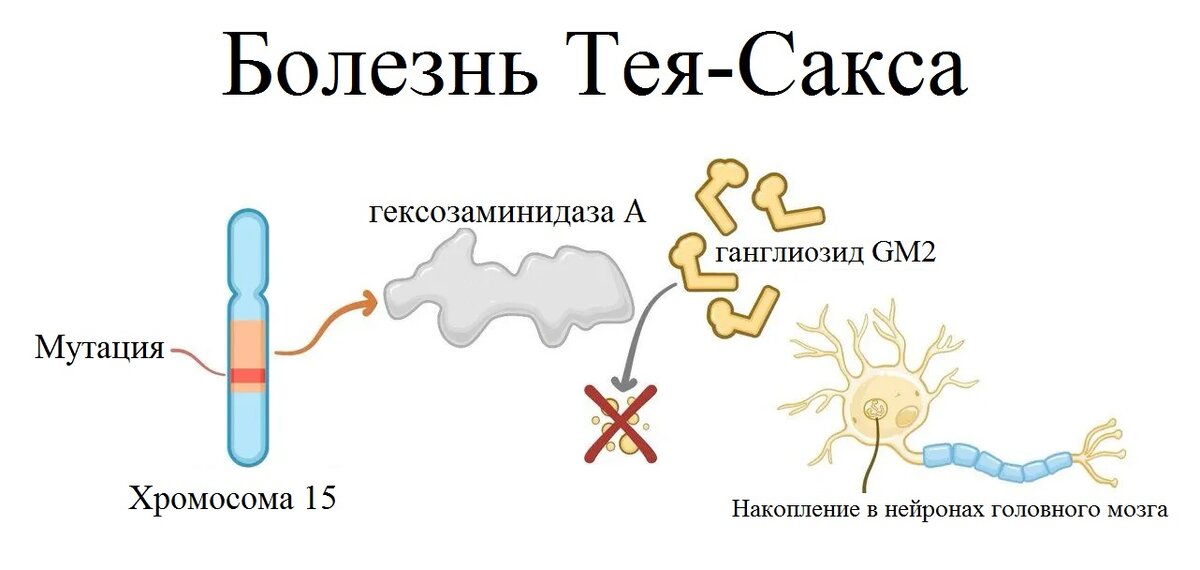

Болезнь Тея-Сакса (БТС) — GM2-ганглиозидоз, тяжелое наследственное нейродегенеративное заболевание из группы лизосомных болезней накопления, обусловленное дефицитом фермента β-гексозаминидазы А (HexA). Впервые описанная в 1881 году, патология приводит к прогрессирующему разрушению нервной системы и в классической инфантильной форме заканчивается летальным исходом к 3–5 годам.
- Частота заболевания в популяции: 1:320 000 новорожденных
- Повышенная распространенность среди евреев ашкенази (1:3 500)
- В России ежегодно рождается 2–5 детей с БТС
- Отсутствие этиотропного лечения (активные исследования генной терапии)
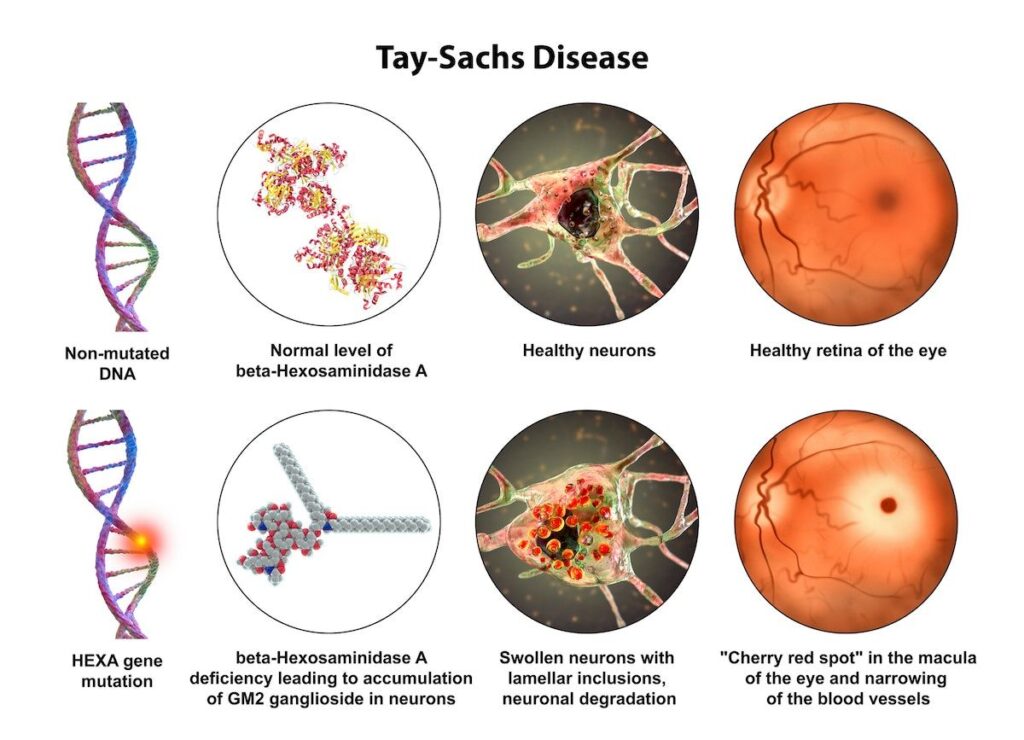

1. Биохимический дефект
Дефицит HexA → накопление GM2-ганглиозида в нейронах →:
- Нарушение синаптической передачи
- Апоптоз нейронов
- Демиелинизация
2. Генетические особенности
- Локализация гена: 15q23
- >130 известных мутаций (80% — миссенс)
- Частые мутации у ашкенази:
- c.1274_1277dupTATC (84%)
- c.1421+1G>C (12%)
Важно: носительство у евреев ашкенази — 1:30
1. Инфантильная форма (классическая) болезни Тея-Сакса
Дебют: 3–6 месяцев
Триада признаков:
1. Потеря моторных навыков (перестает переворачиваться/держать голову)
2. Гиперакузия (вздрагивание на звуки)
3. "Вишнёво-красное пятно" на глазном дне (95% случаев)
Динамика:
- К 1 году: спастический тетрапарез
- К 2 годам: декортикационная поза, слепота
- Летальный исход: 3–5 лет (дыхательная недостаточность)
2. Поздние формы (редкие) болезни Тея-Сакса
| Тип | Дебют | Симптомы | Выживаемость |
| Ювенильная | 2-10 лет | Атаксия, дизартрия | до 15-20 лет |
| Взрослая | старше 15 лет | Психозы, слабоумие, дистония | десятилетия |
1. Скрининг
- Пренатальный (CVS/амниоцентез):
- Активность HexA в культуре клеток
- Генетический анализ (NGS панель)
- Неонатальный (в группах риска):
- Ферментный анализ в сухих пятнах крови
- Определение GM2 в моче
2. Подтверждение диагноза
1. Ферментный анализ:
- Активность HexA в лейкоцитах <1% от нормы
- Соотношение HexA/HexB
2. Генетическое тестирование:
- Полное секвенирование гена HEXA
- Выявление делеций (MLPA)
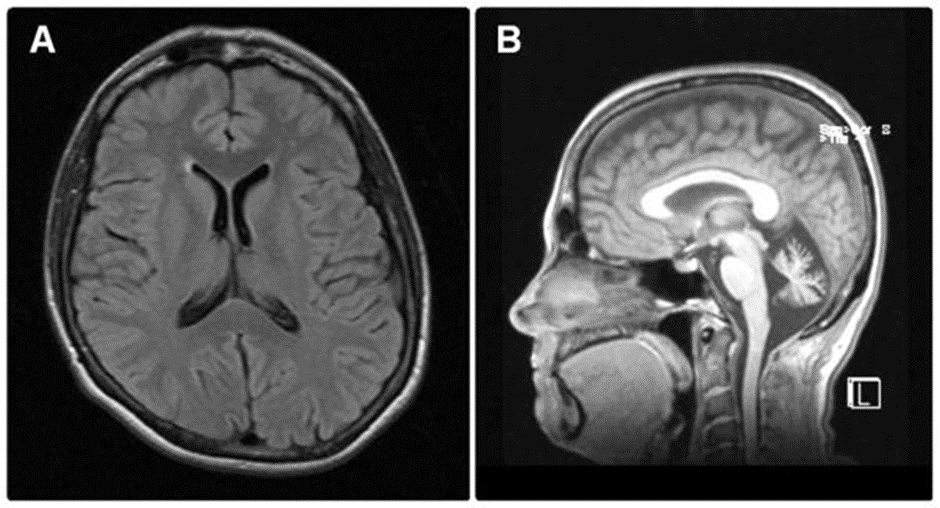
3. МРТ головного мозга:
- Гиперинтенсивность таламуса (симптом "тигрового глаза")
- Атрофия мозжечка
1. Симптоматическое лечение
- Судороги: вальпроевая кислота + леветирацетам
- Спастичность: баклофен, ботулотоксин
- Питание: гастростома при бульбарных нарушениях
2. Перспективные методы
1. Генная терапия:
- AAV-векторы с кДНК HEXA (исследование NCT04798235)
- CRISPR-Cas9 коррекция in vivo (доклинические испытания)
2. Субстрат-редуцирующая терапия:
- Пириметамин (увеличивает остаточную активность HexA)
- Миглустат (ингибитор синтеза GM2)
3. Трансплантация стволовых клеток:
- Гемопоэтические стволовые клетки (ограниченная эффективность)
1. Скрининг носителей в группах риска:
- Евреи ашкенази, канадские франко-квебекцы, луизианские кажуны
- Анализ на 3 частые мутации (охват 94-98%)
2. Преимплантационная диагностика (ПГД) для пар-носителей
3. Пренатальная диагностика:
- Биопсия ворсин хориона (10-12 нед.)
- Неинвазивный тест ДНК плода (cffDNA)
1. Генная терапия: прорывные разработки
a. AAV-векторные технологии
Исследование NCT04798235 (США–ЕС):
- Цель: интратекальное введение AAV9-HEXA 12 пациентам с инфантильной формой
- Результаты фазы I/II (2024):
- У 4 из 6 пациентов достигнуто 15–20% активности HexA в ЦНС
- Замедление прогрессирования (шкала CHOP-INTEND +8 баллов за 12 мес.)
- Побочные эффекты: транзиторный лептоменингит (у 2 пациентов)
Новые векторы (MIT, 2025):
- AAV-PHP.eB с промотором GFAP:
- В 3 раза выше экспрессия в астроцитах
- Доклинические данные: снижение GM2 в мозге мышей на 65%
b. CRISPR-коррекция
Лондонский консорциум (UCL):
- Ex vivo подход: редактирование гемопоэтических стволовых клеток
- Эффективность: 45% отредактированных клеток у приматов
- Планируемые клинические испытания: 2026 г.
In vivo доставка (Nature Biotech, 2024):
- Липидные наночастицы с sgRNA Hexa-Ex3
- Однократное введение → коррекция 25% нейронов
2. Субстрат-редуцирующая терапия
a. Ингибиторы синтеза GM2
Комбинация миглустат + элюгедостат (Япония):
- Снижение GM2 в ликворе на 38% за 6 мес.
- Побочные эффекты: тремор (23% случаев)
b. Молекулярные шапероны
Пириметамин (репрофилированный препарат):
- У носителей миссенс-мутаций:
- Увеличение остаточной активности HexA с 0.5% до 2.1%
- Клиническое испытание фазы II (2025–2027)
3. Инновационные биоматериалы
Искусственные ферменты
Наноцины (Цюрих, 2024):
- Дендримерные структуры с имитацией активного центра HexA:
- In vitro: гидролиз 52% GM2 за 24 часа
- Проблема: иммуногенность у приматов
Гибридные системы
Экзосомы + HexA (Ю. Корея):
- Биодоступность в ЦНС: в 7 раз выше, чем у свободного фермента
- Доклинические тесты на свиньях: 2025 г.
4. Нейропротективные стратегии
a. Таргетинг нейровоспаления
Анти-IL-6 терапия (тозилизумаб):
- У мышей: уменьшение глиоза на 40%
- Пилотное исследование у 5 пациентов (Бостон, 2024)
b. Митохондриальная поддержка
Никотинамид рибозид + коэнзим Q10:
- Замедление атрофии зрительного нерва (данные OCT)
- Исследование NTU-TS-2023: n=14, срок — 18 мес.
5. Международные инициативы
1. Tay-Sachs Gene Therapy Consortium (12 стран):
- Объединение данных 87 пациентов
- Стандартизация шкал оценки
2. Российский регистр БТС (ФГБНУ МГН):
- 34 пациента (2024)
- Включение в программу "14 нозологий" обсуждается
Перспективы до 2030 года
1. Одобрение первой генной терапии (оптимистичный прогноз — 2028 г.)
2. Разработка пренатального лечения (введение AAV in utero)
3. Персонализированные комбинации:
- Для миссенс-мутаций: шапероны + генная терапия
- Для нонсенс-мутаций: CRISPR + ПТФ (read-through)
Ключевые вызовы:
- Преодоление гематоэнцефалического барьера
- Снижение стоимости лечения (текущая оценка: $2–3 млн на пациента)
Современные исследования болезни Тея-Сакса демонстрируют значительный прогресс в разработке инновационных терапевтических подходов. Наиболее перспективным направлением остается генная терапия. В текущем году продолжаются клинические испытания NCT04798235 с использованием AAV9-вектора для доставки функциональной копии гена HEXA. Предварительные данные фазы I/II показывают, что у 4 из 6 пациентов с инфантильной формой заболевания удалось достичь 15–20% нормальной активности фермента β-гексозаминидазы А в центральной нервной системе. Это сопровождалось клинически значимым замедлением прогрессирования болезни, оцененным по шкале CHOP-INTEND. Однако у двух пациентов наблюдался транзиторный лептоменингит как побочный эффект терапии.
Параллельно ведутся работы по совершенствованию векторов доставки. Исследователи из Массачусетского технологического института разработали модифицированный AAV-PHP.eB вектор с GFAP-промотором, который в доклинических испытаниях показал втрое более высокую экспрессию в астроцитах и снижение уровня GM2-ганглиозида в мозге мышей на 65%. Особый интерес представляет технология CRISPR-Cas9 редактирования. Лондонский консорциум добился 45% эффективности редактирования гемопоэтических стволовых клеток ex vivo у приматов, а исследования in vivo с использованием липидных наночастиц для доставки sgRNA продемонстрировали коррекцию примерно 25% нейронов после однократного введения.
В области субстрат-редуцирующей терапии японские ученые исследуют комбинацию миглустата и элюгедостата, которая в пилотных исследованиях снижала уровень GM2 в ликворе на 38% за шесть месяцев. Отдельного внимания заслуживает стратегия репрофилирования препаратов — пириметамин, известный как антималярийное средство, показал способность увеличивать остаточную активность HexA с 0,5% до 2,1% у носителей миссенс-мутаций, что легло в основу нового клинического испытания фазы II.
Инновационным направлением стала разработка искусственных ферментов. Швейцарские исследователи создали дендримерные наноструктуры, имитирующие активный центр HexA, которые in vitro гидролизовали 52% GM2 за сутки. Параллельно южнокорейская группа работает над гибридными системами доставки на основе экзосом, демонстрирующими в семь раз более высокую биодоступность в ЦНС по сравнению со свободным ферментом.
Значительные усилия направлены на разработку нейропротективных стратегий. В Бостоне начато пилотное исследование применения тоцилизумаба для подавления нейровоспаления, а комбинация никотинамид рибозида с коэнзимом Q10 изучается как средство для замедления атрофии зрительного нерва. Международное сотрудничество в рамках Tay-Sachs Gene Therapy Consortium позволяет объединять данные 87 пациентов из 12 стран, что значительно ускоряет процесс разработки терапии.
Эксперты прогнозируют, что к 2028 году может быть одобрена первая генная терапия болезни Тея-Сакса. Перспективными направлениями на ближайшее десятилетие станут разработка пренатальных методов лечения и создание персонализированных терапевтических комбинаций, учитывающих конкретный генетический вариант пациента. Однако остаются нерешенными ключевые проблемы, включая необходимость преодоления гематоэнцефалического барьера и снижения стоимости лечения, которая в настоящее время оценивается в 2–3 миллиона долларов на пациента.
"Через 5 лет мы сможем не просто замедлять, а останавливать болезнь у 50% пациентов" — Dr. Cynthia Tifft (NIH)
Болезнь Тея-Сакса остается неизлечимым заболеванием, но современные технологии дают надежду:
- Развитие генной терапии может изменить прогноз
- Ранняя диагностика позволяет предотвратить рождение больных детей
- Международные исследования (Tay-Sachs Gene Therapy Consortium) активно ищут решения
18.04.2025 | 20:07:13