Миокардит у больных COVID-19
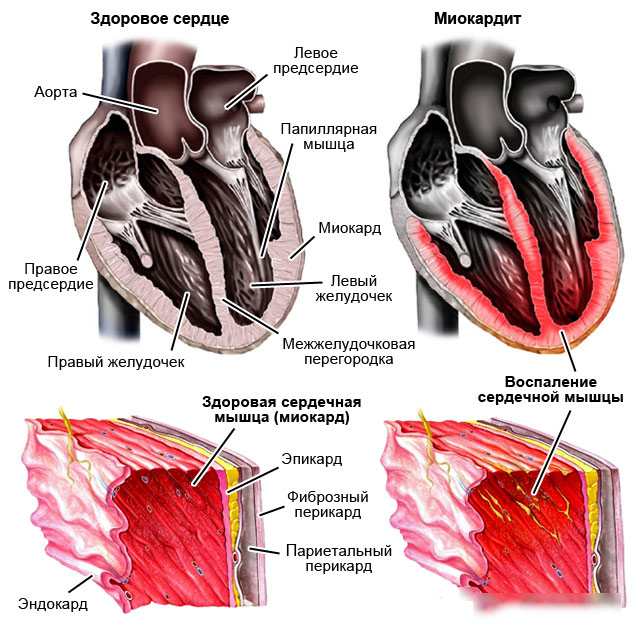
Наличие большого количества АПФ2-рецептора к вирусу SARS-CoV-2 в миокарде позволяет предполагать и прямое повреждающее действие вируса на кардиомиоциты с последующими структурными изменениями. Á. Irabien-Ortiz (2020) и соавт. предполагают еще один механизм повреждения миокарда под действием цитокинов и антител, то есть цитокиновое повреждение миокарда. Следует признать, что о прижизненной верификации коронавируса в кардиомиоцитах в эндомиокардиальном биоптате сообщается к настоящему времени только в одной работе (Felicitas Escher, 2020). Поводом для эндомиокардиальной биопсии у 104 пациентов, включенных в это исследование, было клиническое подозрение на дебют миокардита или диагностический поиск причин развития выраженной НК при отсутствии коронарной патологии. У пяти из 104 пациентов в ткани биоптата был обнаружен геном SARS-CoV-2. Еще в одной работе (Wichmann D., 2020) анализировались вопросы, связанные с тромбозом глубоких вен голени и ТЭЛА. В ходе посмертного анализа определялась вирусная РНК в ткани легкого (средний уровень составил 1,2×104-9×109 копий/мл); у 5 из 12 исследуемых вирусная РНК была обнаружена в ткани печени, почек и миокарде. В четырех случаях вирусная РНК обнаружена в ткани мозга. Интересно, что эти, по сути, единичные работы, указывающие на присутствие вируса в миокарде, представлены на фоне десятков исследований, подтвердивших присутствие вирусной РНК в ткани легких, плазме и ротоносоглотке. Изучение этой проблемы в настоящий период не может дать однозначный ответ на вопрос, существует ли длительная персистенция вируса в миокарде либо роль вируса совершенно иная - повреждение клетки, запуск воспаления и быстрая элиминация? В контексте приведенных данных также неясно, какой термин следует использовать при описании процессов, происходящих в миокарде на фоне инфицирования SARS-CoV-2: «острое повреждение миокарда» или правомочен термин «миокардит»? Тем не менее термин «миокардит» довольно часто используется при описании клинических случаев. Так, в работе S. Sala (2020) приведено описание миокардита у 43-летней пациентки с верифицированным инфицированием SARS-CoV-2, имевшей в момент госпитализации SpO2 89%, уровень высокочувствительного тропонина 135-107-106 нг/л (норма <14), подъем сегмента ST в V1-V2 и реципрокное снижение ST V4-V6. Интервал Q-Tc 452 ms, СРП 18 мг/л, NT-proBNP 512 пг/мл (норма <15), ФВ=43%. Госпитализирована на 3-и сутки недомогания, проявлявшегося в чувстве тяжести в грудной клетке и нехватки воздуха. С учетом гипокинеза в базальном отделе миокарда и отсутствия патологии в коронарных артериях трактовалась как больная с синдромом такоцубо. Однако выполненная на 7-й день эндомиокардиальная биопсия выявила воспалительные инфильтраты T-лимфоцитов (CD3+ >7/мм2), что позволило установить диагноз «миокардит» (вируснегативный лимфоцитарный миокардит), геном SARS-CoV-2 в биоптате не был обнаружен. В работе Е.А. Коган (2020) изучены аутопсийные материалы 5 пациентов пожилого возраста с COVID-19 и двусторонней полисегментарной пневмонией тяжелого течения (стадии 3-4 по КТ) При иммуногистохимическом исследовании с типированием клеточного инфильтрата подтверждены наличие CD3-позитивных Т-лимфоцитов, повышенная экспрессия рецепторов TLR-4. Во всех случаях выявлена картина коронарита, в том числе с тромбированием микрососудов. Таким образом, доказана возможность развития лимфоцитарного вирусного миокардита при COVID-19. В работе G. Tavazzi описано клиническое наблюдение за 69-летним пациентом, госпитализированным на 4-е сутки стойкой лихорадки, кашля и слабости. В день госпитализации верифицирован ПЦР-реакцией вирус SARS-CoV-2. На КТ грудной клетки - двустороннее интерстициальное поражение легочной ткани. СРБ - 52,7 мг/л, высокочувствительный тропонин I - 4332 нг/л, ФВ ЛЖ - 34%, в течение часа снизившаяся до 25%, гипотензия (АД систолическое 80/67/60 мм рт.ст.). Коронарные артерии без патологии. Начата V-A ЭКМО, на 5-е сутки полностью восстановлена гемодинамика, однако через 12 дней пациент скончался от нозокомиальной инфекции. Уникальность этого наблюдения заключается в том, что пациенту прижизненно была выполнена эндомиокардиальная биопсия, анализ которой позволил установить наличие в интерстиции миокарда единичных и небольших групп вирусных частиц размером 70-120 нм. В кардиомиоцитах вирусных частиц не обнаружено. В целом отмечены невыраженное воспаление в миокарде и отсутствие полей некроза. (Эти изменения практически идентичны изменениям в миокарде при инфицировании MERS-CoV Middle East respiratory syndrome-related coronavirus, MERS-CoV- Ближневосточный респираторный синдром) Известно, что вирусные частицы SARS-CoV-2 обнаружены не только в альвеолярных макрофагах, но и в ряде других тканей: проксимальном канальце нефрона, макрофагах, инфильтрирующих мышцы, селезенке, ЛУ, печени, почке, мышцах и других тканях. Наличие вирусных частиц в интерстиции миокарда авторы объясняют миграцией альвеолярных макрофагов из легочной ткани в другие органы и ткани, считая что таргетными клетками для вируса являются альвеолярные макрофаги. Отсутствие вирусных частиц в кардиомиоцитах, по мнению авторов, позволяет усомниться в кардиотропизме вируса, хотя, бесспорно, требуется подтверждение этого факта в других работах.
Таким образом, гистологическая и гистохимическая картины позволяют идентифицировать изменения в миокарде как миокардит, развивающийся на фоне инфицирования SARS-CoV-2. Отличительными особенностями миокардита при COVID-19 являются наличие коронарита и возможность сочетания миокардита с лимфоцитарным эндо- и перикардитом, а также (предварительные данные) отсутствие вирусных частиц в кардиомиоцитах. Можно предполагать, что ведущим механизмом повреждения миокарда, по-видимому, является тромбоз на различных уровнях сосудистого русла.
Для повседневной практики представляет особый интерес анализ частоты развития миокардитов у больных, инфицированных SARS-CoV-2. К сожалению, точного ответа на этот вопрос в настоящее время не существует. В самом первом обсервационном исследовании Shaobo Shi (включено 416 пациента, поступивших в госпиталь Wuhan University с 20.01.20 по 10.02.20) установлено, что у 82 (19,7%) пациентов развилось повреждение миокарда. Сопоставление уровней высокочувствительного тропонина и NT-proBNP у пациентов с повреждением миокарда и без него выявило их достоверное различие (0,19 [0,08-1,12] vs <0,006 [<0,006-0,009] μg/L и 1689 [698-3327] vs 139 [51-335] пг/ мл). В группе пациентов с повреждением миокарда достоверно
чаще возникала необходимость в переводе на искусственную вентиляцию легких и была достоверно выше частота летальных исходов (42 из 82 (51,2%) vs 15 из 334 (4,5%); p <0,001). В другом китайском популяционном исследовании (Tao Guo - 7th Hospital of Wuhan City, включены 187 пациентов в период с 23.01.20 по 23.02.20) повреждение миокарда диагностировалось по повышению уровня тропонина Т (TnT). Поражение миокарда зафиксировано у 52 из 187 пациентов, что составило 27,8%. Повышенный уровень тропонина Т был предиктором летального исхода, особенно значимо повышая риск летального исхода в группе пациентов с предшествующей инфицированию SARS-CoV-2 коронарной болезнью сердца (13,3% смертности при нормальном уровне тро-понина Т vs 69,44% при повышенном уровне тропонина Т и предшествующей коронарной болезни сердца). Авторы этих работ предположили, что пациенты имевшие прижизненно высокий уровень тропонина и умершие в остром периоде болезни, имели фульминантный миокардит, хотя результаты посмертного исследования миокарда, которые могли бы подтвердить или опровергнуть это предположение, в работах не приводятся. В ряде других работ отмечена частота поражения миокарда, равная 12-22%. Как видно из приведенных данных, повреждение миокарда, идентифицируемое в исследованиях как миокардит, диагностировалось по повышенному уровню тропонина, что, бесспорно, приводит к завышенной прижизненной оценке частоты этого события. Достаточно отметить, что посмертное исследование миокарда выявляет признаки миокардита существенно реже. В работе M.K. Halushka (2020) проанализированы данные посмертного исследования миокарда 277 пациентов, умерших от COVID-19 (по данным, опубликованным в 22 статьях). Гистологические признаки миокардита отмечены в 20 случаях, что составило 7,2%. Последующий повторный анализ показал, что случаи, не вызывающие сомнения в отношении миокардита, составили менее 2%, а изменения в миокарде, типичные для COVID-19, - макро- и микроваскулярные тромбозы - отмечены в 47,8%. Именно эти изменения, по-видимому, и стали причиной повышения уровня тропонина в абсолютном большинстве случаев. Исчезают ли повреждения в миокарде, возникшие в остром периоде COVID-19, совместно с основными клиническими проявлениями или сохраняются и после выздоровления от COVID-19? Существует исследование V.O. Puntmann (2020) - проспективное, обсервационное, когортное, в которое включено 100 пациентов из регистра COVID-19 Registry, либо выписанных из университетского госпиталя Франкфурта в период апрель - июнь 2020 г. (33% пациентов), либо в этот же период проходивших лечение в домашних условиях. Группа сравнения - идентичные по возрасту и полу здоровые добровольцы. Всем пациентам выполняли МРТ сердца ( в среднем на 71-й день [64-92]) и измеряли уровень высокочувствительного тропонина. В день проведения МРТ уровень тропонина Т у 71% пациентов был выше 3 пг/мл, а у 5% был выше 13,9 пг/мл). У 78 пациентов отмечены патологические изменения на МРТ (T1 и Т2-взвешенные изображения. T1-взвешенные изображения оптимально показывают анатомию и жир нормальных мягких тканей (например, для подтверждения жиросодержащей массы). Т2-взвешенные изображения оптимально показывают жидкости и аномалии (например, опухоли, воспаления, травмы). У 73 пациентов отмечалось увеличение T1, у 60 пациентов увеличение Т2-взвешенных изображений. Таким образом, у 60% пациентов сохранялось воспаление в миокарде. Эндомиокардиальная биопсия, выполненная пациентам с выраженными изменениями в миокарде, подтвердила наличие лимфоцитарной воспалительной инфильтрации. Достоверно различались группы пациентов, госпитализированных и проходивших лечение на дому. У госпитализированных пациентов были выявлены существенно большие изменения в миокарде. Эти данные позволяют утверждать, что изменения в миокарде, возникшие в остром периоде COVID-19, имеют тенденцию сохраняться довольно долгий промежуток времени.
Специфичных для миокардита жалоб у пациентов, инфицированных SARS-CoV-2, нет. В метаанализе L. Li (включено 1995 пациентов) установлено, что самыми частыми жалобами являются лихорадка - 88,5%, кашель - 68,6% и одышка - 21,9%, слабость - 35,8%. По данным анализа, выполненного в госпитале Wuhan, боли в грудной клетке отмечены в 3,4%.
Важный факт заключается в том, что у пациентов с повышенным уровнем тропонина боли в грудной клетке встречаются достоверно чаще, чем у пациентов с нормальным уровнем тропонина (у 11 из 82 пациентов (13,4%) vs 3 из 334 пациентов (0,9%); p <0,001. Не существует специфических маркеров для лабораторной диагностики миокардита у инфицированных SARS-CoV-2. Повышенный уровень высокочувствительного тропонина I, по данным F. Zhou, на 4-й день болезни свидетельствует о повреждении миокарда и о высоком риске летального исхода (8,8 пг/мл в популяции умерших пациентов vs 2,5 пг/мл у выживших), но не является абсолютным признаком обязательного наличия у пациента миокардита. Точно так же повышенный уровень NT-proBNP не является абсолютным признаком обязательного наличия у пациента миокардита. В работе J. He проанализированы изменения на ЭКГ у больных COVID-19 (в работе представлен анализ клинических случаев). Установлено, что в период манифеста болезни отмечались нарушения проводимости - атриовентрикулярной и блокады ножек пучка Гиса, вентрикулярные тахикардии, изменения сегмента ST. В более крупном анализе F. Angeli проанализированы изменения на ЭКГ у 50 пациентов с COVID-19. Отмечено, что у 30% изменения проявились в подъеме сегмента ST и изменениях зубца Т, у 26% пациентов отмечены пароксизмы фибрилляции предсердий и развитие синдрома тахи-бради, в нескольких случаях развился конкордантный подъем сегмента ST (картина, идентичная изменениям при перикардите). Как видно из приведенных данных, специфичных для миокардита изменений на ЭКГ не зафиксировано. Canadian Society of Echocardiography рекомендует выполнять ЭхоКГ всем пациентам с COVID-19 в качестве рутинного теста. Оценка в динамике объемов камер сердца и сократительной способности миокарда позволит оптимизировать диагностический поиск. Диагностическим методом выбора является МРТ сердца. Society for Cardiovascular Magnetic Resonance в рекомендациях по ведению больных COVID-19 (Han Y., 2020) отмечает, что МРТ сердца обладает наиболее высокой чувствительностью в выявлении острого миокардита, а совпадение по площади участков позднего контрастирования и отека миокарда позволяют дифференцировать острый и хронический воспалительный процесс в миокарде. Критерии Lake Louise (диагностика миокардита базируется как минимум на одном критерии Т1: увеличение времени релаксации, экстра-целлюлярного объема и как минимум одном критерии Т2: увеличение времени релаксации, визуальный отек миокарда) имеют специфичность 91% и чувствительность 67% в диагностике миокардитов. Эндомиокардиальная биопсия рекомендуется, но не является обязательной процедурой в диагностическом поиске пациентов с COVID-19, госпитализированных в реанимационные отделения (Pirzada A., 2020).
Таким образом, диагностика миокардита у пациента с COVID-19 - трудная задача, требующая комплексной оценки инструментальных, лабораторных и клинических данных. Попытки диагностировать миокардит по одному критерию - как правило, по повышенному уровню тропонина - приводят к гипердиагностики миокардитов.
Лечение миокардитов у больных COVID-19 - трудная и нерешенная задача. Препарат ремдесивир, новый противовирусный препарат в классе нуклеотидных аналогов, в исследовании Remdesivir for the Treatment of Covid-19 - Final Report (John H. Beigel, 2020) был испытан у 1062 пациентов (541 получали ремдесивир). По сравнению с плацебо препарат снижал количество дней до выздоровления (медианное время выздоровления с 15 до 10 дней RR=1,29; 95% CI, 1,12-1,49; р <0,001). Препарат также продемонстрировал тенденцию (!) к снижению смертности. Смертность на препарате на 15-й день наблюдения составила 6,7 vs 11,9% в группе плацебо, а на 29-й день наблюдения - 11,4 vs 15,2% (HR=0,73; 95% CI, 0,52-1,03), при этом количество побочных эффектов было ниже в группе ремдесивира. На основании этих данных Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (U.S. Food and Drug Administration) 1 мая 2020 г. выдало в упрощенном порядке «разрешение для экстренного использования» ремдесивира для лечения COVID-19 в США. Предполагалось, что препарат будет назначаться всем пациентам с COVID-19, в том числе и пациентам с миокардитом. На момент написания этого раздела препарат входит в рекомендации по лечению COVID-19 в Европе и РФ. Однако исследование SOLIDARITY (многонациональное клиническое исследование III-IV фазы, организованное ВOЗ в 500 клиниках 30 стран с целью сравнить клинический эффект четырех непроверенных методов лечения пациентов с тяжелой формой COVID-19: 2750 пациентов получали лечение ремдесивиром 200 мг нагрузочная доза, затем по 100 мг в/в 10 дней; 954 получали лечение гидроксихлорохином; 1141 - лопинавир + ритонавир; 2063 - интерферон бета-1a; 4098 - плацебо) установило, что ни один из препаратов не был эффективнее плацебо, что поставило под сомнение эффективность и ремдесивира. В исследовании RECOVERY (Randomised Evaluation of COVID-19 Therapy) анализировалась эффективность потенциальных методов лечения больных COVID-19: стандартный уход без дополнительных методов лечения (стандартное стационарное лечение); комбинация лопинавира и ритонавира; дексаметазона в низких дозировках; гидроксихлорохин; азитромицин; тоцилизумаб; плазма выздоровевших - с целью введения готовых антител против вируса SARS-CoV-2; внутривенный иммуноглобулин (детская ветвь лечения). Единственная ветвь исследования, доказавшая эффективность, - применение дексаметазона. Установлено, что в группе применения малых доз дексаметазона на 28-й день наблюдения умерли 482 пациента (22,9%) (в группе сравнения - 1110 пациентов [25,7%]), что достоверно снижает риск на 17% (RR=0,83, CI 0,75-0,93; p <0,001). Субанализ в группе леченных дексаметазоном показал, что наибольший эффект отмечен у пациентов, переведенных на искусственную вентиляцию легких - 29,3% летальных исходов в группе лечения vs 41,4% в группе сравнения (RR=0,64. CI 0,75-0,93; p <0,001). Эффект препарата отмечен и в группе пациентов, нуждавшихся в ингаляции кислорода 23,3 vs 26,2% (RR=0,82; 95% CI, 0,72-0,94). Однако препарат не оказывал никакого влияния на пациентов с легким течением болезни, то есть не нуждавшихся в респираторной поддержке, - 17,8 vs 14,0% (RR=1,19; 95% CI 0,91-1,55). С учетом того, что гормональная терапия не рекомендована для лечения вирусных миокардитов, а препарат ремдесивир, по-видимому, не обладает клинической эффективностью, в настоящее время (Review Update on COVID-19 Myocarditis) рекомендовано в лечении миокардитов у больных COVID-19 следовать рекомендациям по лечению ХСН и использовать иАПФ/сартаны/АРНИ, β-адреноблокаторы, антагонисты минералокортикоидных рецепторов, диуретики. С целью коррекции нарушений ритма рекомендованы β-адреноблокаторы и амиодарон (следует помнить о его проаритмогенном эффекте - удлиняет интервал Q-T, особенно в комбинации с азитромицином). Фульминантный миокардит требует инотропной поддержки, в том числе и экстракорпоральной, а также применения ЭКМО (ELSO Guidance Document: ECMO for COVID-19 Patients with Severe Cardiopulmonary Failure). Прогноз больных миокардитом в настоящее время остается тяжелым.
Источник: Внутренние болезни: избранные лекции: учебное пособие / Г. П. Арутюнов, А. Г. Арутюнов. - Москва: ГЭОТАР-Медиа, 2022
02.05.2022 | 21:16:41