Хронический панкреатит.
Содержание
Определение
Эпидемиология
Профилактика хронического панкреатита
Скрининг
Классификация хронического панкреатита
Этиология
Патогенез хронического панкреатита
Клиническая картина
Диагностика хронического панкреатита
- Анамнез
- Физикальное обследование
- Лабораторные исследования
- Инструментальные исследования
- Диагностика и диагностические алгоритмы
Дифференциальная диагностика
Показания к консультации специалистов
Примеры формулировок диагноза
Лечение хронического панкреатита
- Немедикаментозное лечение
- Медикаментозное лечение хронического панкреатита
- Хирургическое лечение хронического панкреатита
Примерные сроки нетрудоспособности
Дальнейшее ведение
Прогноз
Термином «хронический панкреатит» обозначают группу хронических заболеваний поджелудочной железы различной этиологии, преимущественно воспалительной природы, с фазово-прогрессирующими очаговыми, сегментарными или диффузными дегенеративными, деструктивными изменениями ее экзокринной части, атрофией железистых элементов (панкреоцитов) и замещением их соединительной (фиброзной) тканью; изменениями в протоковой системе ПЖ с образованием кист и конкрементов, с различной степенью нарушения экзокринной и эндокринной функций.
Нарушения инкреторной и внешнесекреторной функции ПЖ у больных с ХП, а также рак ПЖ (РПЖ) можно считать вероятными исходами заболевания.
Коды по МКБ-10
К86.0. Хронический алкогольный панкреатит.
К86.1. Другие хронические панкреатиты.
В структуре заболеваемости органов желудочно-кишечного тракта ХП составляет от 5,1 до 9%, а в общей клинической практике - от 0,2 до 0,6%. За последние 30 лет отмечена общемировая тенденция к увеличению заболеваемости ХП более чем в 2 раза. Если в 80-е годы заболеваемость ХП составляла 3,5-4,0 на 100000 населения в год, то в последнее десятилетие отмечена общемировая тенденция роста частоты этого заболевания до 8,2-10 на 100000 населения.
В России отмечен более интенсивный рост заболеваемости ХП как среди взрослого, так и детского населения. У детей этот показатель составляет 9-25, у взрослых - 27,4-50 случаев на 100000 населения. Распространенность заболеваний ПЖ среди взрослых за последние 10 лет увеличилась в 3 раза, в то время как у подростков данный показатель вырос более чем в 4 раза.
С учетом роли пищевых факторов в первичной профилактике ХП необходимо следовать алгоритму рекомендаций по здоровому питанию:
• употребление разнообразной пищи;
• баланс количества принимаемой пищи с физической активностью;
• поддержание нормальной массы тела;
• выбор рациона с большим количеством зерновых продуктов, овощей и фруктов;
• выбор пищи с низким содержанием жира, насыщенных жиров и холестерина;
• выбор пищи с умеренным содержанием сахара;
• выбор пищи с умеренным содержанием поваренной соли;
• исключение содержащих алкоголь напитков, отказ от курения.
Диспансерное наблюдение за больными с хроническим панкреатитом в поликлинике осуществляют терапевт и гастроэнтеролог, с четким соблюдением преемственности между ними, а при необходимости и хирург. Больных после операции на поджелудочной железе наблюдают так же, как и больных с ХП.
Основной алгоритм наблюдения за больными по программе реабилитации: активный вызов 2-4 раза в год в зависимости от тяжести заболевания. Больных с легким течением хронического панкреатита наблюдает участковый терапевт 2 раза в год. Больные с ХП средней тяжести и с тяжелым течением должны быть на активном наблюдении у гастроэнтеролога. Контрольное обследование проводят 3-4 раза в год. При визитах должна быть проведена оценка общего состояния, жалоб и физикальных данных. Необходимы контрольные обследования, включая исследования в динамике активности ферментов ПЖ в сыворотке крови, концентрации глюкозы плазмы крови, скрининг синдромов мальдигестии и мальабсорбции (полное копрологическое исследование, исследование кала на эластазу 1), проведение УЗИ ПЖ и желчевыводящей системы.
В зависимости от полученных данных проводят курсы противорецидивного лечения, дието- и фитотерапии.
При компенсации хронического процесса, благоприятной динамике и отсутствии обострений в течение 5 лет больных с ХП можно снять с диспансерного наблюдения. Это, как правило, подходит больным с так называемыми вторичными ХП, если устранена их причина (холелитиаз, стеноз БДС и др.).
Больные с хроническим панкреатитом с экскреторной и инкреторной недостаточностью, пациенты, перенесшие оперативное вмешательство на ПЖ, подлежат пожизненной (бессрочной) диспансеризации.
В профилактике обострений хронического панкреатита большое значение имеют своевременная санация желчевыводящих путей с устранением дисфункциональных расстройств, раннее выявление калькулезного холецистита и своевременное оперативное лечение. У пациентов с доброкачественным стенозом БДС или терминального отдела общего желчного протока и устья протока ПЖ проводят ЭПСТ.
УЗИ показано пациентам с повышенной вероятностью развития хронического панкреатита и рака ПЖ: злоупотребляющим алкоголем, курящим, с несбалансированным рационом питания, с нарушением режима питания, имеющим заболевания билиарного тракта и гастродуоденальной зоны, предъявляющим жалобы на ощущение дискомфорта в левой подреберной и эпигастральной областях, опоясывающие боли, с проявлениями диспепсии, снижением массы тела.
Вторичную профилактику ХП, направленную на устранение факторов, способствующих его рецидивированию или прогрессированию, проводят в рамках диспансерного наблюдения.
По морфологическим признакам:
• интерстициально-отечный;
• паренхиматозный хронический панкреатит;
• фиброзно-склеротический (индуративный);
• гиперпластический (псевдотуморозный) хронический панкреатит;
• кистозный хронический панкреатит.
По клиническим проявлениям:
• болевой вариант;
• гипосекреторный;
• астеноневротический (ипохондрический);
• латентный;
• сочетанный.
По характеру клинического течения:
• редко рецидивирующий;
• часто рецидивирующий;
• персистирующий.
По этиологии:
• билиарнозависимый;
• алкогольный хронический панкреатит;
• дисметаболический (сахарный диабет, гиперпаратиреоз, гиперхолестеринемия, гемохроматоз);
• инфекционный;
• лекарственный хронический панкреатит;
• идиопатический хронический панкреатит.
Осложнения:
• нарушения оттока желчи;
• портальная гипертензия (подпеченочная форма);
• инфекционные (холангит, абсцессы);
• воспалительные изменения (абсцесс, киста, парапанкреатит, ферментативный холецистит, эрозивный эзофагит, гастродуоденальные кровотечения, в том числе синдром Мэллори-Вейса, а также пневмония, выпотной плеврит, острый респираторный дистресс-синдром, паранефрит, острая почечная недостаточность);
• эндокринные нарушения (панкреатогенный сахарный диабет, гипогликемические состояния).
По этиологии все ХП делят на первичные и вторичные. К первичным панкреатитам относят формы, когда ПЖ - это орган-мишень, ее поражение первично (токсико-метаболический, наследственный, аутоиммунный, идиопатический). Вторичные панкреатиты развиваются вследствие патологии других органов (чаще органов пищеварения) или как одно из проявлений заболевания, поражающего ряд органов и систем.
Основные этиологические факторы приведены в представленной выше классификации ХП и несколько расширены в более поздней международной классификации TIGAR-O.
• Токсико-метаболический хронический панкреатит:
❖ алкоголь;
❖ курение;
❖ медикаменты;
❖ токсины;
❖ гиперкальциемия;
❖ гиперпаратиреоидизм;
❖ гиперлипидемия;
❖ ХПН;
❖ сахарный диабет.
• Идиопатический хронический панкреатит:
❖ ранний и поздний идиопатический ХП;
❖ тропический ХП.
• Наследственный хронический панкреатит.
• Аутоиммунный хронический панкреатит.
• Рецидивирующий и тяжелый ОП:
❖ постнекротический тяжелый;
❖ рецидивирующий;
❖ сосудистые заболевания;
❖ постлучевой.
• Обструктивный хронический панкреатит:
❖ pancreas divisum;
❖ патология сфинктера Одди;
❖ протоковая обструкция (например, опухолью);
❖ периампулярные кисты стенки ДПК;
❖ посттравматические рубцовые изменения главного панкреатического протока (ГПП).
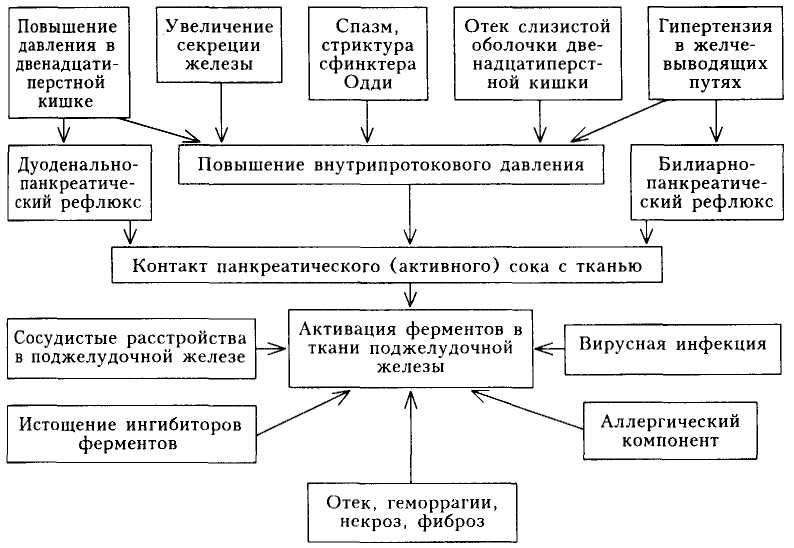

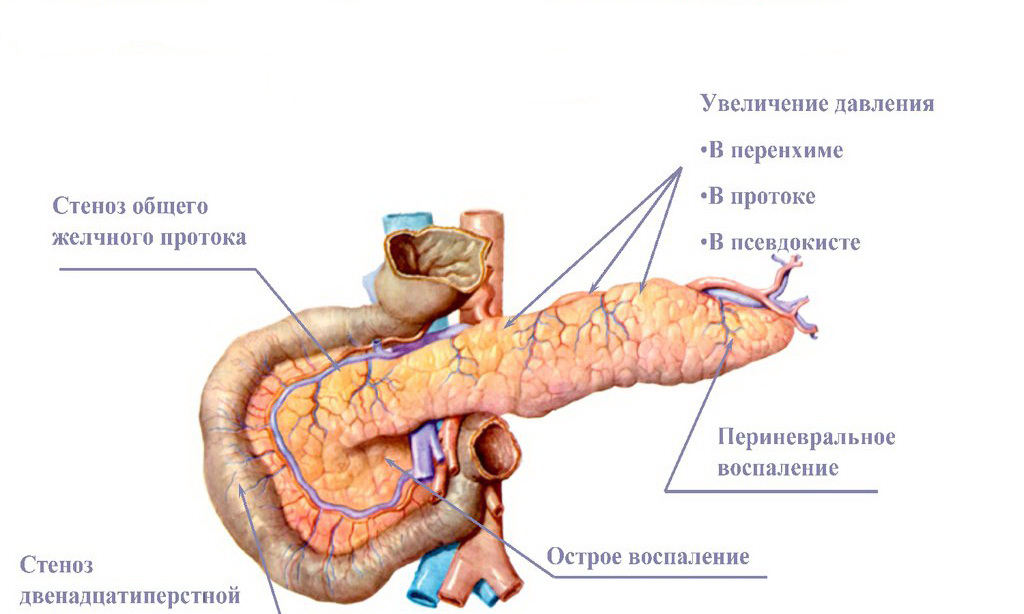
С учетом полиэтиологичности ХП патогенез этого заболевания имеет определенные особенности в зависимости от этиологического фактора. Существуют доказанные экспериментальные модели алкогольного, наследственного, обструктивного, аутоиммунного ХП. Общее для всех этиологических форм заболевания:
• очаговые фазовые деструктивные изменения за счет экзогенных факторов (алкоголя и т.п.), протоковой гипертензии (обструкции, отека), интрапанкреатической активации проферментов;
• воспалительная инфильтрация паренхимы ПЖ;
• прогрессирующий фиброз паренхимы;
• развитие экзо- и эндокринной панкреатической недостаточности.
Клиническая картина панкреатитов полиморфна в связи с полиэтиологичностью этого заболевания и частым вовлечением в патологический процесс соседних органов. Ведущие синдромы: болевой абдоминальный синдром и синдромы экзо- и эндокринной панкреатической недостаточности. Клиническая картина ХП в значительной степени определяется длительностью персистирования симптомов и тяжестью заболевания. Именно поэтому выделяют три периода течения.
Начальный период (чаще до 10 лет течения заболевания), характеризуемый чередованием периодов обострения и ремиссии. Основные проявления обострения - боли разной интенсивности и локализации. Диспептический симптомокомплекс если и бывает, то носит явно сопутствующий характер и купируется при лечении в первую очередь.
Второй период - стадия внешнесекреторной недостаточности ПЖ (чаще после 10 лет течения заболевания). Боли уступают свое место диспептическому симптомокомплексу (желудочному и кишечному). Симптомы желудочной диспепсии связаны с частыми явлениями дуоденостаза, гастроэзофагеального рефлюкса; симптомокомплекс кишечной диспепсии возникает на фоне синдрома мальдигестии, появляются моторные нарушения кишечника. Болевой абдоминальный синдром становится менее выразительным или его может не быть. Вследствие развившегося синдрома мальабсорбции прогрессирует трофологическая недостаточность.
Осложненный вариант течения хронического панкреатита (возможно развитие в любом периоде). Происходит изменение привычного варианта клинической картины: меняется интенсивность болей, она может стать постоянной, иррадиировать, изменяться под влиянием лечения. Более упорно представлен диспептический симптомокомплекс. При формировании кист и инфекционных осложнениях изменяется обычная динамика ферментных тестов, гиперамилаземия может держаться неопределенно долго.
Наибольшие трудности вызывает анализ особенностей болевого абдоминального синдрома, поскольку боль не имеет четкой локализации, возникая в верхнем или среднем отделе живота слева или посередине, иррадиирует в спину, иногда принимая опоясывающий характер. В некоторых случаях боль исходно локализована на спине. Более чем у половины больных болевой абдоминальный синдром имеет высокую интенсивность, сохраняется длительное время. Как правило, боли усиливаются на фоне приема пищи, обычно через 30 мин (особенно при стенозировании панкреатических протоков). У части пациентов появление боли не связано с едой. Примерно у 15% больных боли отсутствуют.
В связи с отсутствем четкой специфичности болевого абдоминального синдрома при ХП предложено выделение нескольких наиболее типичных вариантов: язвенноподобного, по типу левосторонней почечной колики, синдрома правого подреберья (в 30-40% протекает с холестазом), дисмоторного болевого синдрома, распространенного болевого синдрома (без четкой локализации).
Анамнез
Поскольку клинически ХП характеризуется двумя ведущими симптомами: рецидивирующей или постоянной абдоминальной болью, экзокринной недостаточностью ПЖ (синдромом мальабсорбции, стеатореей, трофологической недостаточностью), собирая анамнез, необходимо выяснить время появления первых симптомов, проследить их динамику во времени, оценить эффективность и адекватность проводимой ранее терапии. Важнейший анамнестический аспект, на котором может базироваться клинический диагноз, - перенесенный ранее тяжелый ОП, рецидивирующий ОП (например, билиарнозависимый), поскольку в настоящее время можно считать доказанным возможность трансформации ОП в ХП, особенно при сохранении повреждающего действия этиологического фактора. Необходимо оценить семейный анамнез, изучить спектр сопутствующих заболеваний, определить наличие и выраженность экзогенных токсических воздействий, что может помочь в установлении этиологии заболевания.
Физикальное обследование
Общее состояние больного может быть различным - от удовлетворительного до крайне тяжелого, что зависит от выраженности болевого синдрома, симптомов интоксикации, степени белково-энергетической недостаточности, нарушений центральной и периферической гемодинамики. Состояние питания весьма вариабельно. Язык обложен, иногда суховат.
При поверхностной пальпации можно определить болезненность в эпигастрии, левом подреберье. При глубокой пальпации выявляют болезненность в проекции ПЖ. Проекцию ПЖ на переднюю брюшную стенку определяют следующим образом: срединную линию от мечевидного отростка до пупка делят на трети. Между верхней и средней третями проводят горизонтальную линию - влево до левой реберной дуги, вправо - вдвое меньше, чем влево, т.е. 2/3 горизонтальной линии находятся слева, а 1/3 - справа. Резистентности в проекции ПЖ обычно нет, так как она расположена забрюшинно. Болезненность в зоне Шоффара и точке Дежардена условно свидетельствует о патологии головки ПЖ, в зоне М. Губергрица-Скульского и в точке А. Губергрица тела ПЖ.
Дополнительное значение имеют следующие симптомы:
• боль при надавливании в левом реберно-позвоночном углу (точка Мейо-Робсона) свидетельствует о патологии хвоста ПЖ;
• симптом Мюсси слева - боль при надавливании между ножками грудино-ключично-сосцевидной мышцы у прикрепления к медиальному краю ключицы;
• симптом Ниднера - при пальпации всей ладонью хорошо определяется пульсация аорты в левом подреберье из-за давления на нее ПЖ;
• симптом Воскресенского - отсутствие пульсации брюшной аорты. Этот симптом неблагоприятен, так как свидетельствует о значительном увеличении ПЖ, которая прикрывает аорту.
Лабораторные исследования
Лабораторная диагностика хронического панкреатита основана на определении активности ферментов ПЖ в крови и моче, диагностике экзо- и эндокринной недостаточности. Дополнительно проводят комплексное биохимическое и общеклиническое исследование крови.
Исследование содержания панкреатических ферментов в крови и моче.
Определение уровня амилазы в крови и моче - наиболее распространенный диагностический тест. Невысокая чувствительность определения амилазы в крови и моче связана с кратковременностью гиперамилаземии и гиперамилазурии при панкреатитах. Например, уровень амилазы крови начинает повышаться через 2-12 ч от начала обострения заболевания, достигает максимума через 20-30 ч, нормализуется через 2-4 сут при благоприятном течении заболевания. Содержание амилазы в моче начинает повышаться через 4-6 ч от начала обострения, а через 810 ч (по некоторым данным 3 сут) уже может нормализоваться. Во многих случаях при тяжелом течении обострения ХП у больных с длительным анамнезом регистрируют нормальные или субнормальные величины амилазы. Определение содержания амилазы в моче более информативно, чем в крови, так как гиперамилазурия более стойка, чем гиперамилаземия. Прямой связи между тяжестью панкреатита и активностью амилазы в крови и моче в ряде случаев не наблюдают.
Для повышения специфичности исследования амилазы в крови (особенно у больных с нормальным содержанием общей амилазы) следует определять не суммарное содержание фермента, а панкреатическую изоамилазу. Специфичность определения панкреатической амилазы при ХП не превышает 88,6% при чувствительности 40,0-96,9%.
Определение сывороточной липазы также недостаточно чувствительно и информативно. Данные о сроках, при которых сохраняется гиперферментемия, варьируют, но они определенно больше, чем для амилазы. По сывороточному уровню липазы невозможно определить тяжесть текущего обострения панкреатита и ближайший прогноз.
Определение активности эластазы 1 в крови считают самым поздним чувствительным тестом диагностики обострений ХП, поскольку повышенный уровень фермента сохраняется в течение 8-10 дней после атаки. В этот период активность эластазы 1 в крови повышена у 100% больных, уровень липазы - у 85%, панкреатической изоамилазы - у 43%, общей α-амилазы - у 23% больных. Однако выраженность гиперэластаземии не соответствует степени деструкции ткани ПЖ и не имеет большого диагностического значения при функциональной недостаточности у больных с многолетним ХП.
Оценка экзокринной функции поджелудочной железы.
Тесты, позволяющие оценить экзокринную функцию ПЖ, разделяют на две группы: зондовые методы, требующие введения кишечного зонда, и неинвазивные беззондовые тесты.
Прямой зондовый метод - секретин-панкреозиминовый (секретин-холецистокининовый) тест. Диагностическая точность метода чрезвычайно высока; чувствительность и специфичность метода составляют более 90%. Большинство ученых признают этот тест в качестве «золотого стандарта» определения нарушений экзокринной функции ПЖ, некоторые из них считают, что проведение прямого зондового метода является обязательным при диагностике ХП. С помощью теста невозможна дифференциальная диагностика с другими заболеваниями ПЖ, поскольку при раке ПЖ, муковисцидозе и других заболеваниях ПЖ регистрируют патологические результаты этого теста в 75-90% случаев.
Интерпретация результатов зондового исследования, выделение патологических типов секреции ПЖ.
• Гипосекреторный - снижение продукции ферментов, бикарбонатов при нормальном объеме секрета. Этот тип характерен для диффузного фиброза ПЖ (поздние стадии ХП), муковисцидоза, реже определяют при раке ПЖ.
• Гиперсекреторный - нормальные или повышенные объемы секрета и дебит бикарбонатов, увеличение активности ферментов. Этот тип характерен для начальных воспалительных процессов в ПЖ без признаков атрофии ацинарных клеток и выраженного фиброза. Наблюдают в начальных стадиях ХП, при недлительной и незначительной задержке оттока секрета ПЖ (при язвенной болезни ДПК, кратковременном спазме сфинктера Одди и т.д.).
Обтурационный тип делят на 2 подтипа.
• Нижний блок - снижение объема секрета при нормальной концентрации бикарбонатов и ферментов, что приводит к снижению их дебита. Характерен для панкреатитов, развившихся вследствие процессов, затрудняющих отток секрета ПЖ (стойкого спазма сфинктера Одди, папиллитов, опухолей фатерова соска или головки ПЖ, обтурации ГПП конкрементом).
• Верхний блок - снижение объема секрета, повышение концентрации ферментов (но их дебит все же снижен), нормальное содержание бикарбонатов. Такой вариант свидетельствует об отеке ПЖ и характерен для отечного панкреатита (ОП, обострения ХП).
Дуктулярный тип - снижение объема секрета, нормальная продукция ферментов, резкое повышение концентрации бикарбонатов. Возможно, такие изменения связаны с воспалением протоков и нарушением реабсорбции бикарбонатов.
К недостаткам метода можно отнести необходимость дуоденального зондирования, обременительного для пациента, большой объем работы лаборанта, высокую стоимость и малую доступность стимуляторов ПЖ.
Чувствительность непрямого зондового метода (теста Лунда) у больных с ХП составляет 90%. Отдельные ложноположительные результаты обнаруживают у больных с тонкокишечной мальабсорбцией, целиакией, сахарным диабетом. Тест Лунда менее чувствителен на ранних стадиях внешнесекреторной недостаточности ПЖ. Он дешевле, проще в выполнении и удобнее для больного.
К недостаткам метода относят необходимость дуоденального зондирования, отсутствие возможности определения объема секреции и концентрации бикарбонатов, влияние на результаты теста интрадуоденальной кислотности и эндогенной секреции гормонов из ДПК.
Непрямые методы без дуоденального зондирования основаны на введении внутрь специфических субстратов для ферментов ПЖ. После взаимодействия последних с ферментами ПЖ в моче или сыворотке крови определяют продукты расщепления, по количеству которых судят о внешнесекреторной недостаточности ПЖ. В настоящее время успешно используют бентирамидный тест (NBT-PABA-тест) (чувствительность составляет 83%, специфичность - 89%). Принципиальный недостаток неинвазивных методов состоит в ослаблении их чувствительности при умеренно выраженной степени экзокринной панкреатической недостаточности.
Определение степени потребления плазменных аминокислот поджелудочной железой было предложено использовать для исследования ее функции у больных с тяжелой внешнесекреторной недостаточностью. Известно, что при стимуляции секретином ПЖ поглощает большое количество аминокислот из плазмы крови, необходимых для синтеза панкреатических ферментов. Чувствительность метода составляет 69-96%, специфичность - 54-100%.
Качественное копрологическое исследование проводят в условиях соблюдения больными стандартной диеты (например, диеты Шмидта, включающей 105 г белка, 135 г жира, 180 г углеводов) при условии неприменения в этот период времени полиферментных препаратов. Критерии внешнесекреторной недостаточности: повышенное содержание в кале нейтрального жира и мыл при малоизмененном содержании жирных кислот. Повышенное содержание мышечных волокон указывает на креаторею.
Количественное определение жира в кале.
В норме после приема 100 г жира с пищей за сутки выделяется до 7 г нейтрального жира и жирных кислот. Увеличение количества жира свидетельствует о расстройствах его переваривания и всасывания, чаще всего панкреатического происхождения. Определение тяжести стеатореи используют как простой и надежный показатель выраженной внешнесекреторной недостаточности ПЖ. Достоверность теста снижается при неполном (неправильном) сборе кала и на фоне неадекватной диеты, особенно у амбулаторных больных. Тест неспецифичен для целого ряда заболеваний, что не позволяет его использовать для определения панкреатического характера стеатореи. Данные теста почти всегда выходят за границы нормы при поражении подвздошной кишки и при бактериальной контаминации тонкой кишки.
За последнее десятилетие широкое распространение получил иммуноферментный метод определения эластазы 1 в кале больных с ХП. Чувствительность эластазного теста у больных с экзокринной панкреатической недостаточностью тяжелой и средней степени приближается к таковой при секретин-панкреозиминовом тесте и, по данным большинства зарубежных исследователей, составляет 90-100% (при легкой степени - 63%), специфичность - 96%. Этот метод простой, быстрый и недорогой, не имеет ограничений в применении, позволяет на более ранних стадиях, чем прежде, определять состояние внешнесекреторной функции ПЖ.
При обострении ХП в общем анализе крови может быть выражен лейкоцитоз, наблюдают сдвиг формулы влево, нейтрофилез, увеличение СОЭ. На фоне лечения отмечают быструю отчетливую редукцию лейкоцитоза, несколько позднее нормализуется значение СОЭ, что считают одним из благоприятных клинических признаков. Длительно сохраняющийся лейкоцитоз со сдвигом влево и повышенные значения СОЭ могут служить одним из неспецифических маркеров развития осложнений. У больных с ХП с внешнесекреторной недостаточностью очень редко определяют лейкоцитоз. Более того, характерна умеренная лейкопения, свидетельствующая о трофологической недостаточности. В этом случае наблюдают длительно сохраняющееся повышение СОЭ, что наиболее часто обусловлено диспротеинемией. У больных с тяжелыми формами синдрома мальабсорбции могут наблюдать признаки железодефицитной, В6-, В12- и фолиеводефицитной, а чаще смешанной анемии.
В биохимическом анализе крови определяют сниженный уровень общего белка крови, альбумина, транстиретина, трансферрина, ферритина и других белков, характеризующих висцеральный пул белков и степень трофологической недостаточности. Регистрируют диспротеинемию, характеризующуюся снижением альбумин-глобулинового коэффициента, относительным увеличением α1- и α2-глобулинов. Нередко регистрируют повышенные показатели трансаминаз крови, γ-глутамил трансферазы, лактатдегидрогеназы. Повышение билирубина, преимущественно прямого, холестерина и щелочной фосфатазы характерно для развившегося синдрома холестаза, что может быть обусловлено блоком холедоха, развитием реактивного гепатита. У больных с алкогольным ХП повышение в крови активности печеночных ферментов может быть обусловлено самостоятельной патологией печени (токсическим гепатитом, циррозом печени). Нередко наблюдают гипокальциемию, степень которой может служить одним из критериев тяжести заболевания. Гиперкальциемия позволяет думать о гиперпаратиреозе как причинном факторе ХП.
Повышение уровня онкомаркеров (СА 19-9, карциноэмбриональный антиген - КЭА) выше значения, допустимого для воспаления, - косвенный признак трансформации ХП в РПЖ. При ХП допускают троекратное повышение СА 19-9, КЭА - двукратное. Следует помнить, что данные онкомаркеры неспецифичны для РПЖ и могут быть выявлены при раке желудка, холангиогенном и колоректальном раке.
Инструментальные исследования
Классическое (трансабдоминальное) УЗИ считают первой линией диагностики. При использовании современного оборудования с датчиком, обеспечивающим широкое поле обзора и высокую разрешающую способность, с компьютерной цифровой обработкой изображения в большинстве случаев УЗИ достаточно для качественной визуализации всех отделов ПЖ, ее паренхимы и протоковой системы. Патогномоничные признаки - диффузное изменение размера органа, неровность и нечеткость контуров, гиперэхогенность паренхимы (вне отечно-интерстициальных изменений), дилатация и утолщение стенок ГПП, кальцификация паренхимы и вирсунголитиаз. В большинстве случаев применение КТ или ЭРХПГ только удорожает обследование и несет риск для больного, не давая дополнительной информации. Необходимость в применении КТ и ЭРХПГ возникает в случае невозможности визуализации каких-либо отделов ПЖ при УЗИ, при объемных процессах в ПЖ, а также при так называемом панкреатите минимальных изменений.
Совпадение гистологической картины при ХП (калькулезный, кистозный, индуративный, фиброзный и др.) по результатам аутопсии с прижизненными данными УЗИ составляет 83,3% случаев. Кроме того, УЗИ позволяет одновременно осмотреть печень, желчный пузырь, выявить явления гастро- и дуоденостаза, информация о которых может дополнить представление об этиологии, внепанкреатических осложнениях, дает возможность установить выпот в брюшной полости.
ЭУС - эндоскопическое ультразвуковое исследование считают высокоинформативным методом ультразвуковой диагностики заболеваний поджелудочной железы, при котором сканирование проводят не через брюшную, а через стенку желудка и ДПК. Такое приближение датчика к ПЖ позволяет детально изучить структуру ткани органа, состояние протоковой системы, провести дифференциальную диагностику панкреатита с раком ПЖ, оценить размеры парапанкреатических лимфоузлов и выявить конкременты протоковой системы. Большую роль отводят ЭУС для диагностики холедохолитиаза у больных с билиарнозависимыми формами панкреатитов. Это основано на том, что ЭУС обладает существенно большей чувствительностью, чем трансабдоминальное УЗИ. ЭУС позволяет с большой точностью выявлять участки панкреонекроза и перипанкреатических жидкостных скоплений, что может играть большое прогностическое значение при тяжелых формах хронического панкреатита.
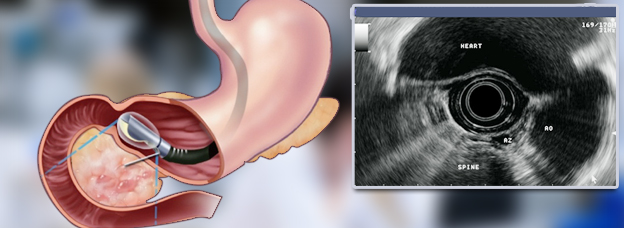
Информативность ЭУС больше или равна диагностическим возможностям КТ, МРТ и ЭРХПГ, однако при всех прочих условиях она однозначно менее инвазивна, чем ЭРХПГ, и вряд ли может существенно усугубить клинику панкреатита. Еще более информативно внутрипротоковое УЗИ ПЖ, диагностическое значение которого в отношении панкреатитов и опухолей ПЖ достигает 100%. Особенно целесообразно проводить внутрипротоковое УЗИ ПЖ для выяснения причины нарушения оттока секрета: при подозрении на аденому или рак БДС. Повышает диагностическую ценность ЭУС возможность проведения с большой точностью пункционной аспирационной биопсии ПЖ, особенно во всех случаях подозрения на опухоль.
Чувствительность, специфичность и диагностическая ценность метода превышают 90%.
КТ дает возможность поставить диагноз прежде всего на стадии осложнения панкреатита, когда чаще всего обнаруживают кальцификацию, псевдокисты, поражение соседних органов, атрофию паренхимы ПЖ и малигнизацию. Чувствительность и специфичность КТ в значительной степени колеблются в зависимости от стадии заболевания и составляют 80-90%.
В сложных диагностических случаях для уточнения патологии ПЖ используют спиральную КТ с внутривенным болюсным усилением неионным контрастным веществом (йопромидом, йогексолом). Спиральная КТ позволяет точнее отличить участки деструкции от сохраненной паренхимы, оценить взаимоотношения ПЖ с сосудами, лимфатическими узлами, парапанкреатической клетчаткой, стенками желудка и ДПК. Главное преимущество КТ - меньше факторов, затрудняющих обследование (тучность больных, наличие газа в толстой кишке и т.д.), как это наблюдают при УЗИ. Однако и ложноотрицательные результаты отмечают сравнительно часто.
Сочетание УЗИ и КТ достаточно эффективно при ХП, но если остаются какие-либо сомнения, следует прибегать к ЭРХПГ ввиду более высокой диагностической информативности последней.
ЭРХПГ - эндоскопическая ретроградная холангиопанкреатография. В большинстве современных научных публикаций и руководств в качестве «золотого стандарта» диагностики ХП приводят именно ЭРХПГ. Этот метод позволяет выявить стеноз ГПП и определить локализацию обструкции, обнаружить структурные изменения мелких протоков, внутрипротоковые кальцинаты и белковые пробки, а также патологию общего желчного протока. ЭРХПГ - один из важнейших методов исследования, позволяющих проводить дифференциальную диагностику с раком ПЖ. Чувствительность и специфичность метода варьируют в пределах 71-93 и 89-100% соответственно.
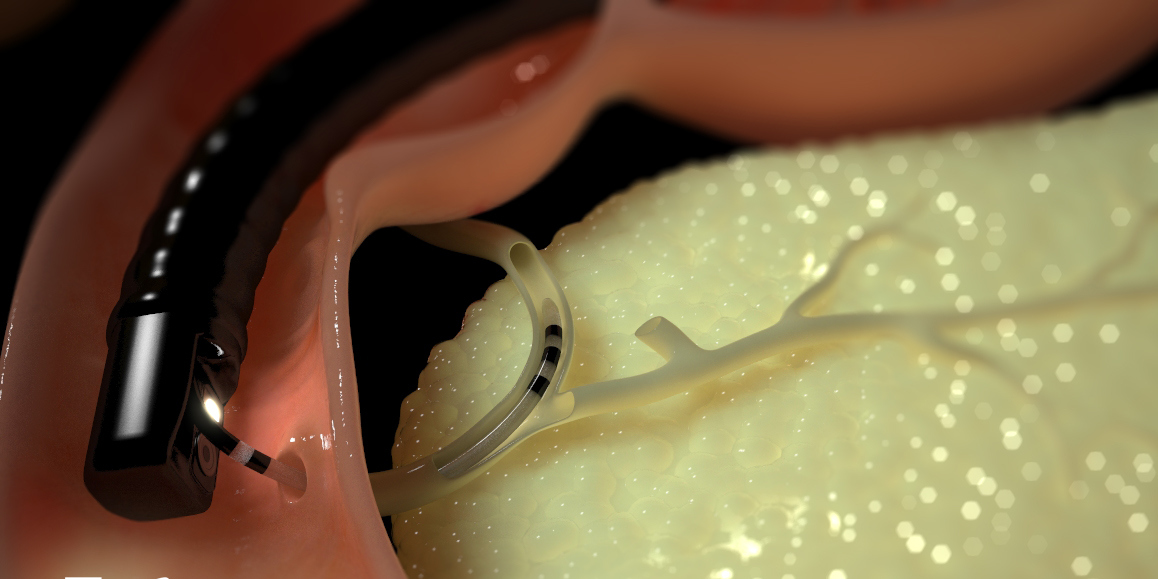

ЭРХПГ не исключает возможности развития серьезных осложнений, связанных с ретроградным введением под давлением контраста в панкреатический проток. К наиболее частым осложнениям относят ОП, холангит, сепсис, аллергические реакции на йодсодержащий контраст, перфорацию ДПК и общего желчного протока, кровотечение и др. Частота составляет от 0,8 до 36,0%, летальность - 0,15-1,0%. В ряде случаев после ЭРХПГ наблюдают повышение лабораторных маркеров холестаза и цитолиза гепатоцитов. Именно поэтому для достижения хороших результатов чрезвычайно важными являются исключение пациентов с высоким риском осложнений и их соответствующая предоперационная подготовка.
Большое диагностическое значение имеет ЭРХПГ при диагностике аутоиммунного ХП, позволяя у всех больных выявить сегментарные или диффузные иррегулярные сужения ГПП (типичный признак этой формы ХП).
МРТ и магнитно-резонансная холангиопанкреатография (МРХПГ). В последние годы в связи с диагностическими возможностями, более высокими чувствительностью и специфичностью МРТ рассматривают в качестве альтернативной КТ-методики при дифференциальной диагностике ХП с раком ПЖ, при диагностике кист и псевдокист, врожденных аномалий развития ПЖ, включая pancreas divisum. Чувствительность МРТ в диагностике ХП - 92,2%, специфичность - 97,1%.
МРХПГ способна во многих диагностических ситуациях заменить в качестве первичного метода диагностики прямые методы контрастирования (ЭРХПГ) с их высоким риском осложнений. МРХПГ ввиду своей неинвазивности может быть методом диагностического выбора, особенно при непереносимости пациентами йодсодержащих препаратов и при декомпенсированном состоянии больных.
Данные, получаемые при МРХПГ, существенно превышают информативность других неинвазивных методик, в том числе УЗИ, КТ и стандартной МРТ. При МРХПГ выполняют и стандартную МРТ брюшной полости, при которой можно определить состояние паренхимы ПЖ и соседних органов, что приобретает особое значение при подозрении на трансформацию ХП в рак. При типичной картине холедохолитиаза как причины тяжелой атаки ХП, включающей желтуху, холангит, расширение холедоха по данным УЗИ, показаний к МРХПГ практически нет. Это объясняется тем, что в данном случае целесообразнее выполнять ЭРХПГ, обладающую, помимо диагностической ценности, и лечебными возможностями (ЭПСТ, литоэкстракция и т.д.). С другой стороны, когда диагностические признаки холедохолитиаза сомнительны (диаметр общего желчного протока <10 мм, быстрая редукция маркеров холестаза, отсутствие признаков холангита и анамнестических указаний на ЖКБ), МРХПГ может быть предложена как процедура выбора для диагностического скрининга.
Дуоденоскопия позволяет диагностировать патологию БДС, выявить заболевания желудка и ДПК, являющиеся возможной причиной развития ХП, проводить селективный забор панкреатического сока для ферментного и морфологического исследования.
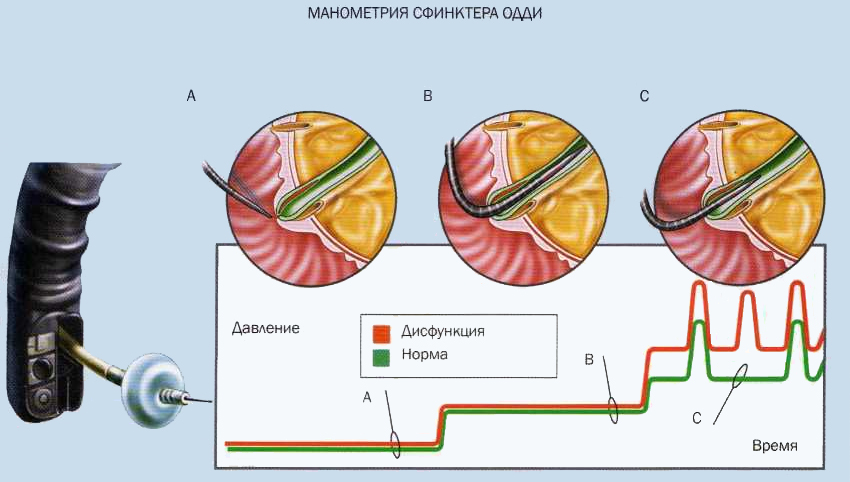
Метод манометрии сфинктера Одди весьма дорог и может быть выполнен только в специализированных медицинских центрах. Кроме того, высокая частота осложнений (преимущественно атака ХП или ОП) в 9-33% случаев также ограничивает широкое применение этого метода.
Рентгеновский метод. Обнаружение кальцификации ПЖ при обзорной рентгенографии органов брюшной полости считают наиболее достоверным рентгенологическим симптомом ХП, патогномоничным для этого заболевания. Кроме того, целесообразна рентгеноскопия органов грудной клетки, при которой иногда выявляют патогномоничные признаки осложнений тяжелой атаки ХП - левосторонний (реже двусторонний) экссудативный плеврит или дисковидный ателектаз нижней доли левого легкого, ограничение подвижности диафрагмы.
Диагностика и диагностические алгоритмы
Для интерпретации данных, полученных при инструментальном и лабораторном исследовании, группами экспертов в разных странах предложены различные критерии диагностики.
Диагностические критерии ХП Japan Pancreas Society (Японское общество по изучению поджелудочной железы)
• Определенный хронический панкреатит. При клиническом подозрении на ХП (хронических рецидивирующих абдоминальных болях и признаках экзокринной и эндокринной недостаточности) диагноз может быть установлен при обнаружении одного или более из следующих признаков.
❖ По данным УЗИ и КТ: интрапанкреатический калькулез.
❖ По данным ЭРХПГ: участки расширения мелких панкреатических протоков по всей паренхиме ПЖ или неравномерное расширение ГПП и проксимальных протоков с полным или неполным нарушением оттока (конкременты, белковые пробки).
❖ По данным секретинового теста: патологически низкая концентрация бикарбонатов в сочетании со снижением продукции ферментов или уменьшением объема секреции.
❖ Гистологическая картина: нерегулярный фиброз с разрушением и потерей экзокринной паренхимы в участках ткани.
❖ Дополнительные критерии: белковые пробки, панкреатические камни, расширение протоков, гипер- и метаплазия протокового эпителия и формирование кист.
• Вероятный хронический панкреатит.
❖ По данным УЗИ: усиленный рисунок ХП, грубое, несимметричное расширение панкреатических протоков или деформация ПЖ с нечетким контуром.
❖ По данным КТ: деформация ПЖ с нечетким контуром.
❖ По данным ЭРХПГ: единичные, неправильной формы участки дилатации ГПП, внутрипротоковые неконтрастирующиеся дефекты, похожие на неотвердевшие панкреатические камни или белковые пробки.
❖ По данным секретинового теста: патологическое снижение концентрации бикарбонатов или уменьшение продукции ферментов в сочетании с уменьшенным объемом секреции.
❖ По данным беззондовых тестов: одновременные изменения PABT-теста и теста на фекальный химотрипсин, наблюдаемые в течение нескольких месяцев.
❖ Гистологическая картина: интралобулярный фиброз в сочетании с одним из следующих признаков: потерей экзокринной паренхимы; изолированными островками Лангерганса; псевдокистами.
Принимая во внимание мнение большинства экспертов о диагностической значимости морфологических и функциональных методов исследования при диагностике ХП, Европейская многоцентровая группа по изучению ПЖ предлагает диагностический алгоритм, представленный на рис. 1. Предварительный диагноз ХП можно поставить на этапе опроса больного. В клинической практике диагноз основан на комбинации тестов. С учетом широкой распространенности и доступности УЗИ рекомендуют как первую ступень диагностики и планирования адекватных диагностических процедур. При эластазном тесте в дополнение к УЗИ можно выявить нарушения экзокринной панкреатической функции. У многих пациентов прямую оценку панкреатической функции невозможно осуществлять длительное время, поэтому прямые тесты имеют в основном научное значение. Дальнейшее исследование можно не проводить, если получены клинические ультразвуковые признаки ХП у больного с четкой клинической картиной заболевания. Если при диагностике возникают сомнения или если требуется получить детализированное представление, могут быть использованы ЭРХПГ, КТ, МРТ. Эти исследования занимают вторую ступень диагностического алгоритма. На ЭРХПГ можно получить детальную информацию о протоковой системе. КТ дает информацию о жидкостных образованиях (кистах, внепанкреатических аномалиях). МРТ чувствительна для выявления ранних фибротических изменений, предшествующих кальцификатам и грубым морфологическим изменениям. Все технические исследования необходимы для дифференциальной диагностики ХП с раком ПЖ. Эндо-УЗИ и ЭРХПГ, КТ и МРТ дополняют друг друга. Комбинация эндо-УЗИ, КТ и ЭРХПГ повышает чувствительность диагностики до 95-97%, специфичность - до 100%. При подозрении на рак ПЖ, туберкулез, гидатидный эхинококкоз, аутоиммунный панкреатит необходимо как можно более раннее проведение прицельной биопсии с последующим гистологическим или цитологическим исследованием. С учетом существенного количества осложнений при ЭРХПГ и высокой стоимости исследования предлагают проводить ЭУС, позволяющую, кстати, выполнить биопсию ПЖ.
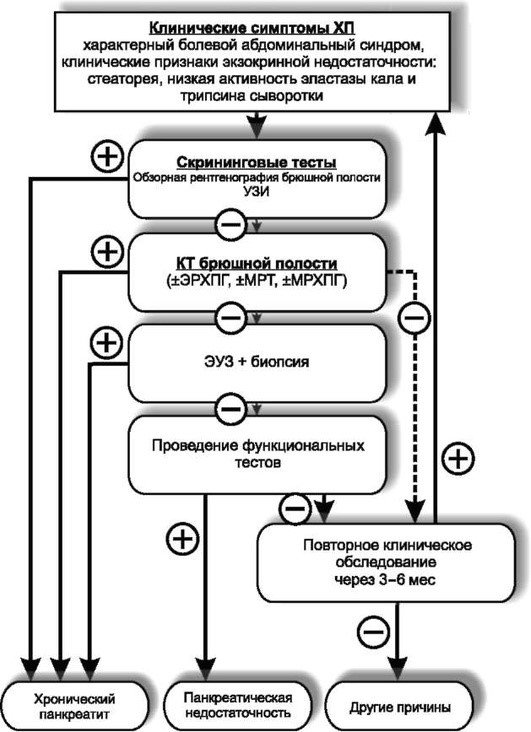
Рис. 1. Диагностический алгоритм при хроническом панкреатите.
В разделе, посвященном диагностике ХП, описана роль различных методов исследования при дифференциальной диагностике с другими заболеваниями. В целом при осуществлении диагностического поиска у пациентов с подозрением на хронический панкреатит необходима дифференциальная диагностика со следующими заболеваниями.
• Билиарный сладж. Часто проявляется атипичным болевым синдромом без четкой локализации. Диагноз основывают на данных УЗИ и микроскопии желчи.
• Дискинезия желчевыводящих путей. Часто проявляется атипичным болевым синдромом. Диагноз устанавливают при УЗИ, сцинтиграфии желчных путей с 99Тс-замещенными имидодиуксусными кислотами, фракционного дуоденального зондирования.
• Патология пищевода: эзофагит, эрозивно-язвенные поражения, эзофагоспазм. Характерны болевые ощущения в эпигастральной области и за грудиной, с обширными зонами иррадиации. Диагноз ставят на основании ФЭГДС, манометрии пищевода, суточного мониторирования рН.
• Язвенная болезнь желудка и ДПК. Характерны боль в эпигастральной области, иррадиирующая в ряде случаев в левое подреберье, спину, проявления диспепсии, ослабляемые при приеме антисекреторных препаратов и антацидов. Необходимо проведение ФЭГДС.
• Заболевания печени: гепатит и опухоли печени. Характерны боль в правой подреберной области, иррадиирующая в правый бок, спину и правую лопатку, тяжесть в левом подреберье за счет спленомегалии. Постановке диагноза помогают определение в крови ферментов печени, маркеров острых гепатитов и визуализирующие исследования.
• Заболевания толстой кишки: синдром раздраженной толстой кишки, опухоли, язвенные и воспалительные поражения (особенно при вовлечении в патологический процесс печеночного изгиба толстой кишки). Болевой синдром не имеет характерных отличительных особенностей и часто обусловлен функциональными нарушениями толстой кишки. Облегчение симптоматики часто возникает после дефекации или отхождения газов. Отличить функциональные изменения от органических позволяет колоноскопия.
• Заболевания легких и плевры. Характерны проявления плеврита, часто связанные с кашлем и одышкой. Необходимо рентгенологическое исследование грудной клетки.
• Патология скелетных мышц. Возможна боль в левом верхнем квадранте живота, связанная с движениями или принятием определенного положения. Пальпация ребер может быть болезненной, усиление боли также возможно при напряжении мышц передней брюшной стенки.
• Функциональные нарушения. Они часто сопровождаются длительной, постоянной болью. Среди таких нарушений необходимо отметить синдром функциональной абдоминальной боли, депрессию, тревожные и другие нейропсихические расстройства. Указанные состояния чаще встречаются у женщин и связаны с различными (в том числе хроническими) стрессовыми ситуациями.
• РПЖ, аномалии развития поджелудочной железы, опухоль фатерова сосочка - принципы дифференциальной диагностики описаны выше.
Больных с психовегетативными нарушениями следует направить на консультацию к психоневрологу (если отсутствует эффект от применения легких антидепрессантов).
Консультация хирурга на диагностическом этапе необходима при отсутствии четкого анамнеза, типичных клинических проявлений, неоднозначных данных лабораторно-инструментального исследования (УЗИ, сцинтиграфии, рентгенографических исследований) для исключения слабоманифестирующей хирургической патологии или при подозрении на развитие осложнений ХП, нарушения оттока желчи; дуоденальный стеноз; холангит, абсцессы ПЖ, парапанкреатит, ферментативный холецистит, паранефрит, кисты и псевдокисты ПЖ; портальную гипертензию (подпеченочная форма).
Консультация эндокринолога показана больным с хроническим панкреатитом с развитием инкреторной недостаточности.
Основной диагноз: хронический алкогольный фиброзно-склеротический панкреатит, персистирующая болевая форма.
Осложнения: синдром панкреатогенной мальабсорбции, панкреатогенный сахарный диабет, латентное течение; псевдокиста головки поджелудочной железы; трофологическая недостаточность 3-й степени по смешанному типу с преобладанием квашиоркора.
Основной диагноз: хронический идиопатический паренхиматозный панкреатит, редко рецидивирующая болевая форма с экзокринной панкреатической недостаточностью.
Осложнения: панкреатогенный сахарный диабет средней степени тяжести, инсулинопотребный, трофологическая недостаточность 2-й степени по типу маразм.
Цели лечения
• Купирование боли.
• Коррекция эндо- и экзокринной панкреатической недостаточности.
• Коррекция трофологического статуса.
• Улучшение качества жизни.
• Предупреждение осложнений.
Показания к госпитализации при хроническом панкреатите
• Рецидивирующий болевой абдоминальный синдром, не контролируемый в амбулаторных условиях.
• Нарастающая трофологическая недостаточность.
• Декомпенсация сахарного диабета.
• Появление признаков осложненного течения: механической желтухи, портальной гипертензии, длительно персистирующей гиперамилаземии и др.
Немедикаментозное лечение
Диетотерапия. Основные принципы диетотерапии больных с хронического панкреатита в период обострения:
• голод и нутритивная поддержка в период выраженных клинических и метаболических признаков аутолитического процесса в ПЖ;
• переход к полноценному питанию по возможности в кратчайшие сроки, особенно относительно квоты белка;
• постепенное включение блюд и продуктов в пищевой рацион при расширении диеты;
• постепенное увеличение объема вводимой пищи и калорийности рациона при расширении диеты;
• максимальное механическое и химическое щажение ПЖ и других органов проксимального отдела пищеварительного тракта.
Основной алгоритм диетотерапии при обострении хронического панкреатита.
В первые 1-2 дня от начала обострения ХП назначают голод. При отсутствии рвоты и признаков гастро- и дуоденостаза разрешают только прием жидкости в количестве 1,0-1,5 л/сут (по 200 мл 5-6 раз). Назначают щелочную минеральную воду комнатной температуры без газа, отвар шиповника (1-2 стакана), некрепкий чай. На фоне проводимой терапии по мере улучшения общего состояния (обычно на 2-3-й день от начала обострения) можно приступить к осуществлению перевода больного сначала на ограниченное, а затем и на полноценное пероральное питание. При этом остаются в силе основные принципы диетотерапии больных с ХП: диета должна быть механически и химически щадящей, малокалорийной и содержащей физиологическую норму белка (с включением 30% белка животного происхождения). Поскольку жидкая пища и углеводы в наименьшей степени стимулируют панкреатическую и желудочную секрецию, пероральное питание начинают со слизистых супов, жидких протертых молочных каш, овощных пюре и киселей из фруктового сока. При расширении диеты строго соблюдают принцип постепенности как в отношении увеличения объема и калорийности рациона, так и в отношении включения в него отдельных блюд и пищевых продуктов. Всю пищу варят, готовят на пару, жидкой или полужидкой консистенции. Режим питания дробный (5-6 раз в сутки). Подобную диету больным необходимо назначать еще 3-4 дня. Затем можно перевести больного на механически щадящий вариант диеты на 3-8-й неделе. А затем при стойкой ремиссии разрешить вариант диеты без оберегания от механического раздражения.
Питание больных с хроническим панкреатитом в период ремиссии
Основным средством стабилизации течения ХП в период ремиссии считают тщательное соблюдение диетического режима. Диета в стадии ремиссии должна содержать повышенное количество белка - 120-140 г/сут, 60% белка должно быть животного происхождения. Рекомендуют пониженное количество жиров (6080 г/сут), причем оно должно быть равномерно распределено на все приемы пищи в течение дня. Жиры в чистом виде из рациона исключают вовсе. В рацион следует включать около 350 г/сут углеводов, главным образом за счет простых, легкоусвояемых. Общая энергетическая ценность должна составлять 2500-2800 ккал/сут. Также ограничивают в рационе поваренную соль (до 6 г/сут).
Даже при значительном улучшении состояния здоровья и кажущемся благополучии не следует допускать резких нарушений ни со стороны качественного содержания диеты, ни со стороны режима питания. Диета больных в этом периоде включает в основном те же продукты, что и при обострении, только блюда могут быть менее щадящими: протертые супы заменяют обычными вегетарианскими, каши могут быть более густыми, рассыпчатыми, можно давать макаронные изделия, растительную клетчатку в сыром виде (овощи и фрукты), мягкие неострые сыры, докторскую колбасу, отварное мясо кусками, печеную рыбу. Пищу готовят в протертом виде, на пару или запекают в духовке. Режим питания дробный (5-6 раз в день), приемы пищи рекомендуют делить на небольшие по объему порции. Обязательное дополнение к этому принципу - есть медленно и тщательно пережевывать пищу. Температура горячих блюд должна быть не выше 57-62 °С, холодных - не ниже 15-17 °С.
Показанием для нутритивной поддержки являются длительное воздержание от перорального питания (при обострении ХП), трофологическая недостаточность 2-3-й степени. Рекомендуют ежедневные внутривенные инфузии аминокислотных растворов в объеме до 1,0 л/сут; концентрированные растворы глюкозы* с инсулином и электролитами - от 1,5 до 2,0 л/сут; жировые эмульсии - от 0,5 до 1,0 л/сут или универсальные смеси для парентерального питания, содержащие все необходимые компоненты (олеклиномель и др.). Поскольку энтеральное зондовое питание более физиологично, в последнее время отдают предпочтение либо комбинированному (энтеральному и парентеральному), либо исключительно энтеральному питанию. В случае выраженной внешнесекреторной недостаточности ПЖ и при наличии трофо-логической недостаточности при переходе на традиционную диету можно рекомендовать дополнительное к столу №5п введение в 2-3 приема в сутки различных смесей для энтерального питания, в том числе и негидролизованных.
Медикаментозное лечение хронического панкреатита
Главные задачи консервативной терапии ХП - уменьшение или купирование болевого абдоминального синдрома и предотвращение или компенсация функциональной панкреатической недостаточности. Основные принципы консервативного лечения ХП следующие:
• снятие боли;
• создание функционального покоя поджелудочной железе;
• уменьшение ее секреторной активности;
• коррекция экскреторной (пищеварительной) недостаточности;
• коррекция углеводного обмена;
• коррекция синдромов нарушенного пищеварения и всасывания;
• купирование боли.
В комплексной терапии болевого абдоминального синдрома у больных с ХП необходимо строжайшее соблюдение диеты, исключение алкоголя и курения. В первую очередь назначают препараты аналгезирующего действия и спазмолитики: 50% раствор анальгина* и 2% раствор папаверина по 2 мл или 5 мл баралгина внутримышечно в сочетании с антигистаминными препаратами.
При возможности перорального питания больного анальгетик первого выбора - парацетамол, который необходимо принимать до еды для предотвращения постпрандиального усиления боли. Максимальная суточная доза - 2000 мг, эффективная разовая доза - 500 мг. Следует помнить, что именно парацетамол наиболее гепатотоксичен из всей группы ненаркотических анальгетиков, что может ограничивать его применение у больных с сопутствующими поражениями печени, в первую очередь алкогольными.
Дозы анальгетиков подбирают индивидуально, причем следует использовать самую низкую эффективную дозу. При неэффективности ненаркотических анальгетиков возможны их применение в максимально допустимых суточных терапевтических дозах, комбинированное назначение (например, парацетамол и трамадол), изменение режима приема и пути введения или попытка замены на другой препарат этой группы. Другой путь повышения эффективности обезболивающей терапии - дополнительное включение в схему психотропных препаратов (нейролептиков, антидепрессантов, транквилизаторов), оказывающих как прямое аналгезирующее, так и потенцирующее действие в отношении ненаркотических анальгетиков. Можно использовать сульпирид в дозе 100-300 мг/сут (препарат назначают в первой половине дня), амитриптилин (10-75 мг/сут) дробно в течение суток, дневные транквилизаторы (медазепам). Выбор психотропного препарата, длительность применения, суточные дозы целесообразно согласовать с психоневрологом ввиду особенностей психовегетативного статуса каждого больного.
В случаях резистентности к ненаркотическим анальгетикам могут быть применены опиаты и их синтетические аналоги.
Хороший эффект, особенно при сопутствующей дискинезии желчевыводящих путей, ДПК, дает применение селективного миотропного спазмолитика мебеверина (дюспаталина*) в дозе 200 мг 2 раза в день (утром и вечером) внутрь в течение 2 нед и более.
Внутрикишечное введение трипсина или химотрипсина по механизму обратной связи ингибирует секрецию ферментов ПЖ, уменьшает ее секреторное напряжение, что способствует снижению болевого абдоминального синдрома. Эти факты позволили еще в начале 1980-х гг. обосновать применение полиферментных препаратов с высокой протеолитической активностью для уменьшения боли при ХП посредством дуоденопанкреатического механизма обратной связи.
В настоящее время эффективная терапия ХП стала возможной за счет назначения больным с хроническим панкреатитом с выраженным болевым синдромом микрокапсулированных ферментных средств, покрытых кишечнорастворимой оболочкой и содержащих достаточные дозы ферментов, способных не только корригировать нарушенное пищеварение, но и эффективно купировать боль.
К таким лекарственным средствам относят ферментный препарат последнего поколения панкреатин (креон 25000), содержащий не только достаточный объем фермента липазы, расщепляющий жиры и помогающий сниженному пищеварению у больных с ХП, но и содержащий протеазы (1000 ЕД) в количестве, достаточном для коррекции болевого синдрома. Следует помнить, что назначать препарат для купирования болевого синдрома следует таким образом, чтобы часть дозы лекарственного средства больной принимал до еды. Именно эта часть препарата и выключает нежелательный интенсивный выброс холецистокинин рилизинг-фактора, приводящий к появлению боли.
Октреотид - синтетический аналог природного гормона соматостатина, эффекты которого - ингибирование желудочной и панкреатической секреции, цитопротективное действие и благоприятное влияние на ретикулоэндотелиальную систему, что может быть полезно в лечении ХП. В клинических исследованиях показано, что соматостатин имеет антиноцицептивную активность у человека. Несмотря на оптимистичные результаты исследований применения пролонгированного синтетического аналога октреотида в суточной дозе 100-600 мг у больных с болевыми формами ХП, перспективность подобных исследований ограничена существенным увеличением побочных эффектов препарата при длительном его использовании. При длительном лечении октреотидом усугубляется мальдигестия за счет резкого снижения выделения ферментов ПЖ в ДПК, возможно развитие пареза кишечника и ухудшение кровоснабжения в ПЖ. Особенно осторожно применяют октреотид при ЖКБ из-за увеличения вероятности камнеобразования при создающейся на фоне лечения гипотонии желчного пузыря.
Уменьшение протокового и тканевого давления и, таким образом, болевых ощущений можно достичь как прямым подавлением панкреатической секреции, так и опосредованно, через ингибирование синтеза соляной кислоты, которое приводило бы к уменьшению образования секретина и в определенной мере холецистокинина. В силу особенностей механизма действия наиболее эффективными следует признать ИПП, особенно последнего поколения - рабепразол.
При отработке тактики лечения болевого абдоминального синдрома у больных с ХП необходимо учитывать нарушения моторики желчного пузыря, модификация которой обеспечит нормальный пассаж секрета ПЖ. Отток желчи и панкреатического секрета может быть затруднен вследствие воспаления БДС, что требует назначения антибактериальной терапии (полусинтетических пенициллинов, препаратов тетрациклинового ряда, цефалоспоринов, макролидов, выделяемых в достаточных концентрациях с желчью).
При гипомоторных нарушениях ДПК и желчевыводящих путей применяют прокинетики - сульпирид (50-100 мг 2 раза в день), домперидон (10 мг 3-4 раза в день).
Для лечения хронического болевого абдоминального синдрома у больных с ХП в последние годы все чаще применяют малоинвазивные и эндоскопические методики (см. ниже).
Только если все возможные консервативные методики, примененные для купирования боли, исчерпаны, включая малоинвазивные вмешательства, следует рассмотреть возможности хирургического лечения. Вариант оперативного пособия выбирают в зависимости от этиологии панкреатита, клинико-инструментальной картины заболевания и предполагаемого механизма боли, о чем более подробно сказано ниже.
Консервативная терапия отечной формы хронического панкреатита. Больных с отечным (интерстициальным) панкреатитом следует лечить в хирургическом отделении, однако в клинической практике бывает трудно выявить отечные изменения ПЖ, особенно при отсутствии панкреатической гиперферментемии, и больные нередко оказываются в терапевтических и гастроэнтерологических отделениях стационаров. Именно поэтому всем больным с ХП с малейшим подозрением на развитие отечно-интерстициальных изменений ПЖ показана базисная терапия.
Заместительная полиферментная терапия. Показания для заместительной ферментной терапии при ХП с внешнесекреторной недостаточностью:
• стеаторея при условии потери с калом более 15 г жира в сутки;
• прогрессирующая трофологическая недостаточность;
• стойкий диарейный синдром и диспептические жалобы.
Наиболее универсальными средствами, нормализующими пищеварение при синдромах мальдигестии и мальабсорбции, считают препараты панкреатина, не оказывающие влияния на функцию желудка, печени, моторику билиарной системы и кишечника. Эти ферменты обеспечивают достаточный спектр пищеварительной активности и способствуют купированию таких клинических признаков, как тошнота, урчание в животе, метеоризм, стеато-, креато- и амилорея.
Комбинированные препараты наряду с панкреатином содержат желчные кислоты, гемицеллюлазу, симетикон, растительные желчегонные (куркума) и др. Ферментные препараты, содержащие желчные кислоты, противопоказаны больным с отечными и болевыми формами ХП, поскольку они увеличивают секрецию ПЖ, стимулируют перистальтику кишечника и моторику желчного пузыря, увеличивают внутрикишечное осмотическое давление и, следовательно, болевой абдоминальный синдром.
Применение желчесодержащих препаратов показано и эффективно только при гипомоторной дискинезии желчного пузыря, симптомах диспепсии при переедании, снижении концентрации желчных кислот в ДПК.
Основная цель заместительной терапии панкреатическими ферментами заключается в обеспечении достаточной активности липазы в ДПК. Поскольку воздействие соляной кислоты на панкреатические ферменты приводит к разрушению до 90% их количества, путем преодоления кислотного желудочного барьера было осуществлено создание галенических форм полиферментных препаратов в кислотоустойчивой оболочке, поскольку использование препарата, имеющего такую оболочку, увеличивает всасывание жиров в среднем на 20% по сравнению с сопоставимой дозой обычного панкреатина.
Для обеспечения быстрого и гомогенного смешивания ферментов с пищевым химусом, предотвращения внутрижелудочной инактивации и адекватного пассажа из желудка в ДПК были созданы ферментные препараты панкреатина нового поколения в виде мини-микросфер (креон*), диаметр которых не превышает 2 мм. Препарат покрыт энтеросолюбильной оболочкой и заключен в желатиновые капсулы. При попадании в желудок желатиновые капсулы быстро растворяются, микросферы, или микротаблетки, смешиваются с пищей и постепенно поступают в ДПК. При рН дуоденального содержимого выше 5,5 оболочки растворяются и ферменты начинают действовать на большой поверхности. При этом практически воспроизводятся физиологические процессы пищеварения, при которых панкреатический сок выделяется порциями в ответ на периодическое поступление пищи из желудка.
Поскольку максимальное физиологическое постпрандиальное поступление панкреатической липазы составляет приблизительно 140000 ЕД/ч в течение 4 ч после еды, а мальабсорбция не развивается, если в ДПК попадает более 5% нормальной максимальной продукции фермента, то для коррекции стеатореи необходимо обеспечить поступление около 28000 ЕД липазы в течение 4 ч постпрандиального периода. Соответственно для коррекции стеатореи необходимо использовать препараты только с высоким содержанием липазы. Очевидно, что применение энтеросолюбильных таблетированных полиферментных препаратов панкреатина, особенно в традиционных дозах, для лечения экзокринной недостаточности ПЖ практически бесполезно. При умеренно выраженной экзокринной недостаточности (эластазный тест - 100-199 мкг/г) рекомендуемая суточная доза панкреатина составляет 100000 ЕД FIP (по 2 капсулы 5 раз в день), при выраженной экзокринной недостаточности (эластазный тест менее 100 мкг/г) минимальная рекомендуемая доза - 150000 ЕД FIP (по 1 капсуле 6 раз в день). Несмотря на правильный выбор ферментного препарата для заместительной терапии и его стартовой дозы, последнюю нередко приходится корректировать как ввиду ее возможной неэффективности, так и при ее эффективности в целях уменьшения суточной дозы для более экономичной терапии.
Побочные эффекты полиферментной терапии возникают нечасто и обычно не носят тяжелого характера.
Лечение внешнесекреторной недостаточности поджелудочной железы носит комплексный характер и включает специфическую нутритивную коррекцию, этиотропную и заместительную терапию экзокринной недостаточности, а также симптоматические средства.
Этиотропная терапия хронического панкреатита с внешнесекреторной недостаточностью ПЖ имеет значение только при некоторых этиологических формах ХП. Это обусловлено тем, что при развитии панкреатической недостаточности происходит потеря до 90% функционирующей экзокринной паренхимы ПЖ, и этиотропная терапия направлена преимущественно на предотвращение прогрессирования заболевания с максимальным сохранением оставшейся функциональной паренхимы, особенно эндокринного аппарата ПЖ. Классический пример этиотропного подхода к терапии - исключение приема алкоголя у больных с алкогольным ХП. Возможно оперативное лечение при обструктивном хроническом панкреатите. В отношении прочих причин развития ХП этиотропная терапия не разработана либо неэффективна на данной стадии заболевания.
Нутритивная поддержка складывается из рекомендаций общего характера: исключения алкоголя и курения вне зависимости от этиологии заболевания, включения большого количества белка в рацион (до 150 г/сут), снижения на 50% нормы содержания в пище жиров. Рекомендуют преимущественно среднецепочечные триглицериды, моно- и полиненасыщенные жирные кислоты, которые легче перевариваются панкреатической липазой и всасываются без образования мицелл. Пищевой рацион обогащают витаминами, в первую очередь жирорастворимыми. Рекомендуют принимать витаминно-минеральные комплексы, содержащие высокие дозы витаминов и микроэлементов, с дополнительным применением антиоксидантных комплексов.
Пациентам с развитием трофологической недостаточности в зависимости от тяжести состояния назначают парентеральное, энтеральное либо комбинированное питание.
Хирургическое лечение хронического панкреатита
Малоинвазивные методики и эндоскопическое лечение хронического панкреатита.
В настоящее время эндоскопическое лечение играет одну из ведущих ролей в лечении панкреатитов, обладая широким кругом возможностей для лечебного воздействия, - ЭпСт, дилатация стриктур и эндопротезирование протоков, литотрипсия и литоэкстракция конкрементов терминального отдела общего желчного протока и ГПП. Перечисленные методы позволяют получить хорошие клинические результаты, сравнимые с таковыми при инвазивных оперативных вмешательствах.
При установлении билиарной этиологии панкреатита (камни внепеченочных желчных протоков, стеноз БДС и терминального отдела холедоха) больному показана ЭПСТ - эндоскопическая папиллосфинктеротомия. Канюляционный способ успешен у 75-95% пациентов. При неудачных канюляциях ампулы ЭПСТ может быть выполнена неканюляционным способом (предрассечением).
ЭПСТ - эндоскопическая папиллосфинктеротомия с установкой билиарного стента (± назобилиарное дренирование) для профилактики и лечения холангита у больных с билиарнозависимым ХП на фоне холедохолитиаза весьма эффективна и может быть альтернативой объемной полостной операции. Однако на фоне гнойного холангита часто возникает обтурация эндопротеза, что несколько увеличивает процент неудачных вмешательств. С другой стороны, если на фоне неадекватного билиарного дренирования и механической желтухи общее состояние больного позволяет выполнить повторное вмешательство, то замена засорившихся стентов будет методикой выбора ввиду меньшей инвазивности по сравнению с оперативным лечением, в частности с наложением билиодигестивного анастомоза.
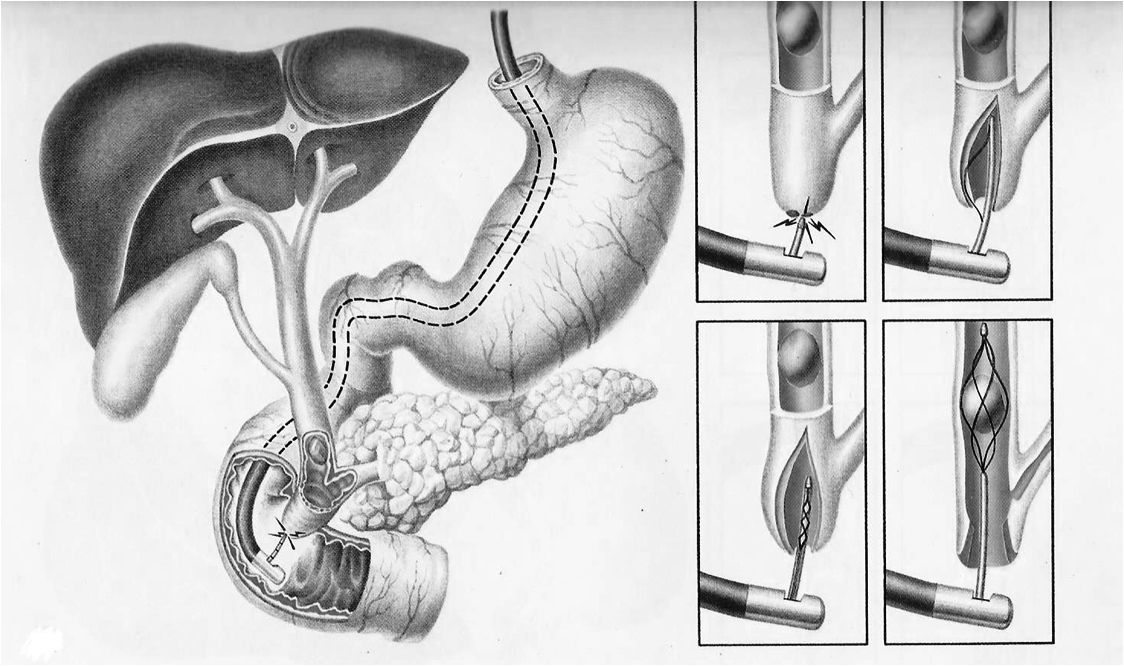
Также показанием к эндоскопическому лечению считают не только стеноз БДС, но и резистентную к консервативной терапии его дисфункцию.
Считают, что ЭПСТ уменьшает выраженность болевого абдоминального синдрома и повышает качество жизни больных с ХП на фоне дисфункции сфинктера Одди. Возможна эндоскопическая инъекция ботулинического токсина (100 ЕД) в зону БДС у больных с рецидивирующим панкреатитом, обусловленным дисфункцией сфинктера Одди.
Важное преимущество эндоскопической папиллосфинктеротомии над хирургическими методиками при обструктивных формах панкреатитов - это возможность более раннего применения ЭПСТ, когда еще нет прямых показаний к оперативному лечению, но исчерпаны возможности консервативных мероприятий. Достаточно важным следует считать и то, что примененное на первом этапе эндоскопическое лечение в случае его неэффективности оставляет возможность хирургического вмешательства.
При невозможности эндоскопической коррекции непроходимости терминального отдела общего желчного протока, желчной гипертензии, увеличенном и напряженном желчном пузыре показана чреспеченочная микрохолецистостома под контролем УЗИ или лапароскопии. Наложение холецистостомы под УЗ-контролем менее травматично, так как не требует наложения пневмоперитонеума. В последние годы появились свидетельства эффективности эндоскопической резекции БДС (ампулэктомии) в качестве альтернативы объемным хирургическим вмешательствам при мягкотканных образованиях БДС, которые считают одной из возможных причин ХП.
Эндоскопическое лечение показано при развитии стриктуры и конкрементах ГПП. При стриктурах, вызванных воспалительными и рубцовыми изменениями ткани ПЖ, проводят стентирование сроком от 2 до 6 мес, в случае невозможности установления стента сразу проводят баллонную дилатацию стриктуры с последующим установлением саморасширяющегося протеза. В целом технический успех в ряде проведенных исследований составил от 82 до 100%, а клиническое улучшение в виде уменьшения или купирования болевого абдоминального синдрома было достигнуто в 55-100% случаев в сроки от 8 до 39 мес. Одним из осложнений стентирования ГПП может быть окклюзия стентов, возникающая у 50% больных в сроки до 8 нед после их установления. При конкрементах ГПП проводят ЭПСТ с возможной попыткой литоэкстракции. Имеется значительный диапазон данных об успешном удалении панкреатических конкрементов после ЭПСТ - от 27 до 100%. Нередко для предварительной фрагментации камней применяют экстракорпоральную ударно-волновую литотрипсию конкрементов ГПП с клиническим улучшением у 50-80% пациентов с болевыми формами хронического панкреатита.
Пункцию и дренирование с лечебной целью псевдокист, непосредственно прилегающих к желудку или ДПК, проводят с помощью эндоскопа, визуально в зоне выпячивания стенки желудка или ДПК. Использование эндоскопического ультразвукового исследования при цистогастростомии позволяет определить оптимальную зону для пункции, повышая эффективность вмешательства и уменьшая риск возможных осложнений, в частности кровотечения и перфорации. Разработан комплексный подход к лечению панкреатогенных псевдокист, включающий трансабдоминальное УЗИ с чрескожной пункцией псевдокисты, аспирацию 10-20 мл жидкости для биохимических и цитологических исследований, введения в кисту 10-15 мл контрастного вещества под рентгеновским контролем. В дальнейшем может быть использована эндоскопическая пункция кист диатермической иглой (только в случае их расположения в пределах 1-4 см от стенки желудка или ДПК) для назокистозного или внутреннего дренирования.
Малоинвазивные методики для купирования боли в настоящее время у больных с болевыми формами ХП применяют нечасто ввиду кратковременности их аналгезирующего действия и необходимости частых повторных манипуляций. Однако простота выполнения блокады, доступность для любого медицинского учреждения, особенно при отсутствии современных методик и анальгетиков, до сих пор оставляют панкреатодуоденальные блокады в арсенале практических врачей.
Появление методики нейролизиса чревного сплетения с использованием ЭУС повысило эффективность вмешательства ввиду большой точности определения зоны введения спирта. В целом блокада чревного сплетения под контролем ЭУС - относительно легковыполнимая и безопасная процедура, сопровождаемая эффективным, но кратковременным облегчением боли. Торакоскопическая спланхнотомия - одна из достаточно новых малоинвазивных методик, заключающаяся в разделении большого и малого внутренностных симпатических афферентных нервов, участвующих в передаче болевых афферентных импульсов. Методика оказалась эффективной при купировании выраженного болевого абдоминального синдрома у больных с ХП. Лучшие результаты замечены при двусторонней торакоскопической спланхнотомии по сравнению с односторонней.
Оперативное лечение.
Показания к хирургическому лечению хронического панкреатита:
• боль, не купируемая другими способами;
• кисты и абсцессы ПЖ, стриктуры или обструкция желчных протоков, не разрешаемые эндоскопически, стеноз ДПК, окклюзия селезеночной вены и кровотечение из варикозно расширенных вен, свищи ПЖ с развитием асцита или плеврального выпота;
• подозрение на развитие рака ПЖ, не подтвержденное гистологически (цитологически).
Оперативное лечение в целях уменьшения или купирования болевого абдоминального синдрома требует тщательнейшего обследования в предоперационном периоде для оценки состояния протоковой системы ПЖ, степени ее функциональных нарушений (эндо- и экзокринная недостаточность ПЖ) и решения вопроса о целесообразности данного лечения. Только комбинированное применение ЭРХПГ, КТ и МРТ обеспечивает необходимой информацией для предоперационной оценки ПЖ, позволяя установить расположение протоков и степень их обструкции, наличие сообщающихся или не сообщающихся с ними псевдокист, перипанкреатического фиброза.
Панкреатогастростомия у больных с кистами ПЖ, панкреатической гипертензией, дилатацией вирсунгова протока и стойким высокоинтенсивным болевым абдоминальным синдромом приводит к купированию или уменьшению боли у 83% пациентов. Важными моментами считают отсутствие в послеоперационном периоде симптомов мальдигестии, достоверных изменений желудочного рН. Наилучший эффект в отношении болевого абдоминального синдрома достигают, если псевдокиста сообщается с крупным протоком ПЖ. Дистальная резекция ПЖ с панкреатоеюностомией эффективна в 70-80% случаев в отношении купирования или уменьшения болевого абдоминального синдрома у больных с ХП. Данную модификацию панкреатоеюностомии целесообразно применять у пациентов с дилатацией протоковой системы ПЖ и наличием кист и псевдокист, особенно локализованных в хвосте ПЖ. Считают, что данная модификация оперативного пособия наиболее безопасна и эффективна, поскольку частота ее осложнений не превышает 5%, интра- и послеоперационная летальность составляет менее 2% при эффективности в купировании или уменьшении боли в 80-90% случаев.
Дистальная резекция ПЖ может быть рекомендована при болевых формах ХП без признаков протоковой гипертензии, эффект наблюдается в 50% случаев. Субтотальная панкреатэктомия или панкреатодуоденальная резекция - чрезвычайно травматичные операции, объем которых, помимо резекции ПЖ, включает резекцию желудка, дуоденэктомию, холецистэктомию, а в ряде случаев и спленэктомию. Главный недостаток методики – существенное усугубление инкреторной и внешнесекреторной недостаточности ПЖ за счет удаления существенной части ее паренхимы. В последнее время предложена модификация без резекции желудка с сохранением его пилорического отдела и соответственно с меньшим количеством потенциальных осложнений и перспективно лучшим прогнозом в отношении состояния, близкого к физиологическим процессам пищеварения в верхнем отделе пищеварительного тракта, а также методика, позволяющая сохранить все экстрапанкреатические органы, подлежащие удалению, включая ДПК. Частота послеоперационных осложнений обеих модифицированных методик - 15 и 20% соответственно при отсутствии случаев послеоперационной летальности.
Этиотропным подходом к лечению билиарнозависимого ХП на фоне ЖКБ считают только холецистэктомию (лапароскопическую или открытым доступом). Несмотря на то что в подавляющем большинстве случаев холедохолитиаза эффективно используют ЭПСТ или эндобилиарную дилатацию БДС с низведением конкрементов в ДПК, встречаются случаи, когда необходимо оперативное лечение эндоскопически не удалимых конкрементов терминального отдела холедоха и БДС, вызывающих повторные атаки панкреатита.
Обострение хронического панкреатита обусловливает временное освобождение больных от работы на различные сроки, которые зависят от выраженности клинической симптоматики, тяжести заболевания, изменений других органов и систем, своевременного проведения лечебных и организационных мероприятий, возрастных особенностей, а также видов и условий труда больного.
При легком течении, когда болевой и диспептический синдромы выражены умеренно, определяют небольшой лейкоцитоз, кратковременную гиперферментемию и гиперферментурию, при своевременной госпитализации и комплексной консервативной терапии трудоспособность восстанавливается довольно быстро. Временная ее утрата составляет не менее 10-14 дней.
В случае благоприятного исхода при осложненном течении (образовании свищей, кист и пр.) процесс реконвалесценции продолжается длительное время, в связи с чем временная нетрудоспособность составляет 1,5-2 мес и более.
Критерии выписки больных, перенесших обострение хронического панкреатита, на работу: нормализация температуры тела, активности ферментов и количества лейкоцитов в периферической крови, резкое уменьшение или исчезновение болевого синдрома, интоксикации и астенизации, а также отсутствие производственных факторов, отрицательно влияющих на состояние здоровья.
Таким образом, решение о состоянии трудоспособности больных и эффективности трудового устройства зависит от правильно поставленного диагноза. Для правильной оценки трудоспособности больных и определения показаний к рациональному трудоустройству необходимо учитывать поражение других органов пищеварения, на фоне которых протекает ХП, частоту, тяжесть, длительность обострения, выраженность болевого синдрома в период обострения и ремиссии, функциональное состояние ПЖ, степень нарушения питания, характер работы и условия труда. Немаловажное значение имеют также личностные особенности больного, его эмоционально-волевая установка на продолжение трудовой деятельности, сопутствующие заболевания.
При легком течении ХП у большинства больных сохраняется профессиональная трудоспособность. Тем не менее этой категории больных противопоказаны трудовые процессы, которые требуют тяжелого физического напряжения и связаны с сотрясением, длительным вынужденным положением тела.
В отдельных случаях, когда рациональное трудоустройство больных с ХП сопровождается значительным снижением профессиональной трудоспособности, устанавливают III группу инвалидности.
При хроническом панкреатите средней тяжести обострения возникают до 3-5 раз в год. Продолжительность временной нетрудоспособности в таком случае составляет не менее 30-40 дней. Это обусловлено медленным обратным развитием патологического процесса и замедленной компенсацией функциональной недостаточности ПЖ, что связано не только с тяжестью морфологических изменений ее ткани, но и с функциональными расстройствами других органов пищеварения (например, реактивный гепатит).
В период ремиссии у данной категории, несмотря на длительное стационарное лечение, чаще сохраняются стойкий болевой синдром, внешнесекреторная, а в ряде случаев и инкреторная недостаточность ПЖ. Нередко существенную роль в развитии синдрома трофологической недостаточности играют пограничные расстройства психики больных, длительно страдающих ХП. Эти нарушения у ряда пациентов считают основанием для перевода на более легкие работы, что значительно изменяет условия труда. Если это связано со снижением квалификации или сокращением объема работы, то им устанавливают III группу инвалидности.
При тяжелой форме хронического панкреатита больным устанавливают II, а иногда I группу инвалидности (при необходимости постоянного постороннего ухода).
Для данной категории пациентов характерны прогрессирующее течение, частые (6-7 раз в году и более), длительные и резко выраженные обострения, нарушения внешнесекреторной функции ПЖ и тяжелая инкреторная недостаточность, развитие механической желтухи, упорная диарея с выраженной трофологической недостаточностью; сроки временной нетрудоспособности могут составлять 2,5-3 мес и более. В период относительной ремиссии внешнесекреторная и инкреторная недостаточность ПЖ, болевой синдром и другие функциональные нарушения остаются резко выраженными, поэтому любая профессиональная деятельность становится недоступной (или противопоказанной) для больных.
Больные, перенесшие резекцию ПЖ, как правило, являются инвалидами II или I группы в связи с тяжелыми нарушениями пищеварения и углеводного обмена.
Поддерживающее лечение хронического панкреатита включает комплексную реабилитацию больных после перенесенного обострения ХП, хирургического лечения по поводу ОП и ХП и их осложнений, включающую амбулаторное и санаторно-курортное лечение, фитотерапию, все методы противорецидивного лечения, длящиеся в ряде случаев всю оставшуюся жизнь.
Больным с ХП в период ремиссии при отсутствии панкреатической гиперферментемии можно назначать различные методы санаторно-курортного и физиотерапевтического лечения.
Необходимо строго индивидуальное проведение лечебных мероприятий на курорте с соблюдением периода адаптации, назначения приема минеральных вод, начиная с небольших доз, исключение тепловых процедур у пациентов с глубокими структурными изменениями ПЖ и выраженными функциональными нарушениями. Основными лечебными средствами на курорте, как правило, должны быть естественные факторы. Медикаментозные средства в лечении больных с ХП на санаторно-курортном этапе играют вспомогательную роль, за исключением случаев, когда назначение - это обязательное продолжение лечения, начатого в стационаре или поликлинике.
Ведущий лечебный фактор на курорте - прием минеральной воды. Положительное влияние на ПЖ оказывает питьевое лечение маломинерализованными и средней минерализации водами, содержащими гидрокарбонаты, сульфатный ион, двухвалентную серу, кальций, цинк: «Славяновская», «Смирновская», «Ессентуки №4». Питьевое лечение минеральными водами действует как тренирующая и адаптационная терапия на ПЖ. Минеральные воды способствуют уменьшению застойных явлений в желчных протоках и ПЖ, обеспечивают противовоспалительное действие за счет постоянного оттока секретов, удаления слизи. Имеют значение ощелачивающее действие этих минеральных вод на ДПК, нормализация моторных нарушений, усиление эвакуации желудочного содержимого.
В стадию ремиссии хронического панкреатита широко используют минеральные воды наружно: углекисло-сероводородные, соляно-щелочные, углекисло-радоновые, сульфидные ванны, а также хвойные, йодобромные, жемчужные.
Грязелечение показано больным с ХП с внешнесекреторной недостаточностью ПЖ, а также с сопутствующими заболеваниями органов пищеварения. Грязелечение способствует улучшению кровоснабжения, оказывает противовоспалительное и аналгезирующее действие. Переносимость грязевых процедур значительно улучшается при чередовании с минеральными ваннами. Более легкая переносимость грязелечения дает возможность с успехом применять его у пациентов с болевым и выраженным астеническим синдромами, сопутствующими заболеваниями, наличие которых считают противопоказанием для аппликационного грязелечения. У больных с ХП в более поздние сроки после обострения заболевания (через 5-6 мес) доказана целесообразность дополнительного включения в комплексную терапию торфяных аппликаций.
Важное звено в системе этапного лечения - диспансеризация больных с хроническим панкреатитом, способствующая значительному повышению эффективности лечения. Целесообразность диспансеризации больных с ХП обусловлена частыми рецидивами заболевания, нередко с прогрессирующим течением и инвалидизацией. Известно, что купирование атаки панкреатита обычно не означает полного выздоровления. Как правило, имеют место выраженные в той или иной мере структурные изменения ПЖ, а значит и нарушения ее функции. У больных с ХП в стадии ремиссии обычно определяют различной степени дисбиоз кишечника, нарушения билиосинтетической и билиоэкскреторной функций печени, гастродуоденальной моторики и т.д.
Диспансерное наблюдение за больными с хроническим панкреатитом осуществляют в поликлинике терапевт и гастроэнтеролог с четким соблюдением преемственности между ними, а при необходимости и с хирургом. Больные после операции на ПЖ наблюдаются так же, как и больные с хроническим панкреатитом.
Методика наблюдения по программе реабилитации состоит в вызове больных на осмотр 2-4 раза в год в зависимости от тяжести заболевания, в оценке общего состояния больного, жалоб и физикальных данных, в проведении контрольных обследований и курсов противорецидивного лечения, дието-, фитотерапии. В поликлинике следует исследовать динамику активности ферментов ПЖ в сыворотке крови, концентрацию сахара и инсулина, определять степень стеатореи и креатореи по данным копрограммы, проводить УЗИ ПЖ и желчевыводящей системы.
Больных с легким течением хронического пакреатита наблюдают участковые терапевты. Контрольное обследование проводят 2 раза в год. Противорецидивное лечение включает диетическое питание (в рамках стола №5п), полиферментные препараты (панкреатин) курсами по 4-6 нед, по показаниям спазмолитики (мебеверин) или про-кинетики 2-3 нед, желчегонные препараты 2-3 нед.
Больным с ХП средней тяжести и с тяжелым течением показано наблюдение у гастроэнтеролога. Контрольное обследование проводят 3-4 раза в год. Противорецидивное лечение назначают каждые 2-3 мес, при необходимости на 6 мес и более. При наличии у больного белково-энергетической недостаточности назначают анаболические стероиды с поливитаминно-минеральными комплексами. При упорной полифекалии с признаками стеатореи показаны увеличение дозы полиферментных препаратов (до 150000 ЕД FIP/сут и более из расчета активности панкреатической липазы) и дополнительное применение смесей для энтерального питания в качестве добавки к пище (пептамена, нутризона и др.). При неэффективности увеличения дозы ферментов целесообразно добавлять к схеме лечения ИПП (рабе-празол в дозе 10-20 мг/сут).
Для улучшения кровотока в поджелудочной железе показан курсовой прием пентоксифиллина. В случае развившейся инкреторной недостаточности больному показаны наблюдения эндокринолога с регулярным контролем уровня гликемии и назначением соответствующей диеты и гипогликемических средств (по показаниям). При расстройствах сна назначают транквилизаторы (диазепам, фенозепам), гипнотики (золпидем, зопиклон).
При компенсации хронического процесса, благоприятной динамике и отсутствии обострений в течение 5 лет больные с ХП могут быть сняты с диспансерного наблюдения. Это, как правило, относится к больным с так называемыми вторичными ХП, если устранена причина (холелитиаз, стеноз БДС и др.). Больные с ХП с экскреторной и инкреторной недостаточностью, перенесшие оперативное вмешательство на ПЖ, подлежат пожизненной (бессрочной) диспансеризации.
На всех этапах медицинской реабилитации к работе с больными с ХП следует привлекать психотерапевта и медицинского психолога.
При хроническом панкреатите, в отличие от острого панкреатита, отсутствуют какие-либо общепринятые прогностические критерии. Прогноз для жизни больного при хроническом панкреатите зависит от возможного развития осложнений, требующих хирургического вмешательства с высокой интра- и послеоперационной летальностью. Считают, что десятилетняя выживаемость больных с алкогольным ХП составляет 80% при условии прекращения приема алкоголя и снижается более чем в 2 раза, если пациент продолжает употреблять алкоголь. Прогноз в отношении качества жизни зависит от развития хронической боли и тяжести внешнесекреторной и инкреторной недостаточности поджелудочной железы в исходе заболевания.
Источник: Гастроэнтерология. Национальное руководство / под ред. В. Т. Ивашкина, Т. Л. Лапиной - М. : ГЭОТАР-Медиа, 2018.
06.01.2020 | 17:15:31