Кахексия и анорексия у пациентов пожилого и старческого возраста. Определение, диагностика, лечение.
Раздел: Статьи
/
Общая врачебная практика.
/
Паллиативная помощь.
/
Кахексия и анорексия у пациентов пожилого и старческого возраста. Определение, диагностика, лечение.
Содержание
Введение
Диагностика кахексии
Тактика ведения пациентов с синдромом анорексии-кахексии
- Рекомендации по организации питания
- Медикаментозное лечение
- Особенности паллиативной помощи у пациентов с дисфагией и аспирацией
Кахексия - прогрессирующая потеря массы тела более чем на 5-10% за 6-12 мес, в основе которой лежат тяжелые хронические заболевания, сопровождающиеся синдромом хронического воспаления (рис. 1.1). В современной литературе вместе с термином «кахексия» используют термин «синдром анорексии-кахексии».

Рис. 1.1. Состояния, связанные с нарушением питания.
ССА - синдром старческой астении; ХНИЗ - хронические неинфекционные заболевания
Синдром анорексии-кахексии - комплексный многофакторный синдром, характеризующийся снижением аппетита, выраженной потерей массы скелетной мускулатуры со снижением объема жировой ткани или без таковой. В основе механизма развития кахексии лежат инсулинорезистентность, повышение в организме уровня провоспалительных цитокинов (α-фактора некроза опухоли, интерлейкина-1, интерлейкина-6), увеличение в крови уровня катаболических гормонов (глюкокортикостероидов, катехоламинов), снижение уровня анаболических гормонов СТГ), инсулина, половых стероидов), приводящие к снижению аппетита, катаболизму мышечной ткани и потере массы тела (табл. 1.3).

Таблица 1.3. Сравнительная характеристика изменений, происходящих в организме при кахексии и недостаточности питания без сопутствующего синдрома хронического воспаления
Длительный прием некоторых препаратов ведет к нарушению вкуса и обоняния, что приводит к снижению аппетита и увеличению риска развития синдрома анорексии-кахексии. В их числе аллопуринол, ингибиторы ангиотензинпревращающего фермента, блокаторы кальциевых каналов, антихолинергические препараты. Метформин, нейролептики, опиаты, дигоксин, некоторые антидепрессанты могут приводить к развитию анорексии. Прием петлевых диуретиков, антихолинергических средств, клонидина может сопровождаться появлением выраженной сухости слизистой оболочки ротовой полости. Нестероидные противовоспалительные препараты и бисфосфонаты могут быть причиной дисфагии. Все эти нарушения в свою очередь могут приводить к нарушениям питания и кахексии.
У 6-28% пациентов пожилого и старческого возраста установить причину кахексии не удается.
От кахексии следует отличать саркопению - состояние, характеризующееся прогрессивным снижением мышечной массы и силы, связанным со старением и не имеющим в своей основе тяжелых сопутствующих заболеваний.
При проведении диагностики у пожилых пациентов следует оценить физический, когнитивный и психологический статус с помощью соответствующих инструментов (индекс Карновского, шкала Восточной объединенной группы онкологов, опросники для выявления деменции, шкалы для оценки эмоционального статуса (табл. 1.4.), например госпитальная шкала тревоги и депрессии).

Таблица 1.4. Шкала оценки тяжести состояния пациента по версии Всемирной организации здравоохранения/Восточной объединенной группы онкологов (The Eastern Cooperative Oncology Group/World Health Organization Performance Status)
Необходимость такого обследования обусловлена тем, что нарушения физического состояния пациента, когнитивные расстройства (например, деменция), психоэмоциональные нарушения (тревога, депрессия) могут быть причиной анорексии и кахексии, приводя либо к неспособности пациента самостоятельно готовить и принимать пищу, либо к отказу от пищи.
Данная шкала используется для описания уровня функционирования пациента с точки зрения его способности заботиться о себе, повседневной активности и физических способностей (ходьба, работа и т.д.). На основе полученных данных рассчитывается индекс Карновского.
Расчет индекса Карновского
• 100% - жалобы у пациента отсутствуют, признаки патологии не были обнаружены.
• 90% - суточная активность сохраняется в нормальном состоянии, симптомы болезни имеют слабую степень проявления.
• 80% - поддержание активности проходит с затруднениями, симптоматика выражена умеренно.
• 70% - пациент может себя обслуживать, однако при выполнении активной работы возникают определенные сложности.
• 60% - способность самостоятельного обслуживания сохраняется, однако при определенных ситуациях требуется посторонняя помощь.
• 50% - больной может обслуживать себя не полностью, в большинстве случаев необходима помощь со стороны медицинского персонала.
• 40% - нужен специальный уход.
• 30% - у пациента отсутствует возможность к самостоятельному обслуживанию себя, назначается госпитализация, несмотря на то что нет угрозы для жизни.
• 20% - болезнь протекает в тяжелой форме, больного госпитализируют, требуется проведение активного поддерживающего лечения.
• 10% - заболевание переходит в стадию термального периода, отмечается быстро прогрессирующее состояние.
• 0% - констатируется смертельный исход.
При объективном осмотре у пожилых пациентов важно оценить состояние зубов, слизистой оболочки полости рта, поскольку отказ от приема пищи может быть обусловлен невозможностью ее пережевывания из-за плохого состояния зубов или зубных протезов либо проявлений заболевания слизистой оболочки полости рта. Однако эти изменения могут быть и вторичными, возникшими вследствие мальнутриции и кахексии.
Для оценки динамики снижения массы тела необходимо выполнить антропометрию. Важно контролировать адекватность режима гидратации. Важно отметить, что простые признаки и тесты, обычно используемые для оценки степени дегидратации, такие как тургор кожи, сухость во рту, изменение веса, цвет мочи или ее удельный вес, биоимпендансный анализ, не должны использоваться у пожилых людей из-за своей неинформативности. Для диагностики дегидратации у пожилых необходимо измерять осмолярность плазмы крови. Диагноз дегидратации ставится при осмолярности плазмы >300 Мосм/кг. Если прямое измерение осмолярности плазмы невозможно, ее можно рассчитать с использованием следующей формулы:
осмолярность = 1,86 × (Na+ + K+) + (1,15 × глюкоза) + мочевина + 14.
Диагноз дегидратации ставится при осмолярности >295 ммоль/л.
Лабораторные исследования включают клинический анализ крови, определение С-реактивного белка, оценку уровня глюкозы, общего белка, альбумина, креатинина, мочевины, билирубина, трансаминаз, электролитов.
Рекомендации по организации питания
При оказании помощи пациентам с анорексией-кахексией важно обсудить проблемы питания с пациентом и его родственниками, осуществляющими уход. Их необходимо проинформировать о возможных причинах развития анорексии-кахексии, о влиянии этих нарушений на общее состояние и прогноз, а также о возможностях лечения данного состояния.
Частью мультимодального мультидисциплинарного подхода, направленного на обеспечение достаточного уровня потребления пищи, поддержание или увеличение массы тела, улучшение функционального статуса, клинического состояния и качества жизни является нутритивная поддержка. Ориентировочный уровень потребляемой калорийности составляет 30 ккал на кг массы тела в сутки; это значение должно быть скорректировано в индивидуальном порядке в зависимости от уровня физической активности, статуса заболевания и переносимости пищи. Суточный уровень потребления белка у здоровых пожилых людей должен составлять от 1,0 до 1,2 г/кг массы тела. При наличии острого или хронического заболевания, сопровождающегося воспалением (включая системное воспаление, инфекции, раны, пролежни и т.д.), потребность в белке может быть еще выше и составлять 1,2-1,5 г/кг, а для людей пожилого и старческого возраста с серьезными заболеваниями, травмами или недостаточностью питания - до 2,0 г/кг массы тела в сутки.
Если пациент получает обычное питание с усиленной калорийностью и повышенным содержанием белка, надо позаботиться о правильной организации его кормления в соответствии с его потребностями и состоянием.
Цель нутритивной терапии заключается в улучшении или по крайней мере поддержании нутриционного статуса пациента, что должно сочетаться с мерами по повышению или сохранению тощей (особенно мышечной) массы тела.
Энтеральное питание (в том числе пероральная энтеральная поддержка, пероральное энтеральное питание) является предпочтительным вариантом нутритивной поддержки пациентов пожилого и старческого возраста, так как питание через желудочно-кишечный тракт наиболее физиологично; энтеральное питание не требует создания стерильных условий для его проведения и не вызывает осложнений, связанных с процедурой парентерального введения; пищеварительная система в силу своих физиологических особенностей сама нуждается в постоянной внутрипросветной трофической поддержке; энтеральное питание, как правило, дешевле парентерального. Основными вариантами реализации энтерального питания являются пероральное энтеральное питание обогащенными продуктами питания; пероральное энтеральное питание специальными смесями; зондовое энтеральное питание: зонд в желудок (в том числе через стому), зонд в двенадцатиперстную кишку (в том числе через стому), зонд в тощую кишку (в том числе через стому).
При добавлении к рациону сипинговых смесей их калорийность должна быть не менее 400 ккал/день, включая 30 г и более белка в день. Рекомендуемая длительность назначения сипинговых смесей - не менее 1 мес. При выборе смеси важное внимание должно быть уделено текстуре, вкусу и запаху смеси, так как органолептические характеристики смесей должны быть привлекательны для пациентов. Систематический обзор по анализу эффективности и безопасности применения высокобелковых пероральных энтеральных питаний (не менее 20% калорийности в виде белков) любой консистенции (препараты для сипинга, порошки, пудинги) на протяжении любого периода показал, что применение перорального энтерального питания по сравнению с традиционной схемой питания способствовало снижению риска развития осложнений и риска повторных госпитализаций, повышению силы пожатия кисти, повышению уровня потребления белка и калорий и оптимизации массы тела. Длительность применения таких препаратов составляет около месяца, с периодической оценкой эффективности.
В настоящее время большинство экспертов считают, что зондовое питание имеет множество негативных последствий и осложнений. Оно должно применяться только по специальным показаниям. В паллиативных ситуациях таких показаний крайне мало. В связи с этим пожилые люди в терминальной стадии заболевания должны получать комфортное для них питание, а не энтеральное зондовое питание. Зондовое энтеральное питание может быть назначено в течение ограниченного периода для преодоления кризисной ситуации, связанной с недостаточным пероральным приемом пищи, если недостаточное потребление пищи вызвано потенциально обратимым состоянием. Гастростома должна быть установлена, если ожидаемое время проведения энтерального питания будет более 4 нед или если пациент против установки назогастрального зонда.
Не рекомендуется назначать и проводить фармакологическую седацию или физические ограничения пациентам пожилого и старческого возраста для проведения зондового энтерального питания, перорального энтерального питания или гидратационной терапии.
При необходимости проведения зондовой или пероральной энтеральной поддержки у пациентов пожилого и старческого возраста начинать их следует рано; объем следует постепенно увеличивать в первые три дня для предотвращения синдрома возобновленного кормления (англ. Refeeding syndrom). В первые три дня зондового энтерального питания и перорального энтерального питания необходимо контролировать уровень фосфатов, магния, калия и тиамина в крови, а при выявлении даже небольшого дефицита перечисленных элементов следует применять соответствующие добавки. Синдром возобновленного кормления связан с потенциальным риском для пациентов с недостаточностью питания, имеющих электролитные нарушения, поскольку ведет к клиническому ухудшению. Возможные последствия включают перегрузку объемом, перераспределение фосфатов, калия и магния, гипофосфатемию, мышечную слабость, анемию и в итоге приводят к органной недостаточности, повышению риска летального исхода. У 20% пациентов может наблюдаться внезапная сердечная смерть.
Был продемонстрирован и является очевидным тот факт, что иммобилизация ведет к потере безжировой массы тела, в частности массы скелетных мышц, особенно у пожилых людей. Пациентам с анорексией-кахексией могут быть даны рекомендации по физической активности (дозированная ходьба, упражнения на сопротивление) в зависимости от общего состояния пациента и выраженности патологических нарушений. Несмотря на отсутствие веских доказательств эффективности физических упражнений в лечении кахексии, их выполнение может оказывать положительное влияние на силу мышц, а также на психологический настрой и эмоциональное состояние пациентов.
Медикаментозное лечение
Кортикостероиды (например, дексаметазон 2-6 мг в сутки) способствуют повышению аппетита и могут улучшать качество жизни пациентов, но их применение ограничено риском развития побочных эффектов, в связи с чем эти препараты назначают только короткими курсами (не более 2 нед). Наиболее доказана эффективность кортикостероидов у пациентов с кахексией, возникшей на фоне онкологических заболеваний, тогда как при кахексии, связанной с неонкологическими заболеваниями, их влияние выражено меньше.
Пациентам с кахексией онкологической природы также может быть рекомендовано назначение омега-3 жирных кислот (1,6-2,4 г в сутки).
Применение мегестрола ацетата у пожилых и старых пациентов с кахексией в настоящее время не рекомендуется, так как его влияние на аппетит и мышечную массу минимально, он не улучшает качество жизни и выживаемость пациентов, но при этом высок риск таких побочных эффектов, как тромбозы и задержка жидкости.
Тошнота и рвота могут вызывать или усугублять анорексию, поэтому при их развитии должны быть своевременно назначены соответствующие препараты с учетом ограничений, описанных в соответствующем разделе.
Особенности паллиативной помощи у пациентов с дисфагией и аспирацией
Дисфагия - это часто встречающийся синдром у пациентов, нуждающихся в паллиативной помощи, характеризующийся либо затруднением прохождения пищи в начале глотания (ротоглоточная дисфагия), либо ощущением препятствия прохождению пищи или жидкости от рта до желудка (пищеводная дисфагия).
Дисфагия является серьезным фактором риска развития и прогрессирования недостаточности питания, обезвоживания, внебольничной пневмонии, обструкции дыхательных путей и смерти (табл. 1.5).
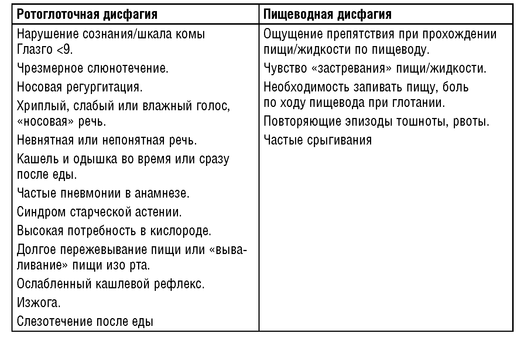
Лица, осуществляющие уход за пациентами, нуждающимися в паллиативной помощи, зачастую пропускают синдром дисфагии, особенно легкой степени, который может проявляться эпизодами бессимптомной аспирации (попадание пищи в верхние дыхательные пути без явных признаков кашля или удушья). Бессимптомную аспирацию у паллиативных пациентов можно заподозрить при появлении эпизодов необъяснимой лихорадки или кашля с ознобом, изменении объема, цвета или вязкости слюны, жалоб на боли в груди или развитии пневмонии.
Причиной ротоглоточной дисфагии чаще всего служат расстройства центральной нервной системы, включая инсульт, БП, деменцию, недавняя экстубация после длительной искусственной вентиляции легких, проведение бронхоскопии, зондовое питание, а также ксеростомия и проблемы с зубными протезами. Развитию ксеростомии способствует прием таких препаратов, как антихолинергические средства (ипратропия бромид, атропин, скополамин*), α-адреноблокаторы (доксазозин, тамсулозин), ингибиторы ангиотензинпревращающего фермента, блокаторы ангиотензиновых рецепторов II типа, антиаритмические препараты (дизопирамид, мексилетин), антигистаминные, диуретики, опиаты, нейролептики.
Наиболее частыми причинами пищеводной дисфагии являются:
• поражение слизистой оболочки, которое приводит к сужению просвета вследствие воспаления, фиброза или роста опухоли;
• болезни средостения, которые приводят к обструкции пищевода путем прямой инвазии или за счет увеличения лимфатических узлов;
• нейромышечные заболевания, поражающие гладкие мышцы пищевода и его иннервацию, нарушающие перистальтику либо работу нижнего пищеводного сфинктера, или то и другое;
• прием препаратов, вызывающих прямое повреждение слизистой оболочки пищевода, - антибиотики (доксициклин, тетрациклин, клиндамицин, ко-тримоксазол), НПВП, алендроновая кислота, зидовудин, аскорбиновая кислота, калия хлорид, теофиллин, хинидина глюконат*, железа сульфат;
• прием препаратов, снижающих давление в нижнем пищеводном сфинктере и усиливающих гастроэзофагеальный рефлюкс, - гиосцина бутилбромид (Бускопан*), теофиллин, нитраты, блока-торы медленных кальциевых каналов.
Основным направлением в борьбе с дисфагией у пациентов, нуждающихся в паллиативной помощи, является немедикаментозное лечение.
1. Планирование времени приема пищи так, чтобы оно совпало с более высоким уровнем функциональной активности пациента.
2. Если пациент вследствие истощения не может завершить прием пищи, рекомендуется переход на частые (6-7 раз в день), регулярные приемы пищи небольшими порциями.
3. Рекомендуется принимать пищу в положении сидя, слегка наклонив голову вперед; если получится, в момент глотка задержать дыхание и наклонить подбородок вниз. Следует сохранять такое положение тела в течение 45-60 мин после еды. Если имеется слабость разгибателей мышц шеи (голова свисает вперед) и слабость в руках, ни в коем случае не стоит усердствовать и наклонять голову к руке с вилкой. Голова должна быть лишь слегка наклонена вперед, а при выраженной слабости даже зафиксирована при помощи полужесткого или жесткого головодержателя. Для того чтобы поднести пищу ко рту, можно пользоваться вилками и ложками с длинными гибкими ручками или помощью других людей (сиделки или родственников, осуществляющих уход).
4. Есть нужно медленно, тщательно пережевывая пищу, не разговаривая во время еды.
5. Размер одной порции для глотания должен быть не более 1/2 чайной ложки.
6. Необходимо чередовать прием твердой пищи с маленьким глотком воды.
7. Необходимо концентрироваться на процессе глотания, не следует отвлекаться на прослушивание радио или просмотр телевизора.
8. Начинать говорить следует, только проглотив всю пищу, которая находилась в ротовой полости.
9. При необходимости следует хорошо откашляться, чтобы не дать пище спуститься в дыхательные пути, а после этого - глотать немедленно, прежде чем будет вдох.
10. Не следует есть в одиночестве. Очень важно, чтобы люди, которые ухаживают за больным, были обучены приему Геймлиха, то есть специальной технике, с помощью которой можно удалить пищу из дыхательных путей.
11. Необходимо обязательно очищать рот после еды.
12. Объем жидкости в сутки должен составлять минимум 1,5-2 л, включая чай, супы и другие жидкие продукты питания.
13. Для стимуляции глотания можно использовать кислую пищу, чередовать холодную и горячую пищу. Однако следует избегать слишком горячей пищи.
14. Для стимуляции глотания можно надавливать ложкой на язык во время кормления.
15. Если при глотании жидкости больной поперхивается, нужно попробовать использовать более густые жидкости (кисели, нектары, простоквашу, йогурты). Нужной густоты можно добиться, добавляя в напитки загустители - желатин, порошки для детского питания.
16. Пища должна аппетитно выглядеть, иметь интенсивный аромат. При приготовлении пищи рекомендуется использовать специи и лимонную кислоту, что способствует улучшению глотательного рефлекса за счет улучшения вкуса и стимуляции кислотой.
17. Пища должна быть однородной, пюреобразной консистенции. Не следует употреблять в пищу продукты, содержащие жидкие и твердые части (непюреобразные супы, виноград, апельсины и т.д.). Избегайте употребления липких, рассыпчатых продуктов, таких как мед, сгущенное молоко, изделия из песочного теста.
Таким образом, рацион должен состоять из продуктов, приготовленных так, чтобы они легко глотались:
• если каша, то жидкая («размазня», лучше овсянка, гречка);
• если мясо, рыба или птица, то суфле или котлеты на пару;
• если овощи, то отварные, тушеные, либо мелко протертые, либо пропущенные через блендер;
• если картофель, то пюре;
• нужно избегать приема сладких, кислых, острых блюд, так как это вызывает повышенное образование слюны и увеличивает слюнотечение, которое приносит неудобство;
• вместо хлеба и макарон рекомендуют каши: овсяную, гречку в виде «размазни», изредка манную. Лучше не есть орехи, сырые овощи и фрукты, гренки, баранки, сухари, жареное мясо, так как их крайне трудно проглотить.
При необходимости для увеличения калорийности рациона можно добавить сливочное или растительное масла, сметану, творог, сливки с повышенной жирностью.
Если невозможно компенсировать энергетические потребности при обычном питании, можно использовать дополнительные смеси, например «Нутридринк крем», который имеет консистенцию пудинга, что облегчает процесс глотания.
1. Контроль за приемом медикаментов. Проглатывание пероральных препаратов может представлять огромные проблемы для пациентов с дисфагией, поскольку трудности с глотанием могут повлиять на приверженность пациента к приему лекарственных препаратов. Лекарства могут быть измельчены и добавлены целиком в пюреобразную пищу, такую как пюре, каши. В то же время измельчение препаратов может привести к изменению их фармакологических свойств, что необходимо учитывать при принятии решения о назначении и способе приема препаратов. Так, измельчение препаратов с отсроченным высвобождением (например, морфина пролонгированного высвобождения или оксикодона*) может привести к быстрому высвобождению действующего вещества и к смерти. В таком случае необходимо искать альтернативные пути введения препаратов, включая трансдермальный, интраназальный, внутривенный, ректальный или сублингвальный.
2. Использование аппаратов для механической инсуффляции-экссуффляции, имитирующих естественный кашель для очистки дыхательных путей и профилактики синдрома аспирации. Действие аппаратов основано на постепенном увеличении положительного давления воздуха в дыхательных путях, а затем быстрой его смене на отрицательное давление. Возникающий сильный поток выдоха вызывает глубокий естественный кашель. Чередование давления в дыхательных путях, а также возможность применения режима воздушной осцилляции позволяют эффективно рекрутировать легочную ткань и мобилизовать (высвободить) мокроту из нижних отделов легких.
3. Своевременная очистка дыхательных путей и борьба с гиперсаливацией (сиалорея, избыточное слюнотечение). Нарушение функции глотания, снижение частоты глотания, боль при глотании, нарушение вертикального положения головы, невозможность полностью закрыть рот, снижение кашлевого и глотательных рефлексов ведут к развитию синдрома гиперсаливации у паллиативных пациентов. В свою очередь избыточное слюноотделение усугубляет синдром дисфагии, вызывает периоральное растрескивание кожи, ее мацерацию и вторичное инфицирование, повышает риск дегидратации, аспирации и пневмонии.
Для борьбы с гиперсаливацией используют медикаментозные и немедикаментозные методы лечения.
К немедикаментозным методам лечения относят следующие.
• Изменение положения головы и тела для облегчения глотания: положение сидя, слегка наклонив голову вперед.
• Использование воротника для поддержания головы при ее запрокидывании.
• Сон на боку, подложив мягкую салфетку под щеку, чтобы слюна свободно стекала из уголка рта.
• Санация полости рта.
• Надо следить за тем, чтобы пациент не помещал свои пальцы или другие предметы в рот, так как эти действия будут стимулировать слюноотделение.
• Для стимуляции процесса глотания и уменьшения слюноотделения при вытирании слюны необходимо плотно прижимать губы салфеткой, а не протирать рот и подбородок.
• Проведение занятий с логопедом для увеличения степени контроля за языком. Данный метод подходит для пациентов с сохранной когнитивной функцией, так как пациент должен знать о том, когда у него происходит слюнотечение, и хотеть контролировать этот процесс, семья или лица, ухаживающие за пациентом, должны быть готовы практиковать упражнения каждый день, пациент должен быть способен выполнять целый ряд движений губами, языком и глотать по команде.
В тяжелых случаях возможно назначение медикаментозного лечения с использованием антихолинергических препаратов:
• скополамин* (гиосцин), пластыри (1 пластырь на 72 ч);
• гиосцина бутилбромид в таблетках или в виде свечей;
• атропин, глазные капли 1% - по 1 капле (0,5 мг/кап) каждые 2-4 ч под язык;
• гликопирролат* 0,1 мг, при необходимости каждые 6 ч.
Тем не менее данные препараты следует назначать с осторожностью, так как они могут вызвать спутанность сознания, галлюцинации, запоры, задержку мочи и сонливость у пожилых пациентов.
Другим возможным средством лечения гиперсаливации может быть введение ботулотоксина в область поднижнечелюстных и околоушных слюнных желез.
Источник: Паллиативная помощь в амбулаторных условиях: руководство для врачей / под ред. О.Ю.Кузнецовой. - Москва: ГЭОТАР-Медиа, 2021.
28.07.2021 | 13:29:13