Ревматическая лихорадка. Причины, классификация и клиника ревматической лихорадки. Диагностика, лечение ревматической лихорадки. Профилактика.
Раздел: Статьи
/
Общая врачебная практика.
/
Ревматология.
/
Ревматическая лихорадка. Причины, классификация и клиника ревматической лихорадки. Диагностика, лечение ревматической лихорадки. Профилактика.
Содержание
Введение
Эпидемиология
Этиология
Патогенез ревматической лихорадки
Клинические проявления ревматической лихорадки
Диагностические критерии ревматической лихорадки
Классификация
Лечение ревматической лихорадки
Профилактика ревматической лихорадки
Ревматическая лихорадка (РЛ) - это системное воспалительное заболевание соединительной ткани с преимущественной локализацией в сердце (ревмокардит), суставах (ревматический полиартрит), головном мозге (малая хорея) или коже (анулярная эритема и ревматические узелки), возникающее как постинфекционное осложнение тонзиллофарингита, вызванного β-гемолитическим стрептококком группы А (БГСА), обусловленное иммунными реакциями на эпитопы стрептококка группы А и перекрестными реакциями со сходными эпотопами тканей человека.
Наиболее часто ревматической лихорадкой болеют дети старше 5 лет и подростки, после 21 года риск заболеть РЛ существенно снижается, а после 30-35 лет заболевание возникает крайне редко. Заболеваемость в 1,5 раза выше у женского пола.
В XX в. заболеваемость ревматической лихорадкой резко снизилась в странах Европы и Северной Америки, а также в России, и составляет менее 2 случаев на 100 тыс. детей школьного возраста в год или ≤1 случая хронической РБС на 1000 человек в год, что соответствует низкому эпидемиологическому риску заболевания. В то же время, высокая заболеваемость РЛ, соответствующая эпидемическому уровню - 50 и более случаев на 100 тыс. детей, сохраняется в странах Африки, в Австралии и Океании, где проживает большая часть населения всего мира.
Рецидивы ревматической лихорадки, возникающие при повторных стрептококковых инфекциях, наиболее вероятны в первый год после перенесенной РЛ, а в последующем риск рецидивов постепенно снижается, в том числе и с каждым годом увеличения возраста при первой атаке.
Возможно полное выздоровление больных, перенесших РЛ, однако у 20-25% больных, перенесших первичный ревмокардит, формируются пороки сердца. В странах с высокой заболеваемостью РЛ через 5 лет после первой атаки РЛ примерно у половины больных диагностируется РБС, и примерно у четверти больных уже есть проявления ХСН. Нарастание частоты пороков со временем может быть связано с естественной эволюцией изначально субклинического повреждения клапанов, но, более вероятно, обусловлено кумулятивным эффектом рецидивов РЛ.
Ревматическая лихорадка является серьезной проблемой здравоохранения в связи с развитием РБС, что, по данным ВОЗ, является главной причиной сердечно-сосудистой смертности в первые четыре десятилетия жизни. Ежегодно в мире выявляется около 1 млн молодых людей, нуждающихся в операции на клапанном аппарате сердца после перенесенной РЛ (WHO, 1999, 2005).
Этиологическим фактором ревматической лихорадки является β-гемолитический стрептококк группы А, что подтверждается хронологической связью с перенесенной острой респираторной стрептококковой инфекцией (ОРСИ). К острой респираторной стрептококковой инфекция относятся 6 заболеваний: фарингит, ангина, скарлатина, отит, ринит, лимфаденит переднешейных лимфатических узлов. Обычно РЛ развивается после острого тонзиллофарингита, при этом риск развития ревматической лихорадки после нелеченого эпизода стрептококкового тонзилло-фарингита оценивается в 0,2-3%.
Другими доказательствами стрептококковой этиологии РЛ являются иммунологические (обнаружение у больных в период РЛ АТ к продуктам жизнедеятельности БГСА в высоких титрах) и профилактические (применение пролонгированных пенициллинов для профилактики повторных ОРСИ после перенесенной РЛ существенно снижает повторные атаки РЛ).
Гипотезы об участии некоторых вирусов в этиологии РЛ не нашли подтверждения.
β-гемолитический стрептококк группы А - грамположительные кокки с гемолитической активностью, колонизируют слизистые оболочки носоглотки и кожные покровы и вызывают ряд инфекционных заболеваний. Основной способ заражения - воздушно-капельный, передаче стрептококковой инфекции способствует прямой контакт с секретами полости рта и дыхательных путей (ДП) и скученность проживания. β-гемолитический стрептококк группы А чувствительны к пенициллинам и цефалоспоринам, хотя могут быть резистентными к другим антибиотикам. Лечение пенициллином укорачивает течение стрептококкового фарингита и предотвращает постстрептококковые осложнения.
По классификации R. Lancefield, в клеточной стенке БГСА имеется карбоги-дратный антиген группы А. На поверхности клеточной стенки БГСА находятся фибриллярные молекулы М-протеина. Это основной поверхностный антиген, который детерминирует антигенную типоспецифичность БГСА и является главным фактором вирулентности, определяя адгезивные свойства и резистентность бактерий к фагоцитозу. Антитела к М-антигену обладают защитными свойствами, иммунитет прочный и длительный, но из-за типоспецифичности М-антител не защищает от инфекции, вызванной другими штаммами БГСА. β-гемолитический стрептококк группы А продуцирует ряд внеклеточных ферментов и токсинов, способствующих распространению инфекции в тканях. Это стрептолизины O и S, обладающие гемолитическим, цитолитическим, кардиотоксическим действием; стрептокиназа, активирующая фибринолиз крови и повышающая инвазивные свойства стрептококка; стрептогиалуронидаза - фактор инвазии БГСА и другие.
Ревматогенные штаммы БГСА (М5, М6, М18 и др.) обычно имеют капсулу, богатую М-протеином, резистентны к фагоцитозу и иммуногенны - М-протеин, стрептолизин О, стрептокиназа, стрептогиалуронидаза, дезоксирибонуклеаза индуцируют образование антител со стойко высоким титром, что дает полезные серологические маркеры перенесенной инфекции, вызванной БГСА в период проявления РЛ, когда стрептококки уже могут не высеваться со слизистых горла. М-протеин обладает свойствами суперантигена, способного вызывать неспецифическую массовую активацию Т-лимфоцитов и индуцировать эффект аутоиммунитета. Приобретенный аутоиммунный ответ может быть, в свою очередь, усилен последующим инфицированием другими ревматогенными штаммами, содержащими перекрестно-реактивные эпитопы. Критерии ревматогенности БГСА указаны в табл. 1.14.
Таблица 1.14

Ревматическая лихорадка возникает у генетически предрасположенных людей в результате иммунопатологических процессов, индуцированных в ходе иммунного ответа после тонзилло-фарингита, вызванного ревматогенными штаммами стрептококков
Факторами риска ревматической лихорадки являются:
■ молодой возраст;
■ скученность проживания;
■ плохое питание;
■ неудовлетворительные социально-бытовые условия;
■ наследственная предрасположенность.
Патогенез РЛ представлен несколькими гипотезами.
1. Токсическая: токсины стрептококка непосредственно могут вызывать отдельные повреждения сердца в эксперименте, но не объясняют всю картину РЛ.
2. Генетическая: редкое развитие РЛ после спорадической ангины, а также более высокий риск заболевания у родственников больных ревматической лихорадкой предполагают наличие генетической предрасположенности. Наиболее изучена ассоциация РЛ с полиморфизмом DR и DQ генов II класса HLA-системы. В разных популяциях у больных ревматизмом наиболее часто выявляется HLA-DR 7 аллель. Для развития заболевания имеют значение полиморфизмы некоторых генов, участвующих в воспалительном ответе и защите от патогенов.
3. Аутоиммунное повреждение и воспаление: общепризнанный ключевой механизм повреждения и воспаления тканей - молекулярная мимикрия антигенов БГСА и многих тканей человека, обусловленная их структурным сходством. В ассоциации с измененным иммунным ответом молекулярная мимикрия приводит к перекрестным реакциям противострептококковых иммунных механизмов (антитела и клеточный иммунный ответ против антигенов БГСА) с белками человека. Есть предположение, что для аутоиммунных повреждений тканей при ревматической лихорадке может иметь значение феномен расширения эпитопа (epitope spreading) - механизм, при котором собственные иммуногенные эпитопы, отличные от индуцирующих эпитопов, становятся основными мишенями аутоиммунного ответа. Антитела против М-протеина и N-ацетил-глюкозамина БГСА перекрестно реагируют в сердце с миозином и другими белками с α-спиральной структурой (ламинином, тропомиозином, виментином и др.) и, с участием активации комплемента и Fc-рецепторов нейтрофилов и моно-нуклеаров, вызывают воспаление: активируют хемотаксис, инициируют клеточную инфильтрацию в миокарде и клапанах, активируют образование провоспалительных цитокинов. Имеются доказательства способности перекрестно-реагирующих антител к виментину (белку промежуточных филаментов соединительной ткани) и ламинину, входящему в состав базальных мембран гладких мышц и эндотелия сердца, активировать молекулы адгезии микрососудистого эндотелия сердца и эндотелия клапанов - это способствует инфильтрации клапана Т-лимфоцитами. Развитие малой хореи может быть опосредовано антителами, перекрестно-реагирующими с дофаминовыми рецепторами и дофаминовыми нейронами в базальных ганглиях мозга. Антитела, образующиеся после стрептококковой инфекции, способны также перекрестно реагировать с протеинами таких органов-мишеней, как синовия, кожа и подкожные ткани, участвуя в патогенезе артрита, анулярной эритемы и ревматических узелков.
Роль клеточного иммунитета. Изменения клеточного иммунитета при ревматической лихорадке проявляются поликлональной стимуляцией В-лимфоцитов; появлением клонов с прямым цитотоксическим действием в отношении пораженных тканей; появлением клонов с цитотоксическим действием, обусловленным образованием аутоантител; расстройством системы иммунорегуляции. При острой ревматической лихорадке клоны перекрестно-реагирующих Т-лимфоцитов (Th1, Th2, Th17), которые отвечают на стрептококковый М-протеин, инфильтрируют клапан через эндотелий, активированный АТ. Воспаление ведет к неоваскуляризации клапана, которая способствует дальнейшему накоплению в клапане Т-клеток. Т-клетки больных РЛ и РБС также перекрестно реагируют на миозин и некоторые пептиды легкого меромиозина миокарда. Продукция ФНОα и γ-интерферона инфильтрирующими мононуклеарами ткани сердца, дисбаланс цитокинов, продуцируемых Th1/Th2-клетками, и повышение экспрессии цитокинов, ассоциированное с инфильтрацией Th17, способствуют персистенции воспаления и играют главную роль в индуцировании прогрессирующего поражения клапанов (РБС) и гранулематозного воспаления в сердце.
Лихорадка у75% больных достигает фебрильных цифр 38-39 °С, реже температура субфебрильная и не сопровождается ознобом. Характерны жалобы на слабость, утомляемость, потливость.
Ревматический полиартрит - ранний клинический синдром ревматической лихорадки - наблюдается у 35-66% больных и характеризуется следующими признаками.
1. Асимметричным поражением крупных и средних суставов (коленных, голеностопных, локтевых, лучезапястных).
2. Мигрирующим («летучим») характером (при отсутствии лечения НПВП) с опуханием, покраснением, болезненностью и ограничением движений каждого пораженного сустава в течение нескольких дней (иногда до 2 нед). Может выявляться поражение одновременно нескольких крупных суставов.
Артрит проходит без остаточных изменений; деформаций суставов или деструкций не возникает. Как правило, наблюдается полиартрит (>3 суставов) или олигоартрит (1-3 сустава); моноартрит, который ранее рассматривался как редкое проявление ревматической лихорадки, в последние годы включен в диагностические критерии РЛ в ряде стран. Крайне редко встречаются атипичные проявления суставного синдрома: поражение мелких суставов кистей и стоп, асимптомные сакроилииты 1-2-й стадии по Dave, хроническая артропатия Жаку, проявляющаяся обратимой ульнарной девиацией пальцев, сформировавшейся в результате растяжения капсул пястно-фаланговых суставов при повторных атаках РЛ с вовлечением суставов кистей рук. Наблюдающиеся преимущественно у взрослых случаи изолированного артрита с укороченным латентным периодом между стрептококковой инфекцией и началом артрита до 1-2 нед в сравнении с классическим течением ревматического полиартрита, слабым эффектом ацетилсалициловой кислоты и других НПВП, наличием экстраартикулярных поражений - теносиновита и отсутствием клинических признаков кардита в последнее время некоторые исследователи выделяют в качестве самостоятельной нозологии «постстрептококковый артрит». Воспалительные поражения суставов при РЛ могут протекать и в виде полиартралгий.
Ревматический кардит, который наблюдается у 75-98% больных ревматической лихорадкой детей и подростков и у 15-69% взрослых, позволяют заподозрить «кардиальные» жалобы у молодых людей: инспираторная одышка, плохая переносимость физической нагрузки, ощущение сердцебиений и перебоев в работе сердца. Редко наблюдающиеся тупые продолжительные боли в области сердца могут указывать на вовлечение в воспалительный процесс перикарда. При современном течении ревматической лихорадки кардит нередко бывает бессимптомным и выявляется только при аускультации сердца или УЗИ сердца.
Международные критерии кардита следующие.
1. Органический шум (шумы), ранее не выслушиваемые, или динамика ранее существовавших шумов.
2. Увеличение сердца (кардиомегалия).
3. Застойная сердечная недостаточность у молодых лиц.
4. Шум трения перикарда или признаки выпота в полость перикарда.
Наиболее постоянным и диагностически значимым признаком ревмокардита является шум в сердце. К шумам, свидетельствующим о наличии ревмокардита, эксперты ВОЗ относят следующие.
■ Проявлением ревматического вальвулита митрального клапана является длительный, дующий, систолический шум над верхушкой, связанный с 1 тоном, обычно проводящийся в левую подмышечную область и отражающий МР - это ведущий симптом ревматического кардита. Интенсивность шума вариабельна, особенно на ранних стадиях заболевания, но существенно не изменяется при изменении положения тела и при дыхании. Данный шум следует отличать от мезосистолического «щелчка» и/или позднего систолического шума при пролапсе митрального клапана.
■ Мезодиастолический шум над верхушкой (шум Carey Coombs), формирующийся во время диастолы в результате ускоренного тока крови из предсердий в желудочки при дисфункции утолщенных створок митрального клапана при вальвулите. Шум лучше выслушивается в положении лежа на левом боку при задержке дыхания на вдохе, имеет переходящий характер и часто пропускается или смешивается с 3 тоном. Наличие этого шума делает диагноз митрального вальвулита достоверным.
■ Протодиастолический шум над аортой и в точке Боткина-Эрба, характерный для вальвулита аортального клапана, - это высокочастотный дующий, затухающий, непостоянный шум.
Отсутствие шумов в сердце при аускультации не исключает ревмокардит; по разным данным, у 16 -18% больных с подтвержденными на ЭхоКГ признаками ревмокардита шум не выслушивался - такие случаи называют «субклинический ревмокардит». Аускультация клапанных шумов может быть затруднена при тахикардии, застойной сердечной недостаточности из-за низкого систолического объема или при перикардите из-за шума трения перикарда или выпота. Шум трения перикарда выслушивается при ревмокардите редко, как правило, вовлечение перикарда определяется только инструментальными методами исследования.
У больных ревмокардитом обычно наблюдаются тахикардия, не соответствующая температуре, приглушенность тонов сердца. Для диагностики и оценки тяжести ревмокардита имеет значение выявление расширения границ сердца и таких проявлений сердечной недостаточности, как увеличение ЧДД, появление акроцианоза, застойных влажных хрипов в легких, отеков нижних конечностей и других симптомов сердечной недостаточности (СН).
Выделяют 3 степени тяжести ревмокардита - легкую, среднетяжелую и тяжелую (табл. 1.15).
Таблица 1.15. Степень тяжести ревмокардита
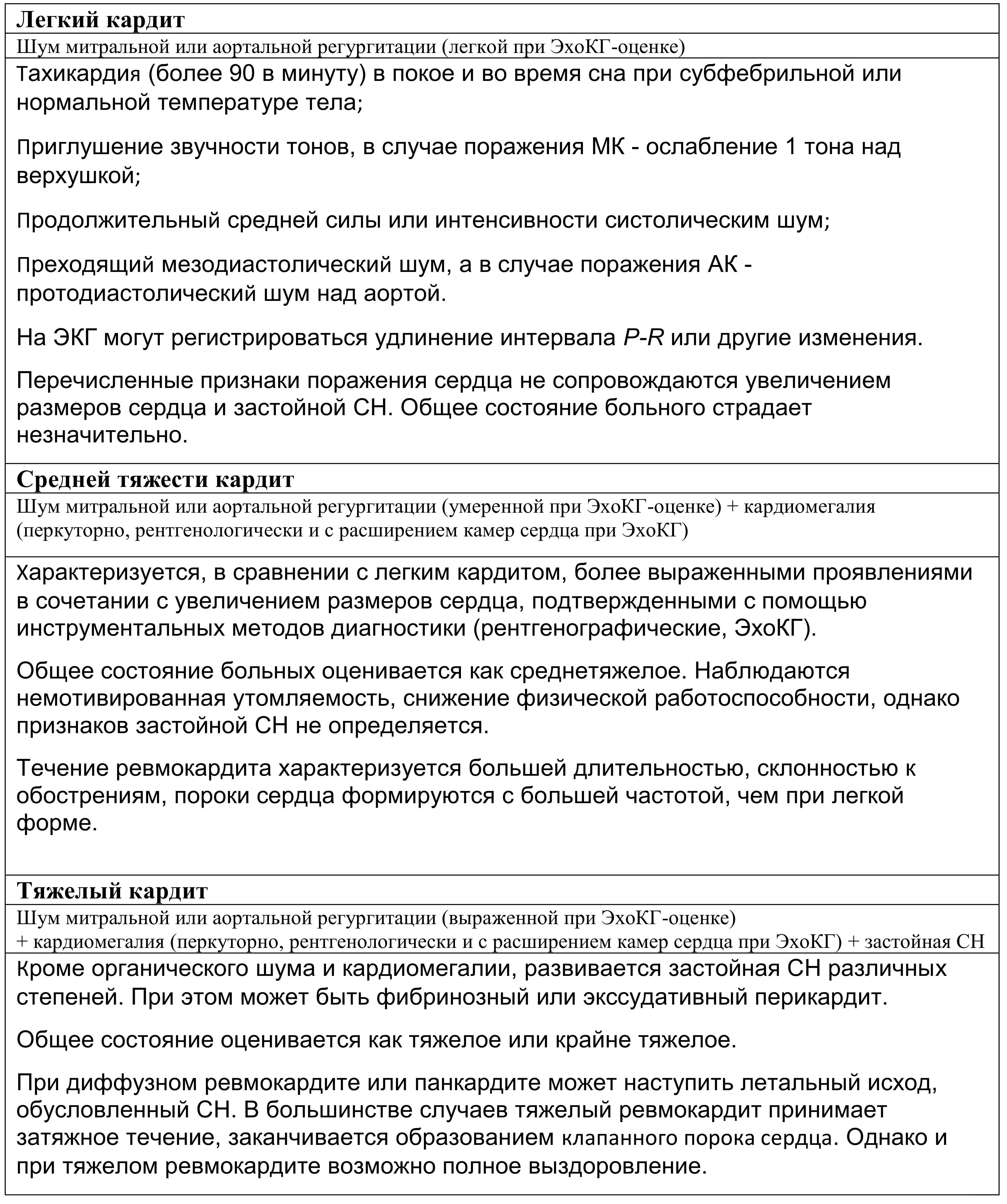
Упрощенно эту градацию можно представить следующим образом: при наличии только одного первого критерия (органический шум) речь идет о кардите легкой степени, при добавлении второго критерия (кардиомегалия) - о кардите средней тяжести, при добавлении третьего критерия (симптомы СН) или сочетании всех четырех признаков кардита - о кардите тяжелом.
Возвратный ревмокардит на фоне сформированного клапанного порока сердца (КПС) диагностировать значительно труднее. При этом решающее значение имеют доказательства недавно перенесенной стрептококковой инфекции, а также знание данных о состоянии сердечно-сосудистой системы в период, предшествующий рецидиву: появление нового шума или изменение интенсивности и продолжительности имевшегося ранее шума, увеличение по сравнению с исходными размеров сердца, появление или нарастание признаков застойной СН, развитие перикардита при наличии критериев ревматической лихорадки и изменения лабораторных показателей дают возможность диагностировать возвратный ревмокардит и определить степень его тяжести.
Инструментальные методы диагностики ревмокардита.
1. При ЭКГ-исследовании может отмечаться нарушения ритма и нарушение проводимости: преходящая АВ-блокада первой, реже второй степени, экстрасистолия, изменения зубца Т в виде снижения его амплитуды вплоть до появления негативных зубцов. Указанные изменения ЭКГ нестойкие, быстро исчезают в процессе лечения. При развитии ревмокардита на фоне уже имеющегося КПС ЭКГ отражает изменения, свойственные данному пороку.
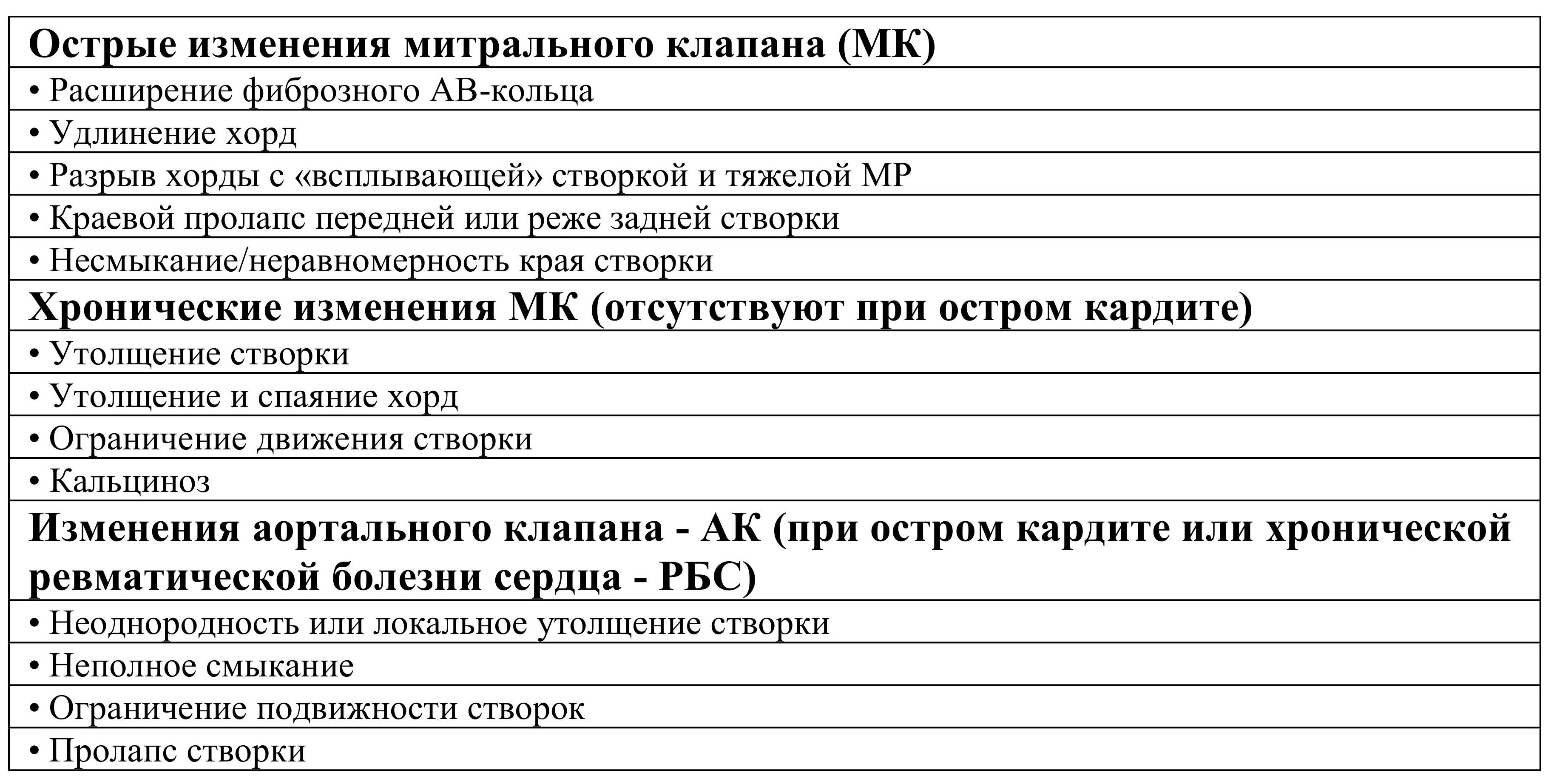
2. Основным инструментальным методом, позволяющим диагностировать ревмокардит, является двухмерная ЭхоКГ с использованием допплеровской техники, которая позволяет оценить анатомическую структуру и функцию клапанов сердца, размер камер сердца и сократительную функцию миокарда, а также установить наличие перикардиального выпота. ЭхоКГ должна выполняться в динамике всем больным с подтвержденным или предполагаемым диагнозом РЛ, в том числе больным без клинических проявлений кардита. Диагностика вальвулита основывается на выявлении патологической клапанной регургитации (табл. 1.16) и морфологических изменений створок (табл. 1.17). Благодаря использованию ЭхоКГ стало возможным распознавание субклинического кардита с клапанной регургитацией без аускультативных симптомов.
Таблица 1.16. Допплерографические признаки ревматического вальвулита (Американская ассоциация сердца, 2015)

Таблица 1.17. Эхокардиографические морфологические признаки ревматического вальвулита (Американская ассоциация сердца, 2015)
Рентгенография грудной клетки позволяет выявить расширение границ сердца и признаки венозной ЛГ при тяжелом кардите. Общее состояние больных РЛ может варьировать от удовлетворительного до тяжелого, и именно ревмокардит является определяющим критерием тяжести ревматической лихорадки.
У 10-30% больных РЛ при осмотре выявляется поражение нервной системы - малая хорея. Клинические проявления ревматической (малой) хореи, описанной Томасом Сиденхамом в 1686 г., суммированы в пентаде симптомов:
1) множественные насильственные движения (гиперкинезы) мышц лица, туловища, конечностей;
2) мышечная гипотония, вплоть до дряблости мышц, с имитацией параличей (chorea mollis);
3) стато-координационные нарушения (нарушения почерка и походки);
4) сосудистая дистония;
5) психопатологические явления (эмоциональная лабильность, нарушение сна).
Малая хорея может быть изолированной или протекать в сочетании с другими проявлениями РЛ, в том числе с кардитом и формированием различных ревматических пороков сердца.
При подозрении на ревматическую лихорадку у больного следует тщательно осмотреть кожные покровы и пальпировать подкожную клетчатку над крупными суставами для выявления таких редких проявлений РЛ, как кольцевидная эритема и подкожные ревматические узелки.
Кольцевидная (анулярная) эритема наблюдается в <6% случаев заболевания и характеризуется бледно-розовыми кольцевидными разных размеров высыпаниями, локализующимися в области плеч, голеней, предплечий, бедер, на туловище (но не на лице). Она не сопровождается зудом или индурацией и бледнеет при надавливании. В связи с транзиторным мигрирующим характером сыпи для ее выявления нужно осматривать кожу пациентов в динамике.
Подкожные ревматические узелки - безболезненные, плотные, округлые, малоподвижные, быстро возникающие и исчезающие образования в фасциях, апоневрозах на разгибательных поверхностях суставов, в области лодыжек, остистых отростков, а также затылочной области наблюдаются редко (в 0-10% случаях РЛ) и ассоциируются с тяжелым или средне-тяжелым ревмокардитом.
Абдоминальный синдром - наиболее раннее проявление РЛ. В клинической картине доминируют симптомы «острого живота», в основе которого лежит асептический перитонит.
У 75-80% больных ревматическая атака стихает по клинико-лабораторным данным в течение 6 нед, примерно у 90-95% к 12 нед (острое течение) и лишь у 3-5% больных атака продолжается более 6 мес, т.е. принимает затяжное течение. При повторной атаке историю заболевания следует рассмотреть с первого эпизода РЛ, обращая внимание на «подражательный» характер повторных атак ревматической лихорадки в большинстве случаев.
При РЛ отмечается повышение неспецифических «острофазовых показателей» крови, к которым относятся: нейтрофильный лейкоцитоз (но не более 12 000- 15 000), диспротеинемия с повышением уровня α2- и γ-глобулинов; увеличение СОЭ; повышение уровня СРБ.
Лабораторными доказательствами недавно перенесенной стрептококковой инфекции являются: увеличение титров АСЛО или других стрептококковых АТ, выделение БГСА при взятии посева из зева и выявление карбогидратного антигена стрептококка группы А в мазке с миндалин экспресс-тестом. Титры стрептококковых АТ АСЛО, АСГ, АСК, АДНК-Б необходимо исследовать в динамике. Их нарастание происходит в течение 4 нед после ОРСИ, нормализация - в течение 2-4 последующих месяцев. У 20% больных повышение титра стрептококковых АТ может сохраняться до 12 мес. Повышение хотя бы одного из титров АТ ретроспективно свидетельствует о перенесенной стрептококковой инфекции.
В настоящее время в соответствии с рекомендациями ВОЗ наиболее широко применяются следующие диагностические критерии Джонса, пересмотренные ВОЗ в 2003 г. (табл. 1.18).
Таблица 1.18. Диагностические критерии ревматической лихорадки Джонса в модификации ВОЗ (ВОЗ, 2003)
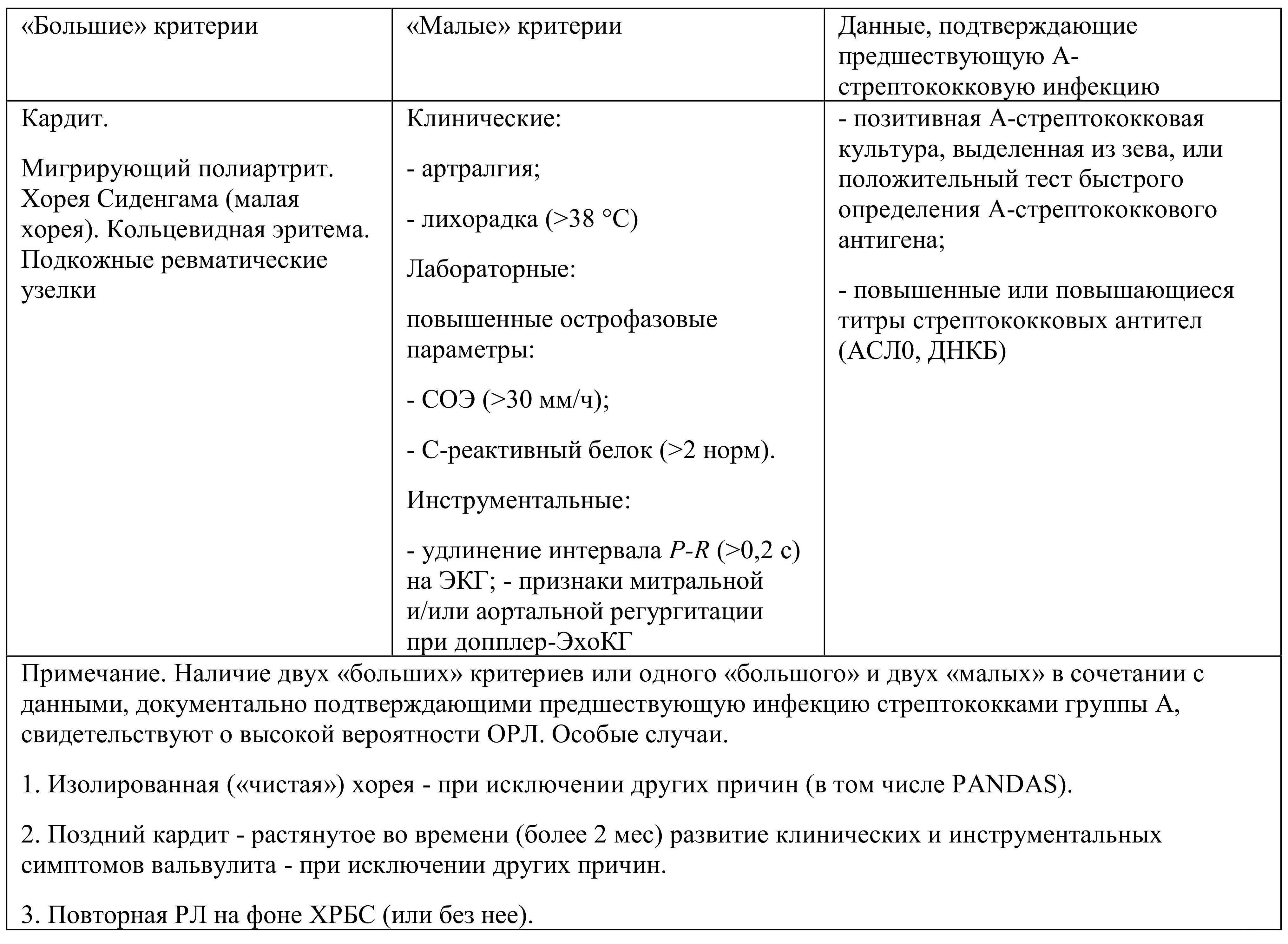
Наличие двух больших или одного большого и двух малых критериев в сочетании с доказательствами предшествующей стрептококковой инфекции свидетельствует о достоверном диагнозе РЛ. Исключениями из диагностического правила, не требующими серологического подтверждения перенесенной ОРСИ, являются позднее возникновение кардита и малая хорея с длительным латентным периодом, ко времени проявления которых титры противострептококковых антител уже снижаются.
Диагностические критерии применимы для диагностики как первичной ревматической лихорадки, так и ее рецидивов. Особо необходимо подчеркнуть, что при диагностике повторной атаки РЛ у взрослых необходимо проводить дифференциальную диагностику с инфекционным эндокардитом, который может имитировать ревматическую атаку.
Признаками инфекционного эндокардита являются:
1) высокая лихорадка, сопровождающаяся ознобами;
2) появление новых шумов регургитации;
3) вегетации на клапанах при ЭхоКГ-исследовании;
4) положительная гемокультура;
5) спленомегалия, анемия, системные тромбоэмболии.
В последние годы в связи с учащением случаев выявления субклинического ревмокардита, более частым моноартритом, а также доказательствами разной диагностической значимости клинических проявлений в популяциях с разным эпидемиологическим риском РЛ критерии Джонса были пересмотрены экспертами ряда стран. В 2015 г. экспертами AHA были предложены следующие пересмотренные диагностические критерии РЛ. Эксперты Ассоциации ревматологов России обсудили пересмотренные AHA критерии Джонса и в целом одобрили их, однако внесение изменений в существующую Российскую классификацию и номенклатуру острой РЛ посчитали преждевременным.
Классификация ревматической лихорадки представлена в табл. 1.19.
Таблица 1.19. Классификация ревматической лихорадки Ассоциации ревматологов России (2003)
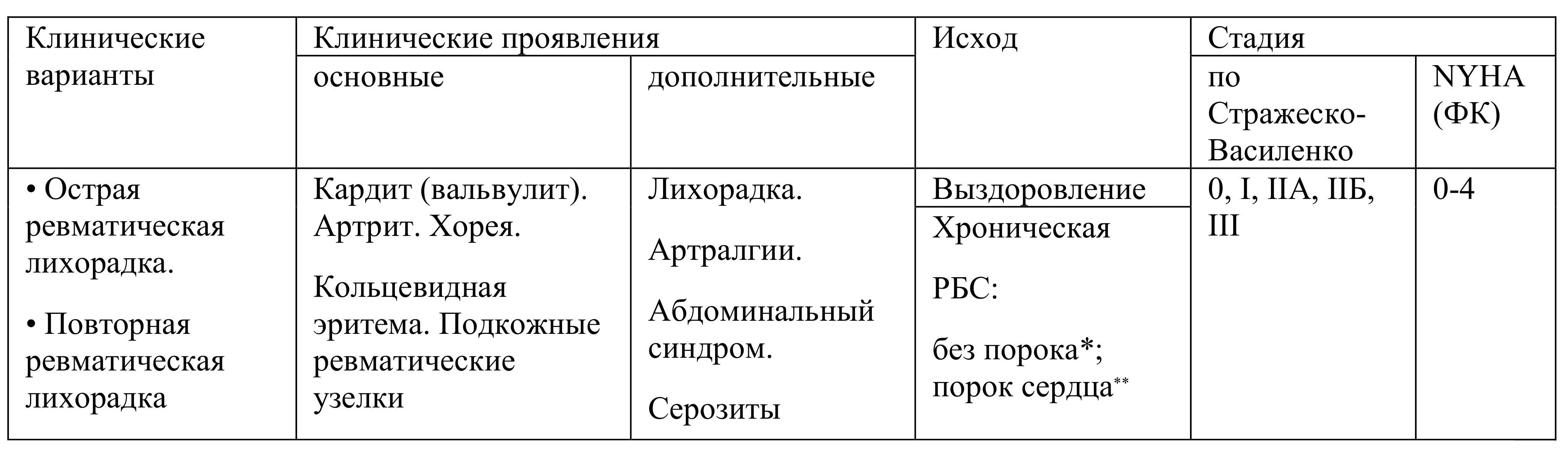
* Наличие поствоспалительного краевого фиброза клапанных створок без регургитации, которое уточняется с помощью ЭхоКΓ.
** При впервые выявленном пороке сердца необходимо исключить другие причины его формирования (инфекционный эндокардит, первичный антифосфолипидный синдром, кальциноз клапанов дегенеративного генеза и др.).
Всем больным РЛ рекомендуется госпитализация с целью подтверждения диагноза, лечения и начала вторичной профилактики заболевания.
Режим физической активности больного ревматической лихорадкой определяется наличием ревмокардита и степенью его тяжести. Больным с ревмокардитом в легкой форме постельный режим рекомендуется на срок не менее 4 нед. В случае сохранения или нарастания симптомов ревмокардита постельный режим назначается по крайней мере до 6 нед. В целом ограничение нагрузки рекомендуется не менее 12 нед. При ревмокардите средней степени тяжести назначается строгий постельный режим на первые 2 нед - период кардиомегалии, затем постельный на 4 нед и в последующем палатный и амбулаторный на 6-8 нед до исчезновения признаков ревмокардита. При тяжелом ревмокардите строгий постельный режим назначается на сроки до исчезновения симптомов сердечной недостаточности и кардиомегалии - 2-3 нед, постельный - на 4-6 нед, палатный (домашний) на 4-6 нед и амбулаторный на 8-10 мес. Больным с ревматическим полиартритом назначается постельный режим на срок не менее 3 нед. Режим физической активности больного ревматической хореей назначается в зависимости от того, имеется ли изолированная хорея или она сочетается с ревмокардитом. Больной хореей нуждается в комфортабельной обстановке, обеспечении душевного покоя, приветливом отношении родителей и окружения. При чрезмерно выраженных гиперкинезах рекомендуется поставить высокие мягкие ограждения с обеих сторон кровати, чтобы избежать возможности ушибов, падения с кровати и т.п. По окончании ревматической атаки режим физической активности определяется с учетом последствий ревмокардита.
Режимы физической активности при РЛ представлены в табл. 1.20.
Таблица 1.20. Режим физической активности при ревматической лихорадке в активной фазе

Диета больного ревматической лихорадкой не представляет каких-либо особенностей. При тяжелом ревмокардите необходимо ограничить поваренную соль. Ограничение употребления соли показано также при лечении глюкокортикоидами, в связи с их способностью повышать реабсорбцию натрия. Вместе с тем следует предусмотреть употребление продуктов с высоким содержанием калия (картофель, томаты, дыни, урюк, курага).
Медикаментозная терапия
Этиотропная антистрептококковая терапия
Всем больным с момента диагностики PЛ назначается лечение антибиотиком, обеспечивающим удаление БГСА из носоглотки, с учетом чувствительности БГСА применяются пенициллины или, при аллергии к пенициллинам, макролиды:
■ пенициллины внутрь - феноксиметилпенициллин (V-пенициллин) 500 мг 2-3 р/день (при массе тела ≥20 кг) или амоксициллин 1000 мг 1 р/день (при массе тела ≥30 кг) или по 500 мг 3 р/день в течение 10 дней;
■ в случае недавней ОРСИ с признаками активного тонзиллита или фарингита (гиперемия зева или задней стенки глотки, наличие слизи и «пробок» в миндалинах, увеличение подчелюстных лимфатических узлов) предпочтительно провести лечение бензилпенициллином в суточной дозе 1,5-3 млн ед. внутримышечно в течение 10-14 дней;
■ если предшествующая стрептококковая инфекция протекала бессимптомно или с минимальными клиническими проявлениями, особенно при поздних проявлениях РЛ, допустимо начать лечение с введения дюрантной формы пенициллина - бензатина бензилпени-циллина в дозе 2,4 млн ед. внутримышечно однократно;
■ при аллергии к пенициллинам макролиды внутрь - кларитромицин. Сразу после завершения курса начальной терапии антибиотиком (через 10 дней при применении антибиотиков внутрь или через 3 нед при применении дюрантной формы пенициллина) в стационаре больному внутримышечно вводится бензатина бензилпенициллин 1 200 000 ЕД у детей при массе тела ≥30 кг и 2 400 000 ЕД у взрослых, что будет означать переход от лечения к профилактике ОРСИ и рецидивов ревматизма; в дальнейшем введение пролонгированных пенициллинов следует повторять каждые 3 нед.
Пенициллины являются антибиотиками выбора, так как БГСА не продуцируют пенициллиназу и высокочувствительны к пенициллину (штаммов, резистентных к пенициллину, не обнаружено). Пенициллины применяются в малых дозах, контролируемые исследования не выявили улучшения исходов РЛ при увеличении доз. Препараты тетрациклина, сульфаниламидов, фторхинолонов не должны использоваться для лечения и профилактики ревматической лихорадки из-за резистентности к ним стрептококков и частых побочных эффектов.
Противовоспалительная патогенетическая терапия
При установлении диагноза PЛ сразу же должна быть начата противовоспалительная терапия НПВП или ГК (табл. 1.21).
Таблица 1.21. Противовоспалительные и анальгетические препараты при лечении ревматической лихорадки
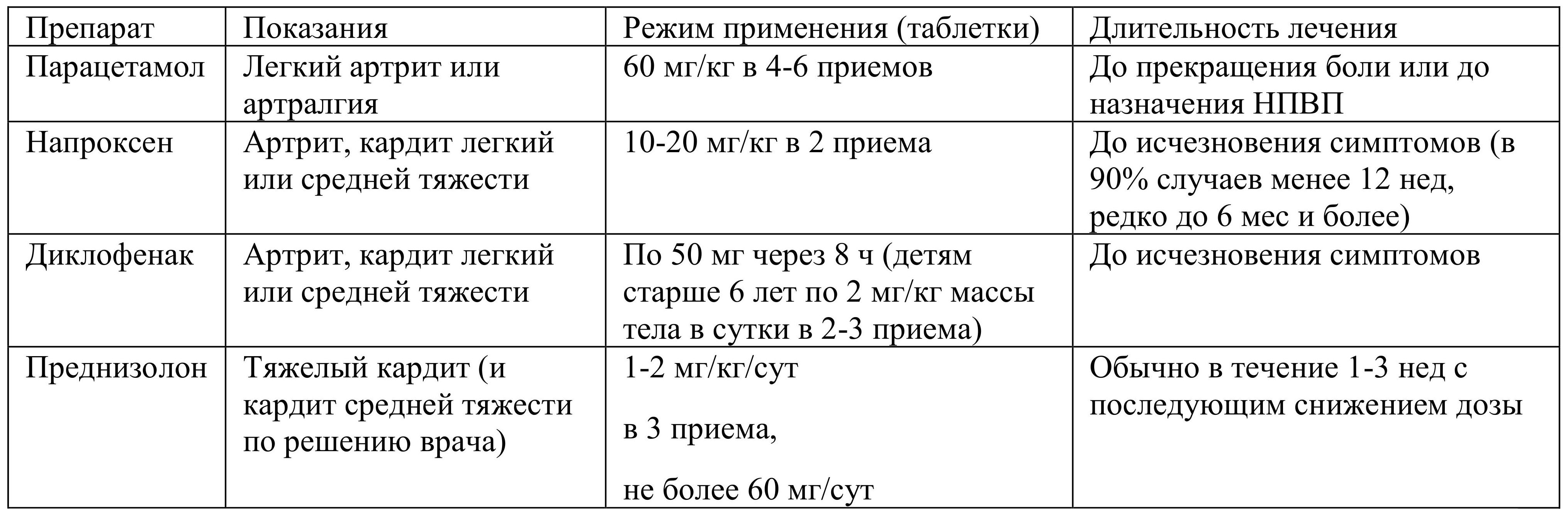
Основной механизм действия НПВП - ингибирование активности ЦОГ - основного фермента метаболизма арахидоновой кислоты, являющейся предшественником простагландинов. Известно два изофермента ЦОГ: ЦОГ-1 - регулирует продукцию простагландинов, участвующих в обеспечении физиологической активности клеток, и ЦОГ-2, активность которой регулируется цитокинами, принимающими участие в развитии иммунного ответа и воспаления. Противовоспалительное, анальгетическое и жаропонижающее действия НПВП связаны с их способностью ингибировать ЦОГ-2. При РЛ наиболее доказана эффективность лечения ацетилсалициловой кислотой в дозе 3-4 г/сут, но в связи с риском развития синдрома Reye у детей и другими побочными эффектами в последние годы рекомендуется использовать диклофенак или напроксен, как более безопасные НПВП.
Глюкокортикоиды обладают более мощным противовоспалительным эффектом, обусловленным многими факторами, главным из которых является подавление активности фосфолипазы А2. Это приводит к подавлению высвобождения арахидоновой кислоты и торможению образования ряда медиаторов воспаления - простагландинов, лейкотриенов, тромбоксана, фактора активации тромбоцитов и др. Кроме того, ГК уменьшают экспрессию гена, кодирующего синтез ЦОГ-2, дополнительно блокируя образование провоспалительных простагландинов. Преднизолон показан для лечения тяжелого кардита и может назначаться по решению врача при кардите средней тяжести.
Выбор НПВП или ГК определяется тяжестью кардита.
При легком кардите, полиартрите и изолированной малой хорее применяется напроксен в дозе 20 мг/кг 2 р/день или диклофенак в дозе 50 мг 3 р/день на весь период ревматической атаки. При появлении симптомов НПВП-гастропатии или профилактически применяют ИПП (омепразол). Антациды сразу после приема НПВП не рекомендуются, так как они снижают всасывание НПВП.
При ревмокардите средней тяжести возможен двоякий подход к назначению медикаментозной терапии в зависимости от того, чем обусловлена кардиомегалия. В первые 3 нед кардиомегалия связана преимущественно с экссудативным компонентом воспалительного процесса в миокарде, вследствие чего целесообразно назначение ГК (преднизолона) в суточной дозе 20-30 мг. По мере улучшения состояния (в среднем через 2 нед) суточную дозу преднизолона уменьшают до 5 мг, и к концу месяца преднизолон отменяют, постепенно снижая дозу. После снижения дозы преднизолона назначают НПВП в указанных выше дозировках на срок до 8 нед. При кардиомегалии, развившейся спустя 3 нед от начала ревмокардита, лечение целесообразно провести аналогично лечению легкой формы ревмокардита или полиартрита, но в течение 10-12 нед.
Ревмокардит тяжелого течения требует назначения преднизолона внутрь из расчета 1 мг/кг массы тела (но не более 60 мг/сут). При наметившемся улучшении (в среднем через 2-3 нед) дозу преднизолона уменьшают на 5 мг через 3-4 дня. Лечение НПВП следует продолжать в течение 1 мес после отмены преднизолона, а далее еще в течение 2-3 нед в уменьшенной наполовину дозировке. При лечении больных тяжелым кардитом с СН может потребоваться назначение диуретиков (или ограничение приема жидкости и соли) и ингибиторов АПФ.
К сожалению, лечение НПВП и ГК не может предотвратить формирование порока сердца, хотя есть доказательства снижения частоты формирования пороков при лечении ГК.
Лечение хореи проводится в зависимости от того, является ли она изолированной или сочетается с другими проявлениями РЛ (ревмокардитом или полиартритом). При изолированной хорее средством выбора является карбамазепин в дозе 400 мг/сут мг/сут до прекращения гиперкинезов с постепенной отменой в течение 2-3 нед. Лечение хореи в сочетании с ревмокардитом или полиартритом проводится по вышеизложенным правилам. Хорея является «самоограниченным» заболеванием, проходит у большинства больных в течение нескольких недель и практически у всех больных в течение 6 мес даже без лечения.
Лечение рецидивов ревматической лихорадки не отличается от лечения ее первой атаки, однако при наличии симптомов декомпенсации сердечной деятельности, особенно у больных с ранее сформированными пороками сердца, в план лечения чаще включают по показаниям диуретики, сердечные гликозиды, ИАПФ.
Побочными эффектами НПВП при лечении ревматической лихорадки являются:
■ НПВП-гастропатии (субэпителиальные геморрагии, эрозии и язвы желудка, реже ДПК, желудочно-кишечные кровотечения), а также энтеропатии и признаки воспаления кишечника;
■ развитие дыхательного ацидоза;
■ кровотечение из-за ингибирования адгезии и агрегации тромбоцитов;
■ нарушение функции почек;
■ анемия при длительном приеме (редко);
■ синдром Reye у детей.
Побочные эффекты ГК:
■ ульцерогенный;
■ проинфекционный, связанный с подавлением иммунитета и проявляющийся обострением хронических очагов инфекции;
■ минералокортикоидный - задержка натрия и воды с возможным появлением отеков и повышения АД.
ГК могут также вызывать гипокалиемию, гипергликемию, ожирение, появление лунообразного лица, образование стрий на коже, нарушения менструального цикла, остеопороз, бессонницу, эйфорию. Поскольку применение ГК занимает при РЛ непродолжительный период, а курсовая доза сравнительно невелика, побочные эффекты, как правило, исчезают после их отмены или коррекции диетой или медикаментозными препаратами (калийсберегающими диуретиками, седативными препаратами, гастропротекторами, анаболическими гормонами, поливитаминами и т.п.).
Синдром возврата активности ревматической лихорадки, или ребаунд. После снижения доз или отмены противовоспалительных препаратов и исчезновения клинических и лабораторных признаков активности РЛ иногда отмечается возврат клинических и/или лабораторных признаков активности ревматического процесса (артралгий, субфебрильной температуры, признаков ревмокардита, острофазовых реакций). Обычно это происходит в сроки от нескольких дней до 5 нед после прекращения лечения или снижения дозы противовоспалительных препаратов. Эти «возвраты» заболевания обозначаются как «ребаунд»-синдром. Они, как правило, не связаны с повторной стрептококковой инфекцией и поэтому не могут свидетельствовать о рецидиве РЛ. Чаще «ребаунд»-синдром возникает после преждевременной отмены ГК. Оказывая быстрое и отчетливое терапевтическое действие на токсические и экссудативные проявления, ГК не подавляют полностью воспалительный процесс и не укорачивают продолжительность атаки. Длительность их применения составляет в большинстве случаев 3-6 нед, т.е. короче, чем продолжительность атаки (в среднем 12-14 нед). Возникновение «ребаунд»-синдромов удлиняет продолжительность ревматической атаки, а также в ряде случаев утяжеляет симптомы ревмокардита.
Профилактика РЛ подразделяется на первичную и вторичную и включает комплекс социально-гигиенических и медицинских мероприятий, препятствующих заболеваемости респираторными стрептококковыми инфекциями и направленных на повышение резистентности к организма к инфекции.
Первичная профилактика
Первичная профилактика ревматической лихорадки заключается прежде всего в своевременной диагностике ОРСИ и лечении заболевших антибиотиками с целью предотвращения первой атаки РЛ, а также в санитарно-гигиенических мерах, направленных на ограничение заболеваемости ОРСИ в популяции (повышение индивидуальной резистентности к инфекции, своевременная диагностика и изоляция от контактов больного с ОРСИ).
Наиболее частыми проявлениями ОРСИ являются: фарингит, тонзиллит, реже - средний отит и синусит. Хотя острый стрептококковый тонзиллит не имеет специфических клинических маркеров, его следует предполагать при тонзиллите с острым началом, высокой температурой (37,5-39 °С) и симптомами интоксикации, болью в горле, усиливающейся при глотании с начала заболевания, гиперемией слизистой нёбных миндалин и дужек, отечностью дужек и язычка, скоплением экссудата на поверхности нёбных миндалин и в лакунах при надавливании, переднешейным лимфаденитом, лейкоцитозом, увеличением СОЭ при отсутствии других симптомов воспаления верхних дыхательных путей (кашля, ринита, охриплости голоса), а также конъюнктивита, стоматита, диареи.
Однако в 35% случаев стрептококковая инфекция протекает со стертой клинической симптоматикой, а в 40% - бессимптомно.
Для точной диагностики стрептококковых инфекций необходимо выявление БГСА лабораторными методами: обнаружение в мазке со слизистой носоглотки БГСА (культуральный метод диагностики), повышение титров стрептококковых антител (серологический метод диагностики). Забор глоточных культур следует проводить до начала лечения антибиотиками в остром начальном периоде заболевания. Чувствительность и специфичность тестов для экспресс-диагностики стрептококковых антигенов нуждаются в уточнении, и они не рекомендуются к применению в рутинной практике.
Выявление больного с ОРСИ требует его немедленной изоляции для проведения терапии. Медикаментозное лечение стрептококкового тонзиллита указано в табл. 1.22.
Таблица 1.22. Дозы и режим введения антибиотиков при остром стрептококковом тонзиллите
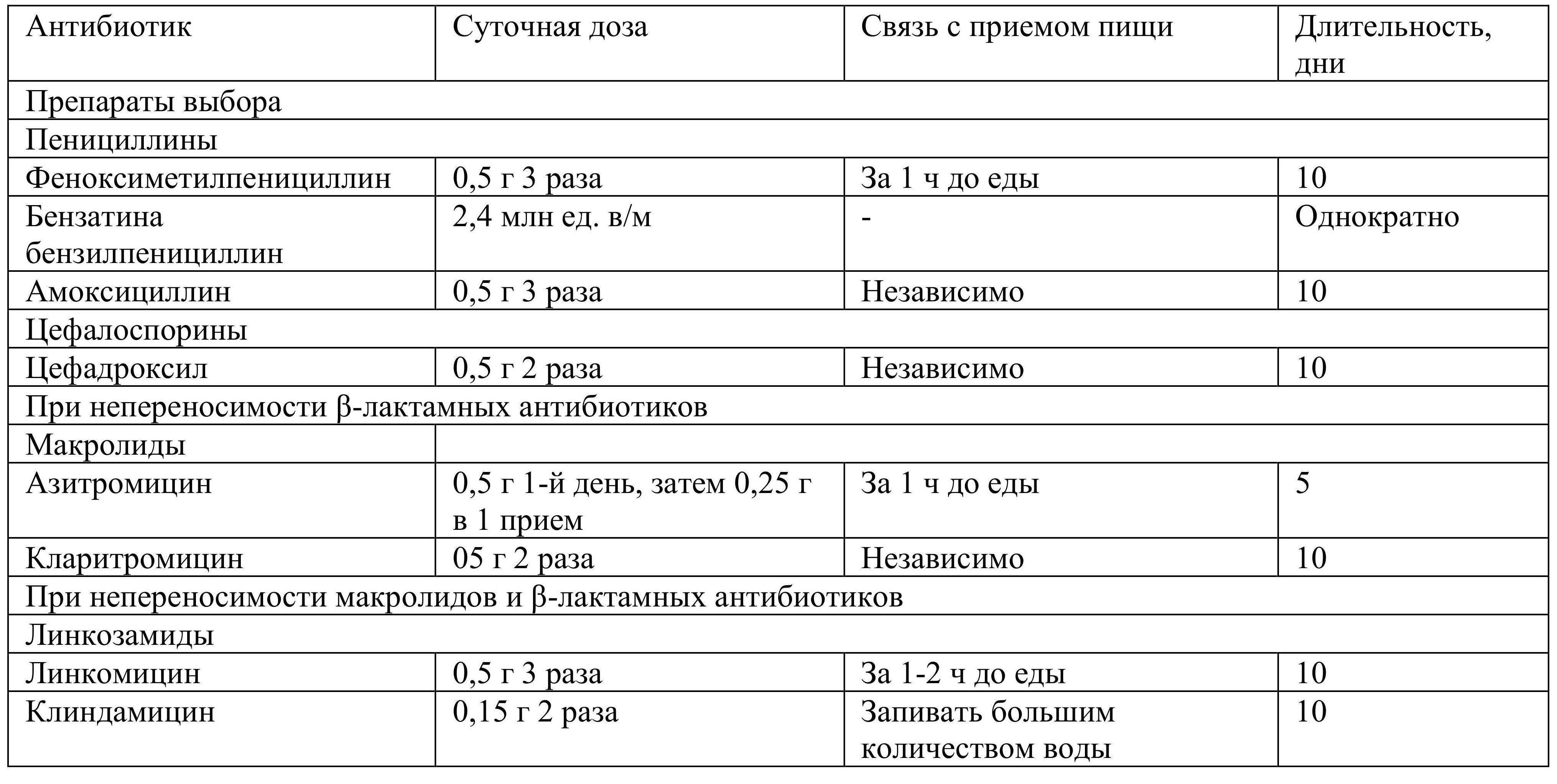
В условиях непереносимости β-лактамов возрастает роль так называемой текущей профилактики ревматической лихорадки - своевременного лечения макролидами стрептококкового тонзиллофарингита.
Длительность лечения стрептококкового тонзиллита составляет не менее 10 дней. После проведения 10-дневного курса лечения рекомендуется вновь произвести забор глоточных культур и определение титров противострептококковых антител. В случае обнаружения в мазках из носоглотки БГСА необходим повторный курс антибактериальной терапии. Если же после повторного курса лечения стрептококк вновь выделяется, таких больных необходимо рассматривать как носителей стрептококковой инфекции, которые не нуждаются в каком-либо лечении.
Большое значение придается предупреждению стрептококковой инфекции в организованных коллективах и проведению в них противоэпидемической работы.
Вторичная профилактика рецидивов ревматической лихорадки
Вторичная профилактика РЛ - комплекс мероприятий, направленных па предотвращение ОРСИ у больных, перенесших РЛ, - предусматривает длительное регулярное введение пенициллинов пролонгированного действия. У взрослых применяется бензатина бензилпенициллин в дозе 2 400 000 ЕД внутримышечно каждые 3 нед (такая частота оптимальна для поддержания эффективной концентрации антибиотика). При отказе пациента от внутримышечных инъекций возможен длительный прием феноксиметилпенициллина внутрь в дозе 500 мг 2 р/день, а при аллергии к пенициллинам - макролидов (кларитромицин 500 мг 2 р/сут) Противорецидивная профилактика должна осуществляться непрерывно в течение всего года.
Продолжительность вторичной профилактики
Существует несколько факторов, влияющих на возникновение рецидивов ревматической лихорадки. К ним относятся: возраст больного, особенности течения предшествующей атаки, время, прошедшее с момента последней атаки, кардиальный статус в исходе атаки, условия окружающей среды. Чем моложе возраст больного при первой атаке ревматической лихорадки, тем больше вероятность рецидива, после 5-летнего периода частота рецидивов, как правило, снижается с возрастом.
У больных с клапанными пороками сердца имеется более высокий риск рецидивов РЛ при инфицировании стрептококком. Отмечена зависимость частоты рецидивирования от тяжести перенесенного ревмокардита.
Социальнo-экономические условия играют огромную роль в возникновении и распространении стрептококка, а следовательно, и РЛ. Улучшение жилищнo-бытовых условий, питания, медицинской помощи влияет на возникновение рецидивов острой ревматической лихорадки. Работники дошкольных и школьных учреждений, медперсонал ревматологических и нефрологи-ческих отделений составляют также группу риска развития повторных атак.
Продолжительность вторичной профилактики следует адаптировать для каждого больного индивидуально с учетом следующих общих принципов (AHA, 2010).
1. При РЛ с кардитом и формированием порока сердца 10 лет или до 40 лет.
2. При РЛ с кардитом без формирования РБС 10 лет или до 21 года.
3. При РЛ без кардита 5 лет или до 21 года. При возникновении РЛ без кардита или с легким кардитом в возрасте старше 21 года допустимо проведение антибиотикопрофилактики в течение 5 лет. Исследования по созданию вакцины, содержащей эпитопы М-протеинов «ревматогенных» штаммов стрептококка, не вступающих в перекрестную реакцию с тканевыми антигенами человека, пока не завершились успехом, хотя применение такой вакцины, особенно у лиц - «носителей» генетического маркера ревматической лихорадки, в рамках первичной профилактики позволило бы избежать возникновения РЛ.
Источник: Рациональная фармакотерапия. Справочник терапевта: руководство для практикующих врачей / под ред. А. И. Мартынова, В. Н. Лариной. - 2-изд. - Москва: Литтерра, 2021.
05.02.2022 | 00:00:14