Интерстициальные болезни легких у детей.
Содержание
Коды по мкб-10
Общие положения
Классификация
Эпидемиология
Патофизиология
Клиническая картина
Диагностика
- лабораторная диагностика
- инструментальные методы
Определение степени тяжести и прогноз
Частные проблемы
- интерстициальная пневмония
- десквамативная интерстициальная пневмония
- синдром хаммана-рича
- облитерирующий бронхиолит
- лимфоцитарная интерстициальная пневмония
Лечение первичных заболеваний паренхимы легких
КОДЫ ПО МКБ-10
J80-J84. Другие респираторные болезни, поражающие главным образом интерстициальную ткань.
J84.1. Другие интерстициальные болезни легких с упоминанием фиброза.
J84.8. Другие уточненные интерстициальные болезни легких.
ОБЩИЕ ПОЛОЖЕНИЯ
В качестве первичных заболеваний паренхимы легких рассматривают ИБЛ (диффузные инфильтративные заболевания легких), первично поражающие альвеолы и периальвеолярные ткани с нарушением газообмена, рестрикцией легких и их диффузной инфильтрацией по данным радиологических исследований. Интерстициальные болезни легких поражают в основном дистальные воздухоносные пространства и интерстиций, поэтому более точен термин «инфильтративные заболевания легких».
Интерстициальные болезни легких у детей представляют собой большую и разнообразную группу заболеваний. В специальной литературе описано около 150 интерстициальных заболеваний. Подавляющее большинство из них встречается крайне редко. Однако врачу необходимо знать основные проявления ИБЛ и постоянно учитывать вероятность этих заболеваний в дифференциальной диагностике. Обычно в дебюте интерстициальные пневмонии рассматривают как банальные «воспаления легких», затем ошибочный диагноз трансформируется в заключение о наличии так называемой хронической пневмонии, БА. Больные длительно не получают адекватного лечения.
Спектр этой группы заболеваний, их течение, исходы и даже гистологическая картина у детей отличаются от таковых у взрослых. Так, идиопатический фиброз легких (криптогенный фиброзирующий альвеолит), наиболее частый вариант ИБЛ у взрослых, в своих классических проявлениях у детей неизвестен. Банальная интерстициальная пневмония характерна для взрослых, но редко встречается у детей. Десквамативная интерстициальная пневмония у взрослых хорошо поддается терапии глюкокортикоидами, но плохо отвечает на указанные препараты у детей, особенно младшего возраста.
У взрослых этиологический фактор ИБЛ в каждом конкретном случае расшифровать, как правило, не удается, видимо, из-за длительного латентного периода между временем действия причинного фактора и манифестацией болезни. У детей в большинстве случаев причина болезни и сама болезнь тесно сопряжены по времени, поэтому причина ИБЛ нередко поддается анамнестическому описанию.
Как уже было указано, ИБЛ у детей - не одно заболевание, а их группа, но патофизиологические механизмы едины и заключаются в ремоделировании дистальных воздухоносных путей с нарушением газообмена. Первым этапом бывает персистирующее воспаление, которое завершается атипичным выздоровлением с фиброзом. Большинство патофизиологических и патологоанатомических описаний ИБЛ строится на исследованиях взрослых и экспериментальных работах на животных. У детей патологический процесс разыгрывается в развивающемся легком, что существенно усугубляет исходы.
КЛАССИФИКАЦИЯ
ИБЛ у детей могут быть:
• Идиопатическими, то есть с неизвестной или предполагаемой причиной;
• Вторичными, сопровождающими системные заболевания. Более чем у трети пациентов причины ИБЛ остаются неизвестными.
ИБЛ с известной причиной
• Инфекция (8-10% всех случаев у детей).
✧ Вирусной этиологии. Облитерирующий аденовирусный бронхиолит (5% всех случаев ИБЛ у детей). Цитомегаловирусной этиологии или вызванная вирусом Эпстайна-Барр.
✧ Бактериальной этиологии. Chlamidia, Legionella, Mycobacterium, Mycoplasma, Pertussis.
✧ Грибковой этиологии. Aspergillus, Histoplasma, Pneumocystis.
✧ Паразитарной этиологии (миграция ларв).
• Экологические причины (13-14%).
✧ Органические загрязнители (7-12%).
✧ Неорганические загрязнители (асбест, кремний, тальк, цинк).
✧ Химические агенты (метил изоцианат).
✧ Газы (кислород, двуокись азота, аммиак).
✧ Радиация (J70.1).
• Лекарственные средства (J70.2, J70.3).
✧ Противоопухолевые препараты (азатиоприн, блеомицин, винбластин, метотрексат, арабинопиранозилметил нитрозомочевина, цитарабин, меркаптопурин).
✧ Другие препараты (препараты золота, пеницилламин).
• БЛД.
• Лимфопролиферативные заболевания (10%).
• Лимфомы (1%), лейкозы, гистиоцитоз.
• Посттравматическое легкое.
• Хроническая аспирационная пневмония (4-6%), J69.0.
• Острый РДС в стадии разрешения.
• Метаболические нарушения.
✧ Лизосомальные болезни накопления (болезни Гоше, Ниманна-Пика).
✧ Другие метаболические нарушения (синдром Германски-Пудлака).
ИБЛ неизвестной этиологии
• Неопределенные (18-28%) - неспецифические ИБЛ.
✧ Хроническая интерстициальная пневмония (пневмонит) - неспецифическая целлюлярная интерстициальная пневмония. (НО НЕ неспецифическая интерстициальная пневмония!)
• Легочный геморрагический синдром - идиопатический легочный гемосидероз (5-8%) с капилляритом легких или без него.
• Десквамативная интерстициальная пневмония (4-8%).
• Лимфоцитарная интерстициальная пневмония (пневмонит, 6%).
✧ Чаще встречается при ВИЧ-инфекции, но может быть идиопатической.
• Банальная интерстициальная пневмония (2-4%).
• Лимфангиоматоз (4%).
• Облитерирующий бронхиолит неаденовирусный (4%).
• Саркоидоз (2%).
• Альвеолярный протеиноз (2%).
✧ Врожденная форма альвеолярного протеиноза обусловлена дефицитом сурфактанта В.
• Эозинофильный синдром (2%) - хроническая эозинофильная пневмония, легочные инфильтраты с эозинофилией.
• Идиопатический облитерирующий бронхиолит с организующейся пневмонией.
• Бронхоцентрический гранулематоз (1%).
• Неспецифическая интерстициальная пневмония.
• Острая интерстициальная пневмония. ИБЛ при системных заболеваниях
• Заболевания соединительной ткани (2-4%), +J99.1.
✧ Системная красная волчанка (M35.0 +J99.1), системный склероз (M34.8 +J99.1), дерматомиозит (M33.0-33.1+J99.1), ювенильный ревматоидный артрит (M05.1), анкилозирующий спондилит, синдром Шегрена (M35.0+J99.1), синдром Бехчета.
• Легочный васкулит (ГВ, узелковый периартериит).
• Аутоиммунные заболевания (болезнь антител к базальной мембране гломерул).
• Болезни печени (хронический активный гепатит, первичный билиарный цирроз).
• Болезни толстой кишки (неспецифический язвенный колит, болезнь Крона).
• Амилоидоз.
• Реакция «трансплантат против хозяина».
• Нейрокожный синдром (атаксия-телеангиэктазия, нейрофиброматоз, туберозный склероз).
Заболевания с наличием клинической симптоматики ИБЛ
• Веноокклюзионная болезнь легких (8-10%). Аномальное впадение легочных вен, легочный гемангиоматоз, стеноз/атрезия легочной артерии.
• Болезни сердца (левожелудочковая недостаточность, лево-правый шунт).
• МВ.
• Первичные ИД.
В качестве детских вариантов ИБЛ рассматривают дисплазию ацинусов, врожденную альвеолярную дисплазию, альвеолярно-капиллярную дисплазию с нарушением венозного оттока, ХЗЛ у недоношенных и доношенных новорожденных, вторичную гипоплазию легких, хромосомные аномалии (в том числе трисомию 21), мутацию протеинов В- или С-сурфактанта, мутации АВСА3 или TTF-1, гиперплазию нейроэндокринных клеток, легочный микролитиаз.
Редкость ИБЛ у детей, патофизиологические, гистохимические и иммунные отличия от взрослых затрудняют создание единой классификации и общепринятых схем лечения.
ЭПИДЕМИОЛОГИЯ
По европейским данным, распространенность ИБЛ среди иммунокомпетентных детей составляет 0,36 на 100 тыс. Детского населения, в то время как у взрослых - 60-80 на 100 тыс. С учетом сложностей диагностики, недостаточного знакомства большинства врачей с проблемой, отсутствия единого регистра распространенность ИБЛ может оказаться выше. Около 10-16% всех случаев ИБЛ - семейные.
ПАТОФИЗИОЛОГИЯ
В большинстве случаев ИБЛ возникают у детей младшего возраста, но манифестируют в школьном или даже подростковом возрасте. Изучение патофизиологии ИБЛ проводили в основном на взрослых пациентах и экспериментальных животных, что обусловлено сложностью клинико-экспериментальных исследований в педиатрии. Кроме того, неизученность проблемы связана и с тем, что болезнь развертывается на развивающемся легком, и сложно отграничить механизмы патологического ремоделирования от физиологических и репаративных реакций.
Сначала непосредственно аденовирусы, органические поллютанты внешней среды, токсические субстанции (чистый кислород, цитостатики) или косвенно (иммунные механизмы, свободные радикалы) поражают эпителий альвеол, базальную мембрану и эндотелий капилляров. В моделях на животных, используя в качестве инициирующего фактора блеомицин, продемонстрировано ведущее патогенетическое значение апоптоза альвеолярного эпителия. В интерстиций и просвет альвеол, богатые прокоагулянтами, пропотевает жидкая часть крови, образуются микротромбы, формирующие примитивный матрикс, содержащий фибронектин. Одновременно с жидкой частью крови в альвеолы и периальвеолярное пространство проникают клетки воспаления и иммунокомпетентные клетки, развивается альвеолит.
В зависимости от типа и стадии воспаления доминируют различные клетки: нейтрофилы (фиброзирующий альвеолит), Т-лимфоциты (саркоидоз) или эози-нофильные гранулоциты (хроническая эозинофильная пневмония). Происходит переключение иммунного ответа на Th2-клетки, они включаются в развитие гуморального ответа, помогая В-клеткам в переключении классов Ig и увеличивая синтез igg и ige. Th2-клетки способствуют депонированию компонентов матрик-са. Если процесс не удается оборвать, альвеолит переходит в фиброз. Формируется «сетчатое легкое», по другой формулировке - «сотовое легкое». Фиброз легкого развивается за счет активации фибробластов. В норме фибробласты окружают альвеолы и дистальные воздухоносные пути. Белки пропотевшей плазмы и растворимые медиаторы активируют фибробласты, они начинают мигрировать в матрикс, пролиферируют и активно синтезируют коллаген. Кроме того, фибробласты в большом количестве образуют такие протеазы, как урокиназа и коллагеназа, разрушающие матрикс, и ингибиторы тканевых металлопротеиназ. Синтез ИЛ-6, ИЛ-8, фактора роста кератиноцитов приводит к активации клеток воспаления, эндотелиоцитов и пневмоцитов типа II. Признаки воспаления обнаруживают при многих ИБЛ. Многие ИБЛ запускаются инфекцией или реакцией гиперчувствительности. В бронхоальвеолярной лаважной жидкости превалируют нейтрофилы и лимфоциты, присутствуют эозинофилы и мастоциты. При десквамативной интерстициальной пневмонии воздухоносные пути заполнены слущенным эпителием. В действительности эти клетки являются не чем иным, как активированными макрофагами. Клетки воспаления синтезируют ИЛ-1 и трансформирующий фактор роста β - сильные активаторы обусловленного фибробластами ремоделирования. В определенных пределах выраженность воспаления определяет степень ремоделирования и фиброза. В то же время такие критерии воспаления, как цитоз бронхоальвеолярной лаважной жидкости, сканирование с 67Ga, уровень циркулирующих в крови медиаторов воспаления, не коррелируют с активностью или прогнозом заболевания. Воспаление играет важную, но не центральную роль в ремоделировании и фиброзе. Банальная интерстициальная пневмония у взрослых течет без признаков воспаления. Пневмонит при реакции гиперчувствительности далеко не всегда переходит в фиброз. Эксперименты с трансгенными мышами показали, что ремоделирование и фиброз могут развиваться без воспаления. Большое значение в развитии ИБЛ имеют факторы ангиогенеза и миграция и пролиферация пневмоцитов типа II. Фиброз - цепь последовательных реакций разрушения и реструктуризации матрикса, реэпителизации, апоптоза фибробластов и клеток воспаления. Именно фиброз ответствен за летальные исходы при ИБЛ. Фиброз приводит к гипоксемии, она - к ремоделированию сосудов. Последнее ведет к формированию ЛС. Усиленный расход энергии, затрачиваемой на дыхание, усугубляет кахектический эффект медиаторов воспаления.
КЛИНИЧЕСКАЯ КАРТИНА
Большой срок от начала заболевания до его клинической манифестации, неспецифичность и стертость клинической картины приводят к тому, что диагноз ИБЛ основан на подозрении (на наличие ИБЛ) и исключении (дифференциальная диагностика с иными заболеваниями). Клиническая картина варьирует в зависимости от возраста. Респираторная симптоматика у детей часто становится основанием для ошибочного диагноза БА. Промедление с правильной диагностикой приводит к быстрому ремоделированию легких, и к специалисту попадают бессимптомные пациенты с существенными изменениями на рентгенограммах.
Ведущий клинический признак - одышка, обнаруживаемая на момент диагностики более чем у 75% больных, у детей младшего возраста - чаще. У детей грудного возраста ДН проявляется отказом от еды, обильным потоотделением во время еды и, наконец, появлением цианоза. У более старших детей снижается толерантность к физической нагрузке. Так же часто, как и одышка, возникает сухой непродуктивный кашель. Почти у половины детей прослушивают свистящие хрипы.
В результате постоянного недоедания и большого расхода энергии на неэффективное дыхание снижаются темпы роста ребенка, появляются признаки дистрофии. Дети школьного возраста могут жаловаться на боли в груди. В случаях инфекционного или иммунного генеза ИБЛ возможно повышение температуры тела. Кровохарканье - признак легочного васкулита или геморрагического синдрома.
При объективном обследовании ребенка регистрируют задержку физического развития, а у детей раннего и младшего возраста - и затруднения приема пищи (повышенная потливость, быстрая утомляемость). Аускультативная картина может быть не изменена, в других случаях прослушиваются сухие хрипы. Часто обнаруживают акцент II тона над легочной артерией, гипертрофию ПЖ и другие признаки ЛГ. У 80-95% детей устанавливают гипоксемию (sao2 <90%). На поздних стадиях появляется цианоз.
В обязательном порядке необходимо исключать наличие диффузных болезней соединительной ткани, системных васкулитов.
ДИАГНОСТИКА
Параклинические методы исследования используют как для исключения более частых состояний, протекающих с интерстициальными изменениями в легких, так и собственно для диагностики ИБЛ.
Лабораторная диагностика
Анемия и ретикулоцитоз развиваются при легочном геморрагическом синдроме, полицитемия - при хронической гипоксии. Эозинофилия свидетельствует о возможной паразитарной инвазии, реакции гиперчувствительности или эозинофильном синдроме.
Анализ мочи помогает выявить сопутствующий гломерулонефрит при легочно-ренальном синдроме.
Скрытую кровь в стуле обнаруживают при идиопатическом легочном гемосидерозе или воспалительных заболеваниях толстой кишки.
Для оценки выраженности воспаления необходимо определение скорости оседания эритроцитов (СОЭ), уровня С-реактивного белка (СРБ). Исключение первичных ИД строится на определении количества нейтрофилов, общей концентрации Ig и подкласса igg, комплемента и его фракций (СН50, С3, С4), антител к антигенам декретированных вакцин (от коклюша, столбняка, кори) и наличия или отсутствия кожной анергии.
Наряду с этим необходимо исключить возможность диффузных болезней соединительной ткани или аутоиммунной этиологии ИБЛ. Для этого определяют наличие ревматоидного фактора, антинуклеарных антител, антител к нативной ДНК, цитоплазме нейтрофилов.
Положительная реакция на сывороточный преципитин типична для пневмонита по типу реакции гиперчувствительности.
При подозрении на лимфоцитарную интерстициальную пневмонию, пневмоцистную пневмонию или диссеминированный гистоплазмоз необходимо исключить ВИЧ-инфекцию.
Для исключения саркоидоза необходимо определить концентрацию ангиотензин-превращающего фермента, содержание которого повышено при болезни Бенье-Бека-Шауманна.
Потовая проба и генный анализ позволяют отказаться от вероятного диагноза МВ.
При необходимости приходится исключать присутствие респираторных вирусов или выполнять серологические пробы на наличие грибковых антигенов.
Для интерстициальной пневмонии характерно повышение уровня ЛДГ, которую выделяют клетки воспаления. В свете этого уровень ЛДГ используют как критерий активности воспаления и при других болезнях легких.
Инструментальные методы
Радиологические исследования служат одними из определяющих для диагноза ИБЛ. В качестве первого шага необходимо УЗИ сердца. Следует добиться визуализации всех четырех легочных вен, так как нарушение венозного возврата может проявляться ДН и, по данным рентгеновских исследований, интерстициальной инфильтрацией. ЛГ, свойственную ИБЛ, регистрируют по расширению ствола легочной артерии, траектории движения ее клапана, градиенту давления, скорости и длительности фазы эжекции ПЖ, нарушению соотношения длительности фаз преэжекции и эжекции. Кроме того, возможны гипертрофия миокарда ПЖ и регургитация через правое атриовентрикулярное отверстие.
Результаты рентгеновских исследований не всегда однозначны. Рентгенограмма грудной клетки в прямой проекции может оказаться совершенно нормальной (до 10% больных) при наличии явных клинических признаков заболевания или выявить достаточно грубые изменения у бессимптомных больных. Однако в целом рентгеновская картина ИБЛ характеризуется такими признаками, как симптом «мутного стекла» («молочного стакана»), интерстициальная, нодулярная или ретикулонодулярная инфильтрация, фиброз и «ячеистое (сотовое) легкое» (рис. 1.1).
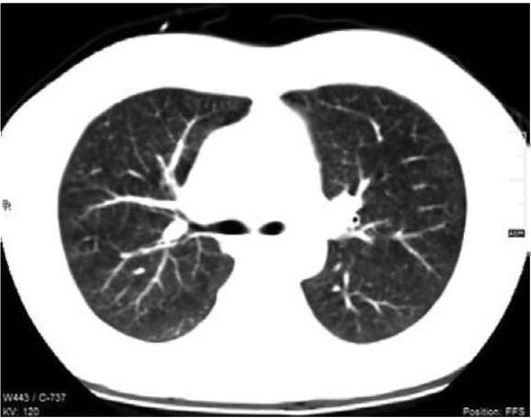
Рис. 1.1. На аксиальных сканах при компьютерной томографии отмечают утолщение интерстиция, общее снижение прозрачности легочной ткани - развитие интерстициальной пневмонии.
Симптом «мутного стекла» характеризует активный альвеолит, «ячеистое легкое» - конечный этап фиброза. В 30-50% случаев присутствует сочетание нескольких рентгеновских признаков. Обычно это нодулярная (альвеолярная) и ретикулонодулярная инфильтрация в сочетании с участками гипервентиляции.
КТ, особенно высокого разрешения, позволяет выявить изменения, свойственные ИБЛ, и их распространенность в легких. Особенно ценно, что методом КТ локализуют зоны для биопсии, хотя специфические КТ-признаки поражения легких при ИБЛ не всегда высокоинформативны для диагностики отдельных типов ИБЛ. Тем не менее симптом «мутного стекла» сопровождает инфильтративные ИБЛ (десквамативную интерстициальную пневмонию, лимфоцитарную интерстициальную пневмонию, пневмонит с реакцией гиперчувствительности). Очаги повышенной прозрачности с бронхоэктазами или без них свойственны облитерирующему бронхиту или бронхоцентрическому гранулематозу. Утолщение септ дает повод думать о лимфангиоматозе или капиллярном гемангиоматозе. Плотные очаги в легких встречаются при аспирации, облитерирующем бронхиолите с организующейся пневмонией или васкулитах. Тонкостенные гетерогенные кисты, чередующиеся с мелкими узелками, очень типичны для гистиоцитоза Лангерганса.
Недостатки КТ, в том числе и высокого разрешения, - сравнительно высокая доза излучения и необходимость активного участия пациента в исследовании (задержка дыхания). Последнее требование для маленьких детей оказывается невыполнимым. Все попытки создания алгоритмов быстрого обследования оказались неэффективными. Кроме того, еще неясна ценность КТ для динамического обследования детей с ИБЛ и оценки результатов лечения.
Сцинтиграфию проводится с 67Ga. Изотоп накапливается в очагах воспаления. Данное исследование целесообразно для определения очагов активного воспаления и динамического наблюдения. Однако при интерстициальном фиброзе взрослых результаты сцинтиграфии никак не коррелируют с активностью воспаления или ответом пациента на лечение.
Оксиметрия. На ранних этапах развития ИБЛ уровень sao2 в покое может быть в пределах нормы, но резко снижается во сне или при физической нагрузке. В последующем определяется снижение уровня оксигемоглобина, что отражает вентиляционно-перфузионные нарушения, развивающиеся вследствие ремоделирования дистальных воздухопроводящих путей. В большинстве случаев ИБЛ у детей выявляют на стадии гипоксемии. У взрослых уровень артериальной деса-турации коррелирует с фиброзом легкого, ЛГ и ожидаемой продолжительностью жизни. У детей определяющим предиктором плохого прогноза бывает ЛГ, значительно опережающая по своей информативности уровень десатурации. Как отражение ДН регистрируют респираторный алкалоз.
Функциональные пробы легких. У подростков и детей, чей возраст позволяет провести спирометрию и плетизмографию, снижены комплаенс респираторной системы, тотальная и ФЖЕЛ, объем формированного выдоха за 1-ю секунду (ОФВ1), а также индекс ОФВ1/ФЖЕЛ, что отражает рестриктивный характер патологии. Указанные показатели используют у детей для мониторинга эффективности терапии (рис. 1.2).
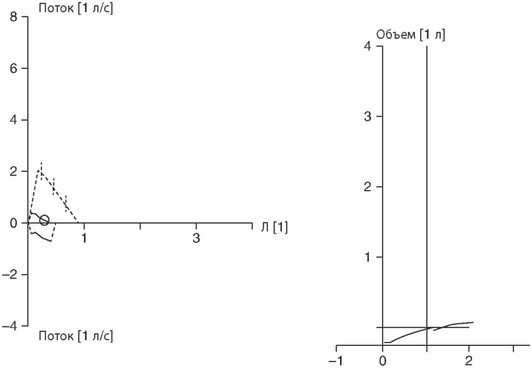
Рис. 1.2. Резкое уменьшение (кривая сплошной линией) объемно-скоростных показателей внешнего дыхания у ребенка с пневмофиброзом как исход интерстициального процесса.
Диффузионная способность, определяемая по окиси углерода (СО), снижена. При легочном геморрагическом синдроме показатель диффузионной способности может быть повышен из-за аффинности внесосудистого гемоглобина к СО.
Пробы с физической нагрузкой выявляют снижение сатурации оксигемоглобина даже при нормальных величинах в покое. Кроме того, пробы с физической нагрузкой целесообразно выполнять в динамике для контроля течения болезни.
Прочие исследования. Мониторирование ph пищевода целесообразно для исключения ГЭРБ, предрасполагающей к аспирации и воспалению.
На электрокардиограмме обнаруживают признаки ЛС, прежде всего - отклонение электрической оси сердца вправо и гипертрофию правых отделов сердца.
В случаях ЛГ с гемоптизом без наличия влажных хрипов в легких необходимо выполнить катетеризацию сердца, которая позволяет диагностировать венооклю-зивную болезнь легких.
Бронхоскопия с бронхоальвеолярным лаважем - важный этап диагностики ИБЛ, включая различные инфекционные состояния, альвеолярный протеиноз, аспирационный синдром. Лаважную жидкость необходимо направить для определения характера и количества клеток, исследования на грибы, бактерии (в том числе микобактерии), вирусы, цитологический анализ (в том числе с окраской гематоксилином для выявления перегруженных липидами макрофагов).
По результатам цитологического исследования возможно обнаружение клеток Лангерганса, указывающих на наличие гистиоцитоза. Исследование маркеров лимфоцитов в лаважной жидкости у взрослых дает противоречивые результаты, а у детей совершенно не стандартизовано. Отсутствие стандартизации методик анализа лаважной жидкости у детей, недостаток доказательных исследований по цитозу жидкости, вариабельность результатов в зависимости от периода течения болезни, низкая корреляция с гистологическими находками - серьезные проблемы, затрудняющие применение бронхоальвеолярного лаважа в педиатрической пульмонологии. В то же время принято считать, что бронхоальвеолярный лаваж должен предшествовать биопсии легкого.
Гистологические исследования биоптата легкого - единственная возможность диагностики и дифференциальной диагностики тех форм ИБЛ, которые невозможно диагностировать неинвазивными методиками. Большинство классификаций ИБЛ, особенно касающихся ИБЛ неизвестной этиологии, основаны на патогистологических находках. Как в педиатрической, так и в терапевтической литературе обсуждают целесообразность выполнения биопсии легкого всем пациентам с ИБЛ. При этом указывают, что после биопсии частота уточненных диагнозов увеличивается несущественно. Точно так же мало сказываются на верификации диагноза количество биоптатов и метод их получения (открытый или торакоскопический). Открытая биопсия позволяет получить оптимальный объем тканей из наиболее измененного участка легкого. Место взятия биоптата предварительно уточняют с помощью КТ высокого разрешения. Торакоскопическая биопсия по сравнению с открытой сокращает длительность оперативного вмешательства и пребывания в стационаре, не сказываясь при этом на качестве диагностики. Решение о выборе открытой или торакоскопической биопсии следует принимать коллегиально.
Трансбронхиальную биопсию применяют в основном у подростков и взрослых. Малый диаметр педиатрического фибробронхоскопа не всегда позволяет провести сквозь него биопсийные щипцы. Объем ткани, полученной при трансбронхиальной биопсии, меньше, чем при открытой или торакоскопической, поэтому приходится брать большее количество биоптатов.
Вне зависимости от метода забора биоптата образцы тканей исследуют на наличие бактерий, грибов, направляют на гистологическое исследование (включая и специальные окраски), электронную микроскопию, иммунофлюоресцентный анализ. Гистологическое исследование с помощью рутинной окраски гематоксилином и эозином - стандарт для диагностики и классификации ИБЛ, оно способно выявить возможную причину болезни или иное системное заболевание. Однако основные трудности и проблемы возникают не при заборе и окраске материала, а при трактовке результатов. Многочисленные неудачи возникают из-за различных классификаций, несогласованности номенклатуры, значительных различий гистологической картины у детей и взрослых.
ОПРЕДЕЛЕНИЕ СТЕПЕНИ ТЯЖЕСТИ И ПРОГНОЗ
Общепринятых критериев для оценки степени тяжести ИБЛ у детей нет. Возможны градации по следующим пунктам:
1) бессимптомное течение;
2) наличие симптомов с нормальной sao2;
3) наличие симптомов с десатурацией во сне или при физической нагрузке;
4) десатурация в покое;
5) ЛГ.
Пункт 5 данной шкалы указывает на крайне плохой прогноз: вероятность летального исхода в ближайшие 60 мес составляет 62%. При соответствии пациента пункту 2 вероятность выживания составляет 76%. Каждый следующий пункт означает повышение риска смерти на 140% по сравнению с предыдущим.
Прогноз отягощают начало ИБЛ в возрасте до 1 года (риск смерти более 90%; обычно это десквамативная интерстициальная пневмония), наличие в семье интерстициального легочного фиброза, гистологические признаки десквамативной интерстициальной пневмонии или легочного васкулита.
ЧАСТНЫЕ ПРОБЛЕМЫ
Интерстициальная пневмония
Синонимы термина «интерстициальная пневмония» - криптогенный фиброзирующий альвеолит, идиопатический фиброз легких. По гистологическим находкам, цитологическим характеристикам бронхоальвеолярной лаважной жидкости и ответу на глюкокортикоидную терапию выделяют две формы этого состояния:
• банальную интерстициальную пневмонию;
• десквамативную интерстициальную пневмонию.
Эти две формы различаются по превалированию фибротических процессов и десквамативным или клеточным реакциям. Однако нельзя исключить, что обсуждаемые формы представляют собой этапы одного и того же процесса. Десквамативный или клеточный тип отражает острую раннюю стадию, а так называемая обычная (банальная) интерстициальная пневмония соответствует хроническому течению или поздней стадии интерстициальной пневмонии с преобладанием склеротических процессов или фиброзирующему альвеолиту.
Причина интерстициальной пневмонии обычно остается нерасшифрованной. Известно, что 30-33% всех больных с интерстициальной пневмонией или фиброзирующим альвеолитом страдают болезнями соединительной ткани с аутоиммунным компонентом и васкулитами. Гистологически у всех больных интерстициальной пневмонией обнаруживают интерстициальные инфильтраты, состоящие из плазматических клеток, гистиоцитов, эозинофилов и лимфоцитов, гиперплазию пневмоцитов II типа; в альвеолах - нейтрофилы, альвеолярные макрофаги и мононуклеары. При иммуногистологии отмечают отложение Ig и компонентов комплемента. В промывных бронхоальвеолярных водах превалируют нейтрофилы. Микроскопическая архитектоника легких изменена мало, что отличает десквамативную интерстициальную пневмонию от фиброза легких и «банальной интерстициальной пневмонии». Хроническое течение проявляется выходом фибробластов в альвеолярный экссудат, формированием коллагеновых волокон, образованием «сотового (ячеистого) легкого». Наличие скоплений пролиферирующих фибробластов свидетельствует о плохом прогнозе.
«Сотовое легкое» характеризуется образованием кистовидных одноили многокамерных просветлений диаметром несколько миллиметров на фоне уплотненных легких. В сущности, «сотовое легкое» по этому определению может быть только вторичным как исход пневмосклероза и интерстициального воспаления при интерстициальных пневмониях и пневмопатиях, хроническом облитерирующем бронхите, МВ. Однако нередко, особенно у взрослых, применяя клинико-рентгенологические исследования, «сотовое легкое» невозможно дифференцировать от первичного множественного кистоза легких. Тем более что врожденные мелкие кисты могут протекать с формированием фиброза легких.
В клинической картине интерстициальной пневмонии на первое место выходит одышка (95%), сначала при нагрузке. Дыхание поверхностное и быстрое. Одышка вскоре появляется и в покое. Глубокий вдох сопровождается иногда остановкой дыхания. На втором месте по выраженности признака и частоте стоит непродуктивный кашель. Иногда он сопровождается периодическим повышением температуры тела. Появляются общая разбитость, артралгии, снижение массы тела. Перкуторно
Выявляют высокое стояние границ легких, что служит достоверным признаком пневмосклероза (фиброза) - «синдром малого легкого». При аускультации дыхательные шумы прослушиваются хорошо, на высоте глубокого вдоха слышны крепитация и нежные мелкопузырчатые хрипы. Цианоз, деформация пальцев по типу барабанных палочек, признаки перегрузки правых отделов сердца и, наконец, ЛС с правожелудочковой недостаточностью - этапы развития клинической картины пневмофиброза. В острой стадии криптогенного фиброзирующего альвеолита или идиопатического фиброза легких умеренно повышается СОЭ, возможен лейкоцитоз. У половины пациентов с фиброзирующим альвеолитом обнаруживают анти-нуклеарные антитела, у 12% - антимитохондриальные, у 8% - антитела к гладкой мускулатуре. Наряду с этим у каждого третьего пациента присутствует ревматоидный фактор. Обнаруживают гаммаглобулинемию, иногда криоглобулины.
При функциональных исследованиях на ранних этапах выявляют снижение диффузионной способности легких, в покое газы крови не изменены. При нагрузке парциальное давление углекислого газа снижается, что служит чувствительным показателем интерстициального процесса. Позднее снижаются жизненная и секундная емкости легких (индекс Тифно остается в пределах нормы), возникают рестрикция, гипокапния и гипоксемия. При рентгеновских исследованиях в острую фазу болезни отмечают только общую замутненность легочного фона (симптом «молочного стакана») и сетчатые инфильтраты, распространяющиеся дельтовидно диффузно по всем легким от ворот к базальным отделам. Реберно-диафрагмальный угол остается неизмененным. В последующем появляются диффузная сетчато-очаговая инфильтрация и «тяжистость» легочного рисунка, корни широкие (ЛГ), верхушки легких длительное время остаются свободными. Выявляют сотовость картины легкого. Диафрагма стоит высоко. На поздних стадиях за счет неравномерного склероза нарушается симметричность, возможно перетягивание трахеи в сторону от срединной линии.
Диагностика интерстициальной пневмонии основана и на данных клинико-рентгенологического исследования, но в основном - на цитологическом анализе промывных вод бронхов и результатах биопсии. Постановка диагноза вызывает большие трудности, когда острый период остался в прошлом, а клиническую картину определяет пневмофиброз. Иногда невозможно определить первичное состояние, приведшее к пневмосклерозу, поэтому об этиологии 45-55% всех его случаев практически неизвестно.
При дифференциальной диагностике интерстициальной пневмонии на первом плане стоят вирусные пневмонии, туберкулез, грибковые инфекции и пневмоцистная пневмония. Диагноз инфекционного поражения легких подтверждают исследованиями крови, мокроты, бронхиального секрета, бактериологически, вирусологически, пункционной биопсией легкого. Общее обследование больного и экстрапульмональные симптомы помогают дифференцировать интерстициальную пневмонию при так называемых коллагенозах от криптогенных вариантов. В ранних стадиях течения саркоидоза дифференциальная диагностика не представляет сложностей, но, когда саркоидоз приводит к пневмофиброзу, иногда она представляется невозможной. Из других заболеваний необходимо учитывать ГВ, идиопатический гемосидероз легких, лимфангиомиоматоз, альвеолярный микро-литиаз. Наряду с иммунологическими исследованиями в ряде случаев приходится прибегать к биопсии легкого. Необходимо помнить о возможности диффузного роста злокачественного образования (например, альвеолярно-клеточный рак, карциноматозный лимфангиоз, лейкозы и лимфомы). Большое значение имеет профессиональный анамнез. Вдыхание органических и неорганических веществ приводит к аллергическому альвеолиту. Так, известны «легкое фермера», или сельскохозяйственного рабочего (J67.0), силикоз (J62), асбестоз (J61), фиброз легкого после облучения и др. Количество медикаментов, приводящих к пневмофиброзу, велико. Это вдыхание высокопроцентных кислородных смесей, прием цитостатиков (действующих в ряде случаев не непосредственно, а позволяющих активизироваться оппортунистической инфекции), нитрофурантоина (Фурадонина♠), салазопиридазинаρ, ганглиоблокаторов, дифенилгидантоинов, амиодарона, препаратов золота. Если повреждающий эффект кислорода и цитостатиков дозозависим, то прием фурадониновых препаратов запускает иммунный механизм.
Десквамативная интерстициальная пневмония
Десквамативная интерстициальная пневмония - хроническое воспаление легких с инфильтрацией мононуклеарами. Поражает обычно курильщиков в возрасте 30-40 лет. Однако существует мнение, что в этих случаях первые признаки заболевания появляются в детстве, даже при рождении, а манифестная клиническая картина провоцируется курением и проявляется значительно позже.
У взрослых десквамативная интерстициальная пневмония хорошо отвечает на лечение преднизолоном. Прогноз данного заболевания у взрослых хороший. Однако у детей заболевание обнаруживают уже на 1-м году жизни. Считают, что смертность от него выше, чем при других ИБЛ.
В противоположность банальной интерстициальной пневмонии процесс при десквамативной интерстициальной пневмонии более диффузный. Инфильтрация интерстиция эозинофилами, лимфоцитами, плазматическими клетками выражена значительно меньше. Альвеолы выстланы гиперплазированными пневмоцитами II типа. Наиболее важное отличие десквамативной интерстициальной пневмонии от банальной интерстициальной - множество макрофагов в дистальных воздухоносных путях. Макрофаги инициируют и поддерживают процесс за счет цитоки-нов - ИЛ-1, ИЛ-6, ИЛ-8, ФНО, моноцитарного хемотаксического пептида.
Клинически больных беспокоят одышка и сухой кашель. Рентгенологическая картина у 10-20% больных остается нормальной, а при КТ высокого разрешения обнаруживают субплевральные очаги уплотнения и типичный феномен «мутного стекла».
Синдром Хаммана-Рича
Синдром Хаммана-Рича - острая интерстициальная пневмония с быстро развивающимся интерстициальным фиброзом легких. Пытаются проводить аналогии с ретроперитонеальным фиброзом Ормонда и системной склеродермией. Обычно заболевание обнаруживают у ранее здоровых людей. Средний возраст заболевших - 50 лет. У детей встречается очень редко. За свою 30-летнюю практику мы (Делягин В.М.) наблюдали данный синдром всего у 4 детей. Развивается остро, появляются и быстро прогрессируют одышка, цианоз, гемоптоэ. Физикальные данные в легких скудные. Рентгенологически обнаруживают сетчатость рисунка, милиарные и более крупные диффузно расположенные очаги. Поскольку биопсию проводят значительно позже дебюта болезни, острую экссудативную фазу практически никогда не улавливают. Фаза организации (фиброзирования) выражается утолщением межальвеолярных перегородок за счет отека и инфильтрации клетками воспаления, пролиферации фибробластов, гиалиновых мембран. В мелких артериях появляются тромбы. За счет развития соединительной ткани легкие настолько тяжелые, что тонут в воде. Большинство пациентов умирают в ближайшие полгода после манифестации клинической картины.
Облитерирующий бронхиолит
Облитерирующий бронхиолит с организующейся интерстициальной пневмонией описан всего 25 лет назад. В определенной мере причисление его к ИБЛ условно. Первоначальный процесс развивается в просвете дистальных воздухопроводящих путей. Клинически и рентгенологически отличить это заболевание от ИБЛ крайне сложно. Гистологически обнаруживают участки гранулематозных тканей в воздухопроводящих путях и альвеолярных ходах с воспалением (первоначально - макрофагальным) в окружающих альвеолах. Миофибробласты в коллагеновой строме прорастают в прилежащие воздухоносные пути. Паренхима легкого страдает мало (рис. 1.3).
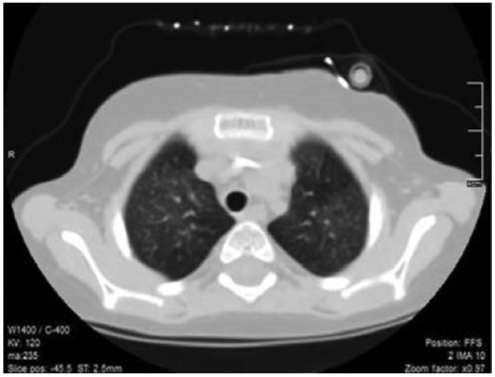
Рис. 1.3. Компьютерная томограмма легких при облитерирующем бронхите. На аксиальных сканах (режим «легочное окно») видна мозаичная пневматизация легких с четко очерченными зонами гипо- и гиперпневматизации.
Облитерирующий бронхиолит с организующейся пневмонией развивается после вирусной инфекции, его связывают с онкологическими заболеваниями. Хорошо отвечает на глюкокортикоидную терапию. Основные признаки - кашель, мокрота, одышка, деформация пальцев по типу барабанных палочек. Обструктивный компонент, несмотря на поражение бронхиол, выражен мало. Преобладает рестрикция со сниженной диффузионной способностью легких. Процесс хронический, острое течение нехарактерно. Рентгенологически наряду с признаками интерстициальной пневмонии определяют преимущественно в нижних долях двусторонние пятнистые инфильтраты со склонностью к слиянию, центролобулярные узелки диаметром 5-10 мм, окружающие мелкие сосуды (рис. 1.4).
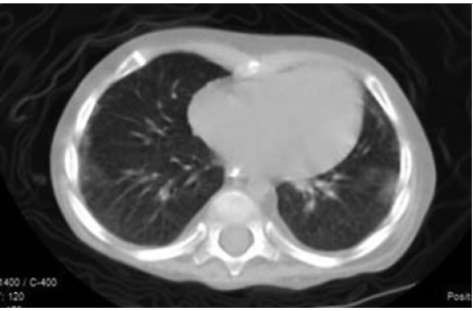
Рис. 1.4. Компьютерная томограмма легких при облитерирующем бронхите с организующейся пневмонией. Полиморфные мультифокальные легочные изменения. На аксиальных компьютерно-томографических сканах в режиме «легочное окно» видны диффузное интерстициальное поражение, снижение пневматизации легочной ткани, мелкосетчатый рисунок интерстиция, распространенные, нечетко очерченные зоны воспалительной инфильтрации «матового стекла» в задних и заднебазальных отделах обоих легких, небольшие очаги пневмофиброза в S3 верхней доле левого легкого субплеврально, очаг перибронховаскулярной воспалительной инфильтрации в центральных отделах S2 слева. Внутридольковые ателектазы субплеврально в задних отделах S2 верхней доли правого легкого, утолщение костальной плевры задних отделов легких
Лимфоцитарная интерстициальная пневмония
Лимфоцитарная интерстициальная пневмония - относительно благоприятная пролиферация лимфоцитов и плазмоцитов в интерстиции и альвеолярном пространстве. Развивается преимущественно у детей. У 3/4 больных зарегистрирована гипогаммаглобулинемия, у остальных выявляют синдром Шегрена, ревматоидный артрит, хронический активный гепатит, тиреоидит Хасимото. Встречается у 30-75% детей со спидом, но только у 3% взрослых, больных ВИЧ-инфекцией. Если не ассоциируется с ВИЧ-инфекцией, то чаще встречается у женщин.
В интерстиции обнаруживают инфильтраты из лимфоцитов, плазматических клеток, центры размножения, многоядерные гигантские клетки без казеозных гранулем. Инфильтраты составлены из поликлональных Т- и В-лимфоцитов, что отличает инфильтраты от моноклональных лимфом. Инфильтраты формируются вокруг сосудов и бронхов, хотя чаще - в межальвеолярных перегородках.
Клинически заболевание дебютирует с кашля и одышки. Возможны повышение температуры тела, снижение массы тела, артралгии, плеврит. Для детей характерны лимфаденопатия, гепатоспленомегалия, увеличение околоушных слюнных желез, сухие свистящие хрипы (для взрослых типичны влажные хрипы). Симптоматика во многом зависит от основного заболевания.
Для детей типично увеличение активности ЛДГ, но в половине случаев - на фоне присоединения пневмоцистной пневмонии. Для взрослых концентрация ЛДГ неинформативна. ДНК вируса Эпстайна-Барр, который многие авторы рассматривали как причину лимфоцитарной интерстициальной пневмонии, в биоптатах легкого обнаруживают только в период первичного заболевания или его обострения. У взрослых титры антител к вирусу повышены значительно чаще.
Рентгенологически (рис. 1.5) на фоне общей замутненности легочного фона (симптом «молочного стекла») выявляют плохо ограниченные центролобулярные (100%) и субплевральные (90%) узелки, усиление бронхососудистого рисунка (85%), утолщение междолевых перегородок, кистозные полости в легких, увеличение лимфатических узлов. Реже отмечают эмфизему, бронхоэктазы, «сотовое легкое», утолщение плевры. Диффузионная способность снижена. Возможна тяжелая гипоксемия. В бронхоальвеолярной лаважной жидкости находят большое количество лимфоцитов.
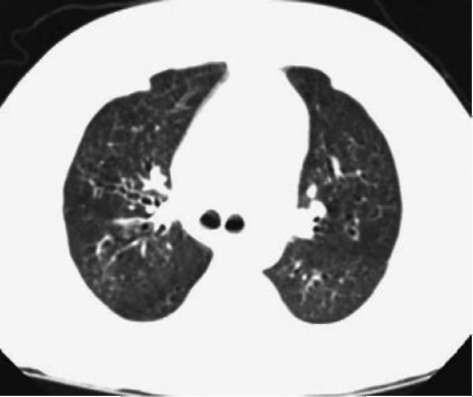

Рис. 1.5. Компьютерная томограмма легких при пневмофиброзе. На аксиальных компьютерно-томографических сканах в режиме «легочное окно» видна неравномерная пневматизация легочной ткани (симптом «лоскутного одеяла») с множественными участками повышенной и пониженной плотности, преимущественно в верхних отделах легких.
Бронхоэктазы обоих легких
Возможные исходы лимфоцитарной интерстициальной пневмонии:
• спонтанное разрешение;
• разрешение после назначения глюкокортикоидов и/или иммуносупрессантов;
• трансформация в лимфому;
• пневмофиброз.
Лечение первичных заболеваний паренхимы легких
Питание. В специальной диете нет необходимости. Однако, как и при каждом хроническом заболевании, нужно достаточное калоражное обеспечение, так как сниженный комплаенс легких с усиленной работой дыхательной мускулатуры требует повышенного притока энергии. Дети старшего возраста обычно способны есть самостоятельно. Детям раннего возраста может понадобиться введение транс-пилорического зонда.
Физическая активность лимитируется степенью одышки. Для объективной оценки работоспособности ребенка необходимо определить уровень sao2 в период пробы с дозированной физической нагрузкой.
Принципы ведения пациента
• Постараться снять стресс и напряжение, испытываемые ребенком и его родителями при посещении врача, новых назначениях, консультациях, изменениях режима и питания.
• Научить родителей и ребенка оценивать свое состояние, обращать внимание на возможные неблагоприятные изменения состояния, осложнения, побочные действия препаратов.
• Продолжить вакцинацию (особенно против гриппа и пневмококковой инфекции). Вакцинацию детей с ИД проводить по специальным схемам.
• Категорически запрещено активное и пассивное курение.
• При наличии пневмонии с реакцией гиперчувствительности необходимо исключить возможный контакт с преципитинами (например, пухом и пером птицы).
С момента установления диагноза лечащий врач должен работать в контакте с трансплантологом, так как ошибка в определении сроков трансплантации ведет к гибели больного. При необходимости биопсии легкого ее нужно предварительно согласовать с патогистологом, знакомым с проблемой ИБЛ у детей. Все новые назначения, особенно цитостатиков и глюкокортикоидов, необходимо начинать в условиях стационара. В условиях амбулаторных визитов следует оценивать физический и психоэмоциональный статус пациента, результаты физикального обследования, sao2, наличие возможных осложнений и побочных действий препаратов, функциональные пробы легких, данные эхокг (вероятность ЛГ). Суперинфекция может быть угрожающим жизни состоянием у ребенка, получающего иммуносупрессивную терапию. Токсический эффект препаратов существенно сказывается на показателях смертности.
Наиболее типичные ошибки - поздняя диагностика сопутствующих состояний, поздняя диагностика ЛС, нераспознанные токсические эффекты терапии.
Причинами смерти чаще всего бывают ДН и ЛС с правожелудочковой недостаточностью. Прогноз отягощают начало ИБЛ в возрасте до 1 года (риск смерти - 90%, обычно это десквамативная интерстициальная пневмония), наличие в семье интерстициального легочного фиброза, гистологические признаки десквамативной интерстициальной пневмонии или легочного васкулита.
Медикаментозная терапия. Лечение детей с ИБЛ отличается от такового у взрослых. Индивидуализированное лечение невозможно из-за малых знаний и неизвестности этиологии и патогенеза. Совершенствование терапии может быть достигнуто только по результатам многоцентровых исследований. Единой схемы (протокола) медикаментозной терапии нет. Предложено много вариантов лекарственного лечения детей с ИБЛ, но ни один из них не прошел проверку в условиях рандомизированных контролируемых исследований.
Если ИБЛ вторична по отношению к какому-либо процессу, необходимо лечение первичного состояния.
В случае признаков гиперреактивности бронхов возможно назначение бронходилататоров и/или ИГК, но эти препараты не сказываются на течении ИБЛ. Оксигенотерапия, особенно длительная или во время сна, может снизить риск ЛГ и формирования ЛС.
В лечении ИБЛ используют многие препараты. В конце 1990-х годов интенсивно прорабатывали возможность лечения ИБЛ хлорохином и гидроксихлорохином. Препараты способны ингибировать хемотаксис эозинофилов, движение нейтрофилов, угнетать комплементзависимую реакцию антиген-антитело, снижать секрецию фноα макрофагами и тем самым уменьшать презентацию антигенов. Однако результаты клинических исследований противоречивы.
Применяют антиоксиданты, ингибиторы синтеза коллагена (пеницилламин), антифибротические агенты (колхицин), стероиды, цитотоксические агенты и иммуносупрессанты, ингибиторы цитокинов.
Известны сообщения о применении каптоприла (ингибитора ангиотензин-превращающего фермента) у взрослых. Определенного мнения о причинах положительного эффекта терапии этим препаратом нет. Высказывают версию о благоприятном действии свободных тиоловых групп, содержащихся в препарате, и об антиапоптозном действии каптоприла.
Шире всего используют глюкокортикоиды, азатиоприн, метотрексат, циклофосфамид. Следует отметить, что указанные препараты сами по себе способны вызвать медикаментозно индуцированные поражения легких.
Глюкокортикоиды. Преднизолон и метилпреднизолон (Солу-Медрол*) подавляют миграцию полиморфноядерных лейкоцитов, снижают экссудацию, оказывают разнообразные метаболические эффекты.
Преднизолон назначают в дозе 2-3 мг/кг в сутки (но не более 60-80 мг/сут) в течение 8-12 нед с дальнейшим постепенным снижением под контролем клинической картины и функциональных легочных проб. Рецидив болезни требует возврата к максимальной дозе. Метилпреднизолон (Солу-Медрол*) назначают по принципу пульс-терапии - 10-30 мг/кг в сутки внутривенно в течение 3 дней. Считают, что пульс-терапия по сравнению с длительным приемом преднизолона внутрь способна улучшить показатели выживаемости и имеет меньше побочных действий.
Противопоказание для лечения глюкокортикоидами - системные инфекции.
Клиренс глюкокортикоидов повышают барбитураты, фенитоин, рифампицин. Клиренс глюкокортикоидов понижают эстрогены, кетоконазол и олеандомицин. Глюкокортикоиды повышают клиренс салицилатов, изменяют ответ на вакцины и анатоксины, вступают в конкурентное взаимодействие с дигоксином и могут вызвать дигиталисную интоксикацию, вторичную по отношению к гипокалиемии. При назначении детям иммуносупрессивных доз глюкокортикоидов противопоказано введение живых и аттенуированных вакцин.
Выраженные побочные реакции связаны прежде всего с длительным приемом глюкокортикоидов. Это нарушения водно-электролитного баланса, артериальная гипертензия, остеопороз, стероидная миопатия, желудочно-кишечные кровотечения, гиперкоагуляция, неврологические нарушения, катаракты, подавление активности коры надпочечников и замедление роста у детей. Резко возрастает риск диссеминации инфекции (особенно ветряной оспы, кори), нивелирования симптомов некоторых других серьезных инфекционных заболеваний. Резкая отмена глюкокортикоидов способна привести к адреналовому кризу.
Азатиоприн. Антагонист обмена пуринов, ингибирует синтез ДНК, РНК, белков, снижает пролиферацию иммунокомпетентных клеток. Назначают первоначально в дозе 1 мг/кг в сутки в течение 6-8 нед. Затем на протяжении 4 нед дозу повышают на 0,5 мг/кг в сутки до достижения клинического эффекта или до дозы 2,5 мг/кг в сутки. Противопоказания - повышенная чувствительность к препарату и/или низкий уровень сывороточной тиопуринметилтрансферазы. Азатиоприн снижает эффект антикоагулянтов, циклоспорина и нейроблокаторов. Азатиоприн ингибируется аллопуринолом, при этом реально действующая доза азатиоприна снижается до 67-75% получаемой пациентом. Одновременное назначение сульфаниламидов пролонгированного действия или блокаторов ангитензин-превращающего фермента может привести к резко выраженной лейкопении. Основные побочные действия - гематотоксичность (лейкопения) и изменения со стороны желудочно-кишечного тракта (тошнота, рвота, гепатотоксичность). Необходима максимальная осторожность при назначении препарата детям с поражениями почек и печени. Для раннего предупреждения токсических эффектов необходимо мониторирование концентрации азатиоприна в крови в 1-й месяц лечения еженедельно, во 2-й и 3-й месяцы - 1 раз в 2 нед, в 4-й месяц и далее - 1 раз в месяц.
Метотрексат. Антиметаболит фолиевой кислоты, подавляет S-фазу митоза, ингибирует синтез ДНК, РНК, белков. Дозы, специфичные для лечения ИБЛ, не разработаны. Рекомендована дозировка, принятая в ревматологии: 10 мг/м2 1 раз в неделю, но не выше 15 мг/нед. Противопоказания - почечная или печеночная недостаточность, выраженная анемия, синдромы ИД. Токсичность метотрексата повышается при назначении салицилатов или нестероидных противовоспалительных средств (НПВС) (снижение тубулярной экскреции), фенитоина, сульфаниламидов (конкурентное вытеснение метотрексата из белковых соединений), пенициллинов (снижение почечного клиренса), ретиноидов (повышение гепатотоксичности). Токсичность метотрексата повышается в условиях дефицита фолиевой кислоты. Тетрациклин и хлорамфеникол (Левомицетин*) снижают абсорбцию метотрексата. Для уменьшения вероятности побочных реакций назначают фолиевую кислоту в дозе 1 мг/сут. Из токсических реакций известны лейкопения, мукозит, тошнота, рвота, оппортунистическая инфекция, нарушение функций печени и ее фиброз. В высоких дозах может вызвать пневмофиброз. При почечной недостаточности, асците или выпоте в плевральную полость необходимо снизить дозу метотрексата.
Циклофосфамид. Механизм действия связан с повреждением ДНК. Назначают в дозе 5-10 мг/кг внутривенно 1 раз в 2-3 нед, не превышая общей дозы 5001600 мг. Противопоказания - гипоплазия костного мозга, лейкопения, тромбоцитопения, анемия, активно текущий инфекционный процесс. Токсичность циклофосфамида повышается при одновременном назначении хлорамфеникола (Левомицетина*), замедляющего его метаболизм. Тиазиды при одновременном назначении с циклофосфамидом, блокируя холинэстеразу, способны усугублять лейкопению и угнетать нервно-мышечную передачу. Из осложнений известны угнетение гемопоэза, алопеция, геморрагический цистит, нарушения фертильности.
Пеницилламин (Купренил*). Механизм действия достоверно неизвестен. Назначают терапию в дозе 3 мг/кг в сутки в течение 3 мес. Суточная доза не должна превышать 250 мг. Затем дозу повышают до 6 мг/кг в сутки, но чтобы суточная доза не превышала 500 мг. Противопоказания - гиперчувствительность, почечная недостаточность, апластическая анемия в анамнезе, хроническая свинцовая интоксикация. Пеницилламин повышает эффект действия иммуносупрессантов и антималярийных препаратов, понижает действие дигоксина. Эффект пеницилламина снижается при одновременном назначении препаратов железа, цинка, золота, антацидов. Из осложнений терапии возможны перекрестная реакция гиперчувствительности с пенициллинами, гематологические и почечные реакции, дефицит железа, синдром Гудпасчера (СГ), облитерирующий бронхиолит, миастенический синдром, волчаночноподобный синдром. С целью раннего выявления возможной токсичности препарата показано определение его концентрации в крови 1 раз в 2 нед в первые 6 мес терапии и 1 раз в месяц позже. Для снижения риска осложнений необходим постоянный прием пиридоксина в дозе 25 мг/сут.
Источник: Детская пульмонология : национальное руководство / под ред. Б. М. Блохина. - Москва : ГЭОТАР-Медиа, 2021.
17.12.2020 | 23:20:46