COVID-19. Лечение коронавирусной инфекции. Акушерская тактика при коронавирусе, ведение новорожденных при COVID-19. Версия 9 от 26.10.2020г.
Раздел: Статьи
/
Общая врачебная практика.
/
Инфекционные болезни.
/
COVID-19. Лечение коронавирусной инфекции. Акушерская тактика при коронавирусе, ведение новорожденных при COVID-19. Версия 9 от 26.10.2020г.
Содержание
Введение
Этиотропное лечение
Клиническое использование плазмы антиковидной, патогенредуцированной
Этиотропное лечение беременных, рожениц и родильниц
Патогенетическое лечение коронавирусной инфекции
Патогенетическое лечение у беременных, рожениц и родильниц
Симптоматическое лечение коронавирусной инфекции
Симптоматическое лечение у беременных, рожениц и родильниц
Особенности ведения пациентов пожилого и старческого возраста
Антибактериальная терапия при осложненных формах инфекций
Акушерская тактика при COVID-19
Тактика ведения новорожденных в условиях пандемии COVID-19
Ведение потенциально инфицированных COVID-19 новорожденных в родильном зале
Введение
Основным подходом к терапии COVID-19 должно быть упреждающее назначение лечения до развития полного симптомокомплекса жизнеугрожающих состояний, а именно пневмонии, ОРДС, сепсиса.
Лечение COVID-19 в соответствии с протоколами настоящих рекомендаций проводится в подтвержденных и вероятных случаях заболевания.
В рамках оказания медицинской помощи необходим мониторинг состояния пациента для выявления признаков ухудшения его клинического состояния. Пациенты, инфицированные SARS-CoV-2, должны получать поддерживающую патогенетическую и симптоматическую терапию.
Лечение сопутствующих заболеваний и осложнений осуществляется в соответствии с клиническими рекомендациями, стандартами медицинской помощи по данным заболеваниям.
В настоящее время следует выделить несколько препаратов, которые могут быть использованы при лечении COVID-19. К ним относятся препараты фавипиравир, ремдесивир, умифеновир, гидроксихлорохин, азитромицин (в сочетании с гидроксихлорохином), интерферон-альфа.
Имеющиеся на сегодня сведения о результатах терапии всеми препаратами не позволяют сделать однозначный вывод об их эффективности или неэффективности, в связи с чем их применение допустимо по решению врачебной комиссии в установленном порядке, в случае если потенциальная польза для пациента превысит риск их применения.
Препарат фавипиравир – синтетический противовирусный препарат, селективный ингибитор РНК-полимеразы, активный в отношении РНК-содержащих вирусов. В ряде исследований было продемонстрировано, что фавипиравир эффективно ингибирует SARS-CoV-2 в культуре клеток. В январе 2020 г. в Китае было проведено открытое нерандомизированное исследование фавипиравира при лечении COVID-19 в сравнении с комбинацией лопинавир+ритонавир. В группе фавипиравира медиана времени до элиминации вируса составила 4 дня и была значительно меньше, чем в группе сравнения (11 дней). При этом к десятому дню элиминация вируса была зарегистрирована у 80% пациентов, получавших фавипиравир. Улучшение по данным КТ ОГК через 14 дней после окончания исследуемой терапии зафиксировано у 91,4% пациентов в группе фавипиравира и только у 62,2% пациентов в контрольной группе. Нежелательные реакции в группе фавипиравира наблюдались в 5 раз реже, чем в группе сравнения.
В Российской Федерации проведено масштабное клиническое исследование по оценке эффективности и безопасности препарата фавипиравир с участием 168 пациентов с легким и среднетяжелым течением COVID-19 (в соотношении амбулаторных и стационарных пациентов 4:1). Частота достижения клинического улучшения на 7-й день терапии в группе пациентов, получавших фавипиравир, была практически в 1,5 раза больше, чем в группе сравнения. Доля пациентов с элиминацией вируса в дни 3-й и 5-й дни терапии была выше в группе лечения фавипиравиром, что свидетельствовало о более раннем наступлении элиминации при применении препарата. В когорте стационарных пациентов, получавших фавипиравир, к 28-му дню терапии была выявлена клинически значимая разница по числу разрешившихся случаев по данным КТ ОГК.
Полученные данные позволяют разрешить применение препарата не только в стационаре, но и в амбулаторных условиях.
Режимы дозирования фавипиравира приведены в приложении 1.


Другим препаратом, обладающим противовирусной активностью в отношении SARS-CoV-2, является ремдесивир. Его активный метаболит выступает в качестве аналога аденозинтрифосфата (АТФ) и конкурирует с природным АТФ-субстратом за включение в формирующиеся РНК-цепи с помощью РНК-зависимой РНК-полимеразы вируса SARS-CoV-2, что приводит к задержанному обрыву цепи во время репликации вирусной РНК. В одном из масштабных исследований, включавшем 1063 пациента, было показано, что у пациентов, получавших 10-дневный курс лечения ремдесивиром, время выздоровления было короче на 4 дня в сравнении с группой, получавшей плацебо (11 и 15 дней соответственно). Достоверной разницы в частоте смертности в описанных группах получено не было.
Применение препарата возможно только в медицинской организации, оказывающей медицинскую помощь в стационарных условиях. До этого необходимо получить письменное согласие пациента. В соответствии с большинством случаев применения ремдесивира в клинических исследованиях на сегодняшний день, его следует использовать для лечения инфекции COVID-19 тяжелой степени у пациентов, SpO2 которых составляет 94% и менее (требуется дополнительная подача кислорода, ИВЛ, ЭКМО).
Среди препаратов, применяющихся для лечения COVID-19, следует отметить противомалярийное средство гидроксихлорохин. Оно используется для терапии малярии и некоторых других протозойных инфекций. Кроме того, в связи с противовоспалительным и иммуносупрессивным эффектом, гидроксихлорохин нашел свое применение в лечении пациентов с системными заболеваниями соединительной ткани, такими как ревматоидный артрит и системная красная волчанка. Механизм действия гидроксихлорохина против некоторых вирусных инфекций изучен не до конца, в опубликованных данных отмечаются несколько вариантов его воздействия на COVID-19, которые препятствуют проникновению вируса в клетку и его репликации. В небольших клинических исследованиях было показано, что комбинация азитромицина с гидроксихлорохином усиливает противовирусный эффект последнего.
ВОЗ прекратила научные изыскания в группе лечения гидроксихлорохином в рамках исследования эффективных препаратов для борьбы с COVID-19 «Solidarity». Решение принято с учетом данных, которые указывают на то, что применение гидроксихлорохина не приводит к сокращению смертности среди госпитализированных пациентов с COVID-19 по сравнению со стандартом оказания помощи.
Однако, следует отметить, что результаты большого количества опубликованных зарубежных исследований, а также отечественный опыт указывают на возможность эффективного применения гидроксихлорохина в низких дозах, в меньшей степени ассоциированных с нарушениями сердечного ритма, у пациентов с легкой и среднетяжелой формой COVID-19 при назначении в течение первых 3-5 дней заболевания. Использование гидроксихлорохина у пациентов с тяжелым течением заболевания, как правило, оказывается неэффективным. Решение вопроса о назначении гидроксихлорохина должно приниматься индивидуально на основе оценки соотнесения пользы и риска для конкретного пациента. Возможно, применение гидроксихлорохина может предотвратить развитие тяжелых форм инфекции.
Перед назначением гидроксихлорохина и во время их приема следует уделить особое внимание результату ЭКГ, в частности, величине QT. Гидроксихлорохин обладает кардиотоксичностью, и его прием может сопровождаться развитием, например, синдрома удлиненного QT. Вопросы о назначении гидроксихлорохина в случае измененной ЭКГ и о дальнейшей терапии в случае возникших при лечении изменений ЭКГ решаются строго индивидуально, в тесном взаимодействии с кардиологами.
Для контроля кардиотоксичности гидроксихлорохина необходимо проведение инструментального и клинического мониторинга, в том числе интервала QT, у всех пациентов, которым планируется назначение гидроксихлорохина.
ЭКГ назначается перед началом лечения, контроль осуществляется 1 раз в 5 дней. Продолжительность интервала QT (корригированного) предпочтительно оценивать с использованием формул Fridericia или Framingham, она не должна превышать 470 мс (у мужчин) и 480 мс (у женщин). Следует оценить уровень печеночных трансаминаз, Ca2+, Mg2+, K+. Алгоритм оценки корригированного интервала QT, электролитных нарушений представлен в Приложении 2-1.


При появлении жалоб на аритмию, ощущения сердцебиения, боли и дискомфорта в области сердца, эпизодов слабости и головокружения, синкопальных состояний назначается внеочередное ЭКГ.
В нескольких небольших клинических исследованиях у больных с COVID-19 было показано, что терапия гидроксихлорохином нередко ассоциирована с развитием серьезных неблагоприятных побочных реакций (НПР), прежде всего со стороны сердечно-сосудистой системы. По данным французских центров фармаконадзора, из 120 поступивших за месяц спонтанных сообщений об развитии НПР у больных с COVID-19 85,8% связаны с использованием гидроксихлорохина, причем в половине случаев НПР гидроксихлорохин был назначен совместно с азитромицином.
При этом медиана возраста пациентов составила 65 лет, что говорит о том, что половина спонтанных сообщений об НПР приходилось на пациентов моложе 65 лет и что пациенты более молодого возраста также подвержены риску сердечно-сосудистых осложнений на фоне терапии гидроксихлорохином. Данные французских центров фармаконадзора коррелируют и результатами других международных регистров.
Учитывая недостаточные доказательства эффективности терапии COVID-19 гидроксихлорохином, относительно высокую частоту развития кардиальных осложнений, а также позиции ряда регуляторных органов и профессиональных сообществ (Food and Drug Administration и Heart Rhythm Society) по ограничению амбулаторного применения гидроксихлорохина при COVID-19, при лечении COVID-19 вне стационарных условий целесообразно рассмотреть соблюдение следующих условий:
• Исследование ЭКГ в 12 отведениях с расчетом и документированием корригированного интервала QT (предпочтительно с использованием формул Fridericia или Framingham). Не рекомендуется использовать гидроксихлорохин без исходной ЭКГ с расчетом QTc;
• Не рекомендуется использовать гидроксихлорохин при исходном QTc ≥ 500 мс.
• Если QTc ≥ 460 мс (у детей) или ≥ 470 мс (у мужчин) и ≥ 480 мс (у женщин), но < 500 мс, то перед назначением гидроксихлорохина следует скорректировать уровень Ca2+, Mg2+, K+, отменить другие лекарственные препараты, которые могут удлинять интервал QT и не являются жизненно важными для пациента.
• Если QTc < 460 мс (у детей), < 470 мс (у мужчин), < 480 мс (у женщин), то возможно назначение гидроксихлорохина.
• Перед назначением гидроксихлорохина необходимо оценить наличие противопоказаний, функцию почек, функцию печени, и при наличии возможности - уровень K+, Mg2+.
• Для контроля кардиотоксичности при наличии возможности целесообразно проведение ЭКГ на 3-й день терапии гидроксихлорохином через 2-3 ч после приема дозы препарата. Если QTc увеличивается более 60 мс (QTc ≥ 60 мс) или абсолютное значение QTc > 500 мс, необходимо рассмотреть возможность прекращения терапии.
• В условиях карантина либо ограниченности ресурсов следует рассмотреть вариант ведения больного без дополнительной регистрации ЭКГ исходно и в динамике при низком риске лекарственно-ассоциированного удлинения интервала QT по шкале Тисдейла (≤ 6 баллов) и отсутствии дополнительных факторов риска удлинения интервала QT согласно модифицированному чек-листу.
• Максимально возможная оценка симптомов возможного удлинения интервала QT по телефону: все амбулаторные пациенты должны тщательно следить за симптомами, обращая внимание на факторы риска аритмии (обмороки, обезвоживание, прием новых лекарств и ухудшение состояния здоровья). При выявлении факторы риска аритмии показано внеочередное ЭКГ.
На сегодняшний день нет четких указаний профессиональных сообществ относительно того, как организовать мониторинг безопасности при амбулаторном применении гидроксихлорохина, в том числе без возможности контроля ЭКГ. В случае амбулаторного применения гидроксихлорохина в условиях карантина и ограниченности ресурсов (отсутствие возможности контроля ЭКГ и электролитов в плазме) следует рассмотреть вариант ведения больного с обязательным соблюдением двух ограничительных условий, указанных в алгоритме Приложения 2-2:


1) низкий риск лекарственно-ассоциированного удлинения интервала QT по шкале Тисдейла (≤ 6 баллов)
2) отсутствии дополнительных факторов риска удлинения интервала QT согласно модифицированному чек-листу.
Рекомбинантный интерферон альфа 2b (ИФН-α2b) для интраназального введения обладает иммуномодулирующим, противовоспалительным и противовирусным действием. Механизм действия основан на предотвращении репликации вирусов, попадающих в организм через дыхательные пути. Как правило, препарат используется в дозе 3000 МЕ интраназально 5 раз в сутки в течение 5 дней.
Этиотропное лечение COVID-19, особенно у больных с сопутствующей патологией, требует внимания к возможным лекарственным взаимодействиям. Лекарственные препараты, которые запрещено или нежелательно принимать с этиотропной терапией COVID-19, можно найти на сайте https://www.covid19druginteractions.org/. Лекарственные взаимодействия антитромботических и препаратов для лечения пациентов с COVID-19 указаны в Приложении 3.
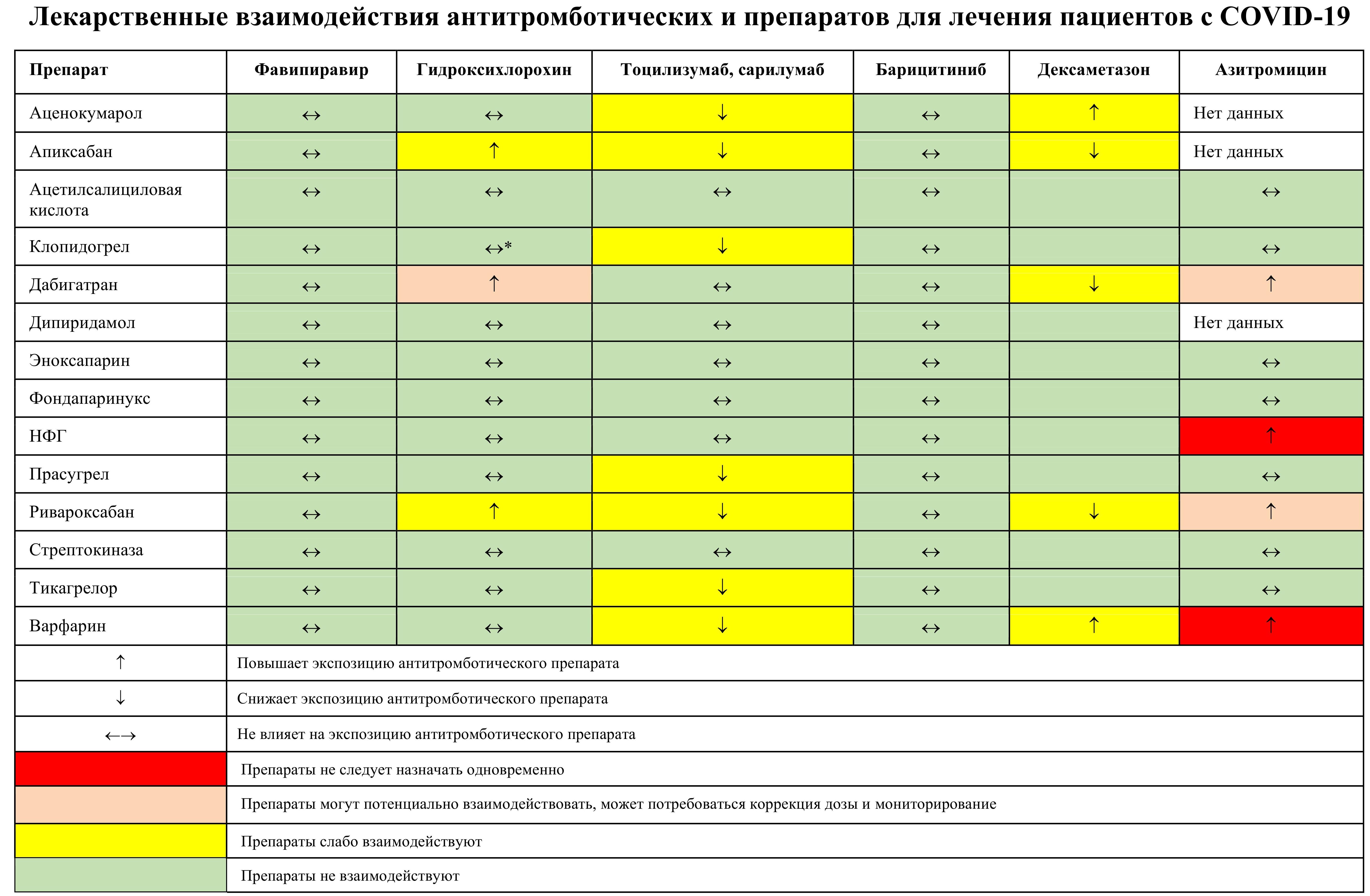

Принимая во внимание сходство клинической картины легких форм COVID-19 с клинической картиной сезонных ОРВИ, до подтверждения этиологического диагноза в схемы терапии следует включать препараты, рекомендуемые для лечения сезонных ОРВИ, такие как интраназальные формы ИФН-α, препараты индукторов ИФН, а также противовирусные препараты с широким спектром активности, такие как умифеновир.
Перечень возможных к назначению лекарственных препаратов для этиотропной терапии COVID-19 у взрослых приведен в Приложении 1.


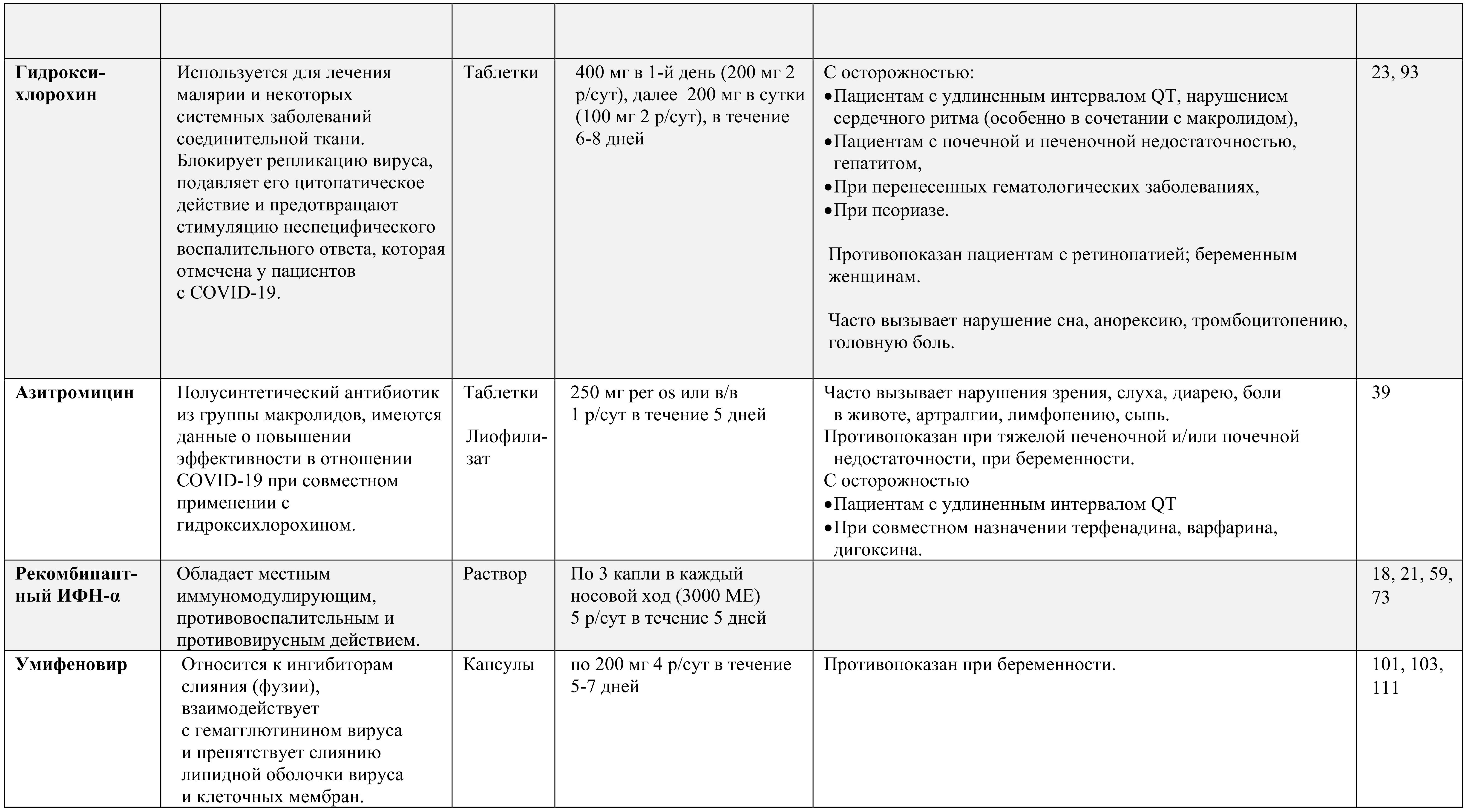

Рекомендованные схемы лечения в зависимости от тяжести заболевания приведены в Приложении 4.








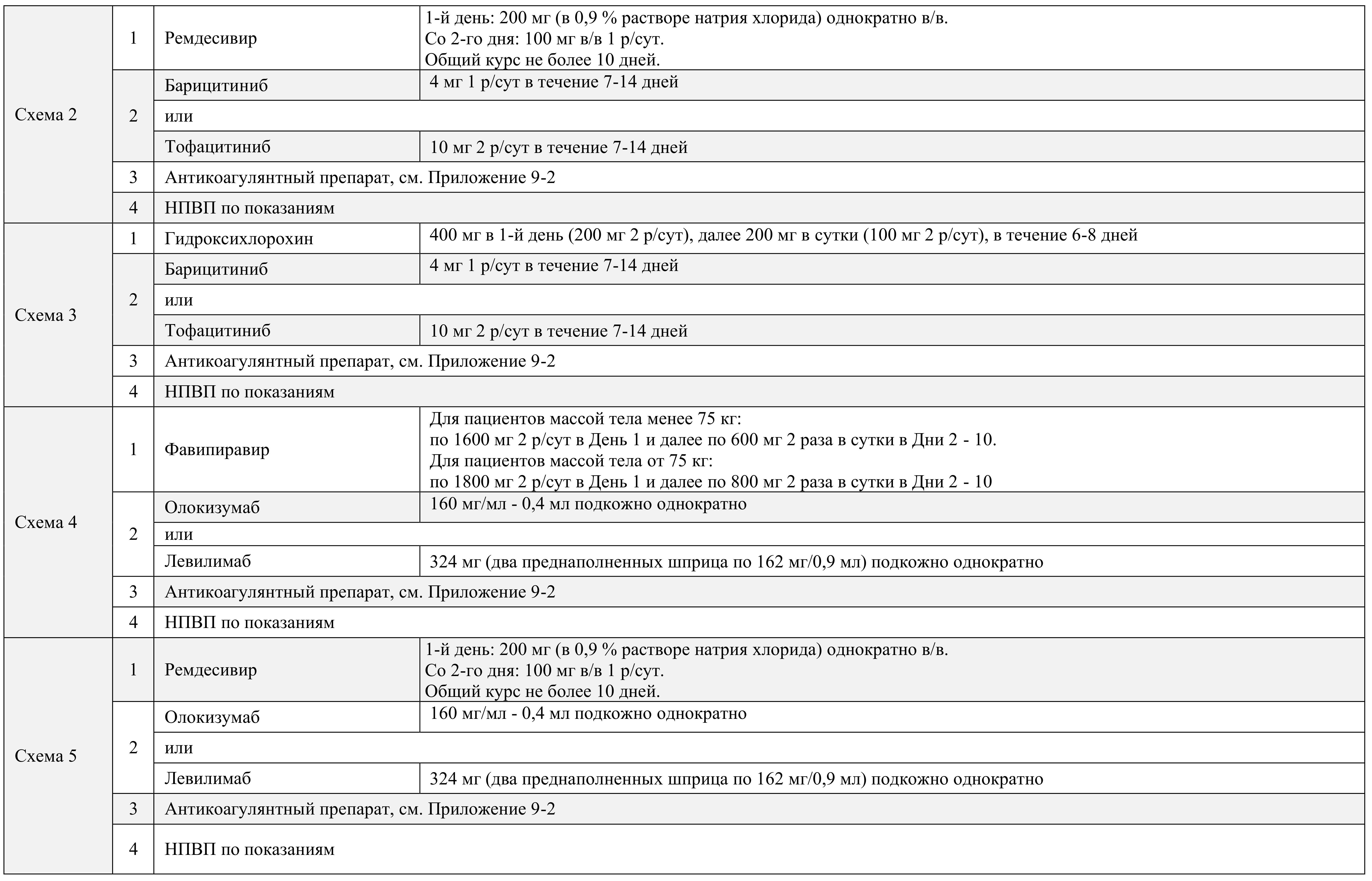
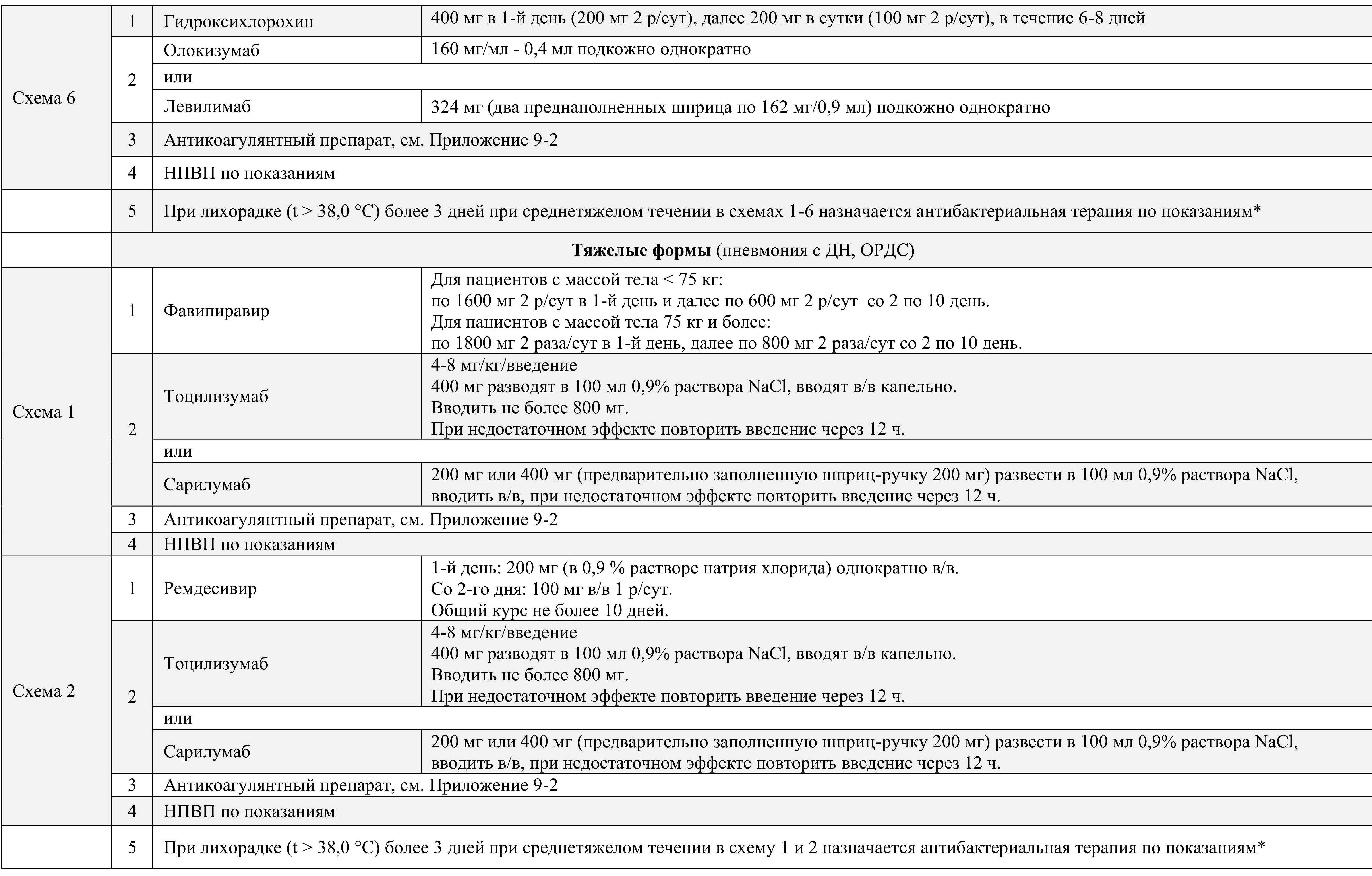


Назначение лечения должно обязательно сопровождаться получением добровольного информированного согласия пациента (или его законного представителя). 



Согласно рекомендациям ВОЗ, возможно назначение препаратов с предполагаемой этиотропной эффективностью «off-label» (то есть применение с медицинской целью не соответствует инструкции по медицинскому применению), при этом их назначение должно соответствовать этическим нормам, рекомендованным ВОЗ.
Вышеуказанная практика оценки целесообразности применения лекарственных препаратов вне показаний, указанных в инструкции по медицинскому применению, является общепризнанной в мире. В текущих условиях распространения новой коронавирусной инфекции и ограниченности доказательной базы по лечению COVID-19, использование препаратов в режиме «off-label» для оказания медицинской помощи пациентам с COVID-19 базируется на международных рекомендациях, а также согласованных экспертных мнениях, основанных на оценке степени пользы и риска при использовании терапии в режиме «off-label».
Информация о случаях побочных действий, не указанных в инструкции по применению лекарственных препаратов, о серьезных нежелательных реакциях, непредвиденных нежелательных реакциях при применении лекарственных препаратов, об особенностях взаимодействия лекарственных препаратов с другими лекарственными препаратами должна собираться и передаваться в установленном порядке в Росздравнадзор.
Согласно рекомендациям ВОЗ, применение плазмы от доноров-реконвалесцентов (лиц с подтвержденным случаем COVID-19 в стадии выздоровления) с целью лечения заболеваний, характеризующихся эпидемическими вспышками и отсутствием специфического лечения, основано на концепции пассивной иммунизации. По опубликованным данным, в КНР и других странах применялась плазма, полученная от доноров-реконвалесцентов COVID-19 (далее – антиковидная плазма), что нашло отражение в национальных руководствах по лечению COVID-19.
Заготовка, хранение, транспортировка и клиническое использование антиковидной плазмы осуществляется в соответствии с требованиями, установленными постановлением Правительства Российской Федерации от 22 июня 2019 г. № 797 «Об утверждении Правил заготовки, хранения, транспортировки и клинического использования донорской крови и ее компонентов и о признании утратившими силу некоторых актов Правительства Российской Федерации», приказом
Министерства здравоохранения Российской Федерации от 02.04.2013 № 183н «Об утверждении правил клинического использования донорской крови и (или) ее компонентов».
Порядок медицинского обследования доноров (приказ Министерства здравоохранения Российской Федерации от 14.09.2001 № 364 «Об утверждении Порядка медицинского обследования донора крови и ее компонентов» (с изменениями и дополнениями)) и осуществление донации при заготовке антиковидной плазмы помимо установленных обязательных требований имеют ряд особенностей, которые должны быть учтены с целью обеспечения безопасности донора и реципиента, а именно:
• Возраст 18-55 лет;
• Масса тела более 50 кг;
• Не ранее чем через 14 дней после исчезновения клинических симптомов и двукратном отрицательном результате на РНК SARS-CoV-2 в орофарингеальном мазке, взятом с интервалом не менее 24 ч;
• Вируснейтрализующая активность плазмы в разведении 1:160; в случае отсутствия доноров с оптимальной вируснейтрализующей активностью плазмы допускается осуществлять заготовку от доноров с вируснейтрализующей активностью плазмы 1:80. Вируснейтрализующая активность плазмы определяется в тесте с использованием пермиссивной культуры клеток, или с помощью набора реагентов для определения содержания антител к антигенам SARS-CoV-2, для которого экспериментально установлена достаточна корреляция между результатами определения содержания антител в плазме с вируснейтрализующей активностью, определенной в тесте с использованием пермиссивной культуры клеток; возможно сохранять контрольный образец плазмы донора для проведения исследований ее вируснейтрализующей способности в более поздние сроки;
• Концентрация общего белка крови не менее 65 г/л.
При незначительных изменениях, выявленных в ходе лабораторного обследования донора, решение о допуске к донации принимается врачом-трансфузиологом по согласованию с заведующим отделением.
Интервал между донациями должен составлять не менее 14 дней.
Показания к клиническому использованию антиковидной плазмы:
1. Оптимально в период от 3 до 7 дней с момента появления клинических симптомов заболевания у пациентов:
• в тяжелом состоянии, с положительным результатом на РНК SARS-CoV-2;
• с проявлениями ОРДС.
2. В случае длительности заболевания более 21 дня при неэффективности проводимого лечения и положительном результате на РНК SARS-CoV-2.
В случае необходимости при наличии показаний у пациента возможно проведение повторных трансфузий антиковидной плазмы.
Противопоказания к клиническому использованию антиковидной плазмы:
• Аллергические реакции на белки плазмы или цитрат натрия в анамнезе;
• Пациентам с аутоиммунными заболеваниями или селективным дефицитом IgА в анамнезе необходима тщательная оценка возможных побочных эффектов.
Заготовка антиковидной плазмы:
• Осуществляется методом плазмафереза и (или) методом центрифугирования из единицы крови;
• Объем донации определяется врачом-трансфузиологом и составляет 200-600 мл с обязательной инактивацией патогенов заготовленной плазмы.
Заготовленный компонент крови маркируется «Плазма антиковидная, патогенредуцированная».
Суммарный объем трансфузии составляет 5-10 мл антиковидной плазмы/кг веса пациента, в среднем 400-600 мл. Антиковидная плазма также может быть использована для плазмозамещения при выполнении плазмафереза.
Этиотропное лечение COVID-19 женщин в период беременности и кормления грудью в настоящее время не разработано. Рекомбинантный ИФНβ-1b, противомалярийные препараты противопоказаны к применению во время беременности. Однако в качестве этиотропной терапии возможно назначение противовирусных препаратов с учетом их эффективности против COVID-19 по жизненным показаниям. В остальных случаях следует учитывать их безопасность при беременности и в период грудного вскармливания.
Лечение должно быть начато как можно раньше, что в большей степени обеспечивает выздоровление. Противовирусные препараты беременным с тяжелым или прогрессирующим течением заболевания необходимо назначать и в более поздние сроки от начала заболевания.
При назначении противовирусных препаратов кормящим женщинам решение вопроса о продолжении грудного вскармливания зависит от тяжести состояния матери.
В настоящее время продолжаются клинические исследования эффективности и безопасности глюкокортикоидов (ГК) и таргетных препаратов у пациентов с тяжелым/критическим течением коронавирусной инфекции.
Учитывая, что вторичный синдром активации макрофагов (САМ)/ гемофагоцитарный лимфогистоцитоз (ГЛГ) при COVID-19 является следствием массированной неконтролируемой активации иммунной системы, спровоцированной острой вирусной инфекцией, пациентам, наряду с симптоматической и этиотропной терапией, в подавляющем большинстве случаев должна проводиться иммуносупрессивная терапия для подавления гиперактивации иммунной системы.
Опыт лечения первичного и вторичного САМ/ГЛГ в ревматологической и гематологической практике, а также синдрома высвобождения цитокинов предполагает раннюю терапевтическую интервенцию для предотвращения необратимого повреждения тканей и неконтролируемой полиорганной недостаточности.
Глюкокортикоиды являются препаратами первого выбора для лечения больных с первичным ГЛГ и вторичным САМ/ГЛГ, они угнетают все фазы воспаления, синтез широкого спектра провоспалительных медиаторов, увеличение концентрации которых в рамках цитокинового шторма ассоциируется с неблагоприятным прогнозом при COVID‑19 и риском развития ОРДС и сепсиса.
Для проявления полного эффекта ГК необходимо несколько часов. Максимум фармакологической активности ГК приходится на тот период времени, когда их пиковые концентрации в крови уже позади.
Различные схемы применения ГК включены в американские, английские, итальянские и др. протоколы лечения COVID-19.
В настоящее время получены предварительные данные крупного исследования RECOVERY, которые показали, что дексаметазон в низких дозах играет положительную роль в лечении тяжелых форм COVID-19: пероральный или внутривенный дексаметазон снизил 28-дневную смертность среди госпитализированных пациентов по сравнению с обычным лечением.
Не рекомендовано использовать ГК для профилактики или лечения COVID-19 от легкой до умеренной степени (т.е. у пациентов, не получающих кислород).
ГК назначаются только пациентам с признаками цитокинового шторма.
Для терапии цитокинового шторма могут применяться различные схемы введения ГК: метилпреднизолон в дозе 1 мг/кг/введение внутривенно каждые 12 ч, или метилпреднизолон 120 мг/внутривенно каждые 8 ч, или дексаметазон в дозе 20 мг/сутки внутривенно за 1 или 2 введения.
Максимальная доза ГК применяется в течение 3-4 суток. Доза ГК снижается при стабилизации состояния (купирование лихорадки, стабильное снижение уровня СРБ, ферритина, АЛТ, АСТ, ЛДГ сыворотки крови).
При прогрессировании синдрома активации макрофагов (нарастание уровня ферритина, СРБ сыворотки крови, развитие двух-трехростковой цитопении) метилпреднизолон применяется по схеме 120-125 мг/введение/внутривенно каждые 6-8 ч или дексаметазон 20 мг/внутривенно в два введения в течение не менее 3 дней с последующим постепенным снижением дозы. Снижение дозы МП/дексаметазона начинается при условии снижения уровня ферритина сыворотки крови не менее чем на 15%.
Доза внутривенно вводимого ГК постепенно снижается на 20‑25% на введение каждые 1‑2 суток в течение 3-4 суток, далее на 50% каждые 1-2 суток, до полной отмены.
В дальнейшем необходимо применение поддерживающей дозы метилпреднизолона 6-12 мг/сут (длительность терапии и дозы зависят от клинической ситуации). Применение ГК должно быть в сочетании с антикоагулянтной терапией НМГ.
Пациенты, получающие ГК, должны находиться под наблюдением на предмет побочных эффектов. У тяжелобольных пациентов к ним относятся гипергликемия и повышенный риск инфекций (включая бактериальные, грибковые); частота этих инфекций у пациентов с COVID-19 неизвестна.
ГК также могут играть роль в лечении рефрактерного септического шока (СШ) у тяжелобольных. В наибольшей степени позитивный гемодинамический эффект ГКС наблюдается у лиц с относительной надпочечниковой недостаточностью. При СШ длительностью менее 1 суток, или необходимости использования норадреналина в дозе, превышающей 0,5 мкг/кг/мин, рекомендовано назначение гидрокортизона в дозе 200-300 мг/сутки.
Одними из ключевых цитокинов, обеспечивающих гипервоспаление у пациентов с COVID-19, являются ИЛ-1 и ИЛ-6. Они индуцируют синтез ферритина, высокий уровень, которого ассоциируются с САМ/ГЛГ и смертностью пациентов с COVID-19. Янус-киназы (JAK – семейство ферментов) регулируют трансдукцию сигнала в иммунные клетки. Ингибирование цитокинов и активности янус-киназ играет важную роль в блокировании цитокинового шторма.
В рекомендациях по лечению пациентов с COVID-19 Национального института здоровья (США) нет рекомендаций по применению или неприменению ингибиторов ИЛ-6, ИЛ-1 и других биотехнологических препаратов при критических формах COVID-19 в связи с недостаточностью данных об их эффективности и безопасности.
Тем не менее, в реальной клинической практике ингибиторы ИЛ-6 и ИЛ-1 применяются для лечения критических форм COVID-19.
Таргетную терапию ингибиторами ИЛ-6 (тоцилизумабом или сарилумабом) или ИЛ-1β (канакинумабом) в комбинации с ГК рекомендуется инициировать до развития тяжелого поражения легких с целью подавления цитокинового шторма и предотвращения развития полиорганной недостаточности.
Показаниями для назначения тоцилизумаба, сарилумаба и канакинумаба являются сочетание данных КТ ОГК (значительный объем поражения легочной паренхимы – более 50% (КТ3‑4) с двумя и более признаками):
• Снижение SpO2;
• СРБ > 60 мг/л или рост уровня СРБ в 3 раза на 8‑14 дни заболевания;
• Лихорадка > 38 °C в течение 5 дней;
• Число лейкоцитов < 3,0*109/л;
• Абсолютное число лимфоцитов < 1*109/л • Уровень ферритина крови > 500 нг/мл;
• Уровень ИЛ‑6 > 40 пк/мл.
При среднетяжелой форме пневмонии с целью подавления гипервоспаления и предотвращения развития серьезных поражений легких и других органов, обусловленных COVID‑19, можно рассматривать назначение ингибиторов янус‑киназ – препаратов барицитиниб и тофацитиниб, а также ингибиторов ИЛ‑6 олокизумаба и левилимаба.
Показаниями для назначения ингибиторов янус-киназ (тофацитиниба и барицитиниба) и ингибитора ИЛ‑6 (олокизумаба и левилимаба) являются сочетание данных КТ ОГК (КТ2‑3 с двумя и более признаками):
• Снижение SpO2;
• СРБ > 30 мг/л
• Лихорадка > 38 °C в течение 3 дней;
• Число лейкоцитов < 3,0*109/л;
• Абсолютное число лимфоцитов < 1,0*109/л
Для быстрого купирования цитокинового шторма тоцилизумаб назначается в дозе 4‑8 мг/кг внутривенно (доза препарата рассчитывается на массу тела) в сочетании с ГК.
При наличии признаков надпочечниковой недостаточности внутривенно вводится гидрокортизон в дозе 50‑100 мг, с последующим медленным внутривенным введением препарата в течение 1 ч в дозе 200 мг в сутки.
Повторное введение тоцилизумаба возможно при сохранении фебрильной лихорадки более 12 ч после первой инфузии, отсутствии снижения уровня сывороточного СРБ при исключении инфекционных осложнений.
Необходимо помнить, что при повторном введении тоцилизумаба повышается риск развития вторичной инфекции (сепсис, оппортунистическая, грибковая инфекция).
Потенциальной терапевтической технологией лечения COVID‑19 – индуцированного цитокинового шторма может быть ингибиция ИЛ-1β.
Для блокирования цитокинового шторма возможно применение моноклонального антитела к ИЛ-1β – канакинумаба в дозе 4‑8 мг/кг/внутривенно, который показал высокую эффективность при лечении системного ювенильного идиопатического артрита с гемофагоцитарным синдромом и аутовоспалительных синдромов, в основе механизма развития которых лежит цитокиновый шторм.
Противопоказания для назначения генно-инженерных биологических препаратов:
• Сепсис, подтвержденный патогенами, отличными от COVID‑19;
• Гиперчувствительность к любому компоненту препарата;
• Вирусный гепатит В;
• Сопутствующие заболевания, связанные, согласно клиническому решению, с неблагоприятным прогнозом;
• Иммуносупрессивная терапия при трансплантации органов;
• Нейтропения < 0,5*109/л;
• Повышение активности АСТ или АЛТ более чем в 5 норм;
• Тромбоцитопения < 50*109/л.
• При беременности применение ГИБП нежелательно;
• На фоне терапии блокаторами ИЛ‑6 следует помнить о возникновении серьезных неже‑ лательных явлений;
• Инфекционные заболевания: бактериальная пневмония, флегмона, инфекции, вызванные Herpes zoster, и др.;
• Повышение активности печеночных трансаминаз.
• Сыпь, зуд, крапивница;
• Повышение артериального давления;
• Лейкопения, нейтропения, тромбоцитопения;
• Повышение показателей липидного обмена (общего холестерина, триглицеридов, ЛПВП, ЛПНП).
При внутривенном введении тоцилизумаба должен быть предусмотрен комплекс необходимых мероприятий для лечения возможной анафилактической реакции.
На фоне применения генно‑инженерных биологических препаратов в условиях острой вирусной инфекции повышается риск развития бактериальной, в том числе оппортунистической (грибковой) инфекции.
Особенности течения вторичной бактериальной инфекции в условиях лечения генно-инженерными биологическими препаратами включают: отсутствие лихорадки или низкий субфебрилитет, низкие (или незначительно повышенные) маркеры воспаления (уровень СРБ сыворотки крови, прокальцитонина, число лейкоцитов крови), развитие нейтропении.
При нарастании признаков дыхательной недостаточности, появлении субфебрильной/фебрильной лихорадки при нормальных/умеренно повышенных/значительно повышенных маркерах воспаления (СОЭ, показатели СРБ, прокальцитонина и лейкоцитов крови) необходимо заподозрить развитие грибковой и/или оппортунистической инфекции и провести:
- микробиологическое (культуральное) исследование бронхоальвеолярной лаважной жидкости, мокроты или эндотрахеального аспирата на бактерии и грибы (дрожжевые и мицелиaльные) и на ДНК Mycobacterium tuberculosis, Pneumocystis jirovecii, Mycoplasma pneumoniae, Chlamidia pneumoniae методом ПЦР;
- исследование крови на антитела класса А и M (IgА, IgM) к грибам рода аспергиллы (Aspergillus spp.), Pneumocystis jirovecii, Mycoplasma pneumoniae,
Chlamydophila pneumoniae;
- контрольную КТ органов грудной клетки для подтверждения/исключения развития интерстициальной пневмонии.
Препараты для упреждающей противовоспалительной терапии представлены в Приложении 5.



Следствием тяжелого жизнеугрожающего синдрома высвобождения цитокинов может стать развитие нарушений свертывания крови. В начальных стадиях заболевания характерно развитие гиперкоагуляции без признаков потребления и ДВС‑синдрома.
Коагулопатия при COVID-19 характеризуется активацией системы свертывания крови в виде значительного повышения концентрации D-димера в крови. Количество тромбоцитов умеренно снижено (число тромбоцитов < 150*109/л находят у 70-95% больных), незначительно удлинено протромбиновое время, значительно повышен фибриноген. Единичные исследования указывают, что концентрация в крови антитромбина редко снижается менее 80%. Концентрация протеина С также существенно не меняется. Таким образом, коагулопатия при COVID-19, наряду с признаками, характерными для развернутой фазы ДВС-синдрома в виде высокого уровня D-димера, не имеет типичных признаков потребления фибриногена и тромбоцитов. Также не отмечено потребления компонентов противосвертывающей системы антитромбина и протеина С, характерного для ДВС-синдрома, отмечаемого при сепсисе. Интерес к коагулопатии при COVID-19 связан с тем, что ее наличие ассоциируется с риском смерти. Кроме того, у больных COVID-19 часто находят артериальный и венозный тромбоз.
Анализ секционных данных пациентов, погибших от COVID-19, указывает на наличие помимо диффузного повреждения альвеол, множества тромбозов мелких сосудов легких и связанных с ним множественных геморрагий в альвеолах. В тромботический процесс в легких вовлечены мегакариоциты, тромбоциты, формирующиеся тромбы богаты не только фибрином, но и тромбоцитами. Отмечаются признаки тромботической микроангиопатии в легких.
Данные электронной микроскопии свидетельствует о наличии значительного повреждения эндотелиальных клеток, связанного с проникновением в клетки SARS-CoV-2, распространенного тромбоза мелких сосудов, микроангиопатии,
окклюзии капилляров альвеол и признаков неоангиогенеза.
ДВС-синдром развивается, как правило, на поздних стадиях заболевания. Он встречается лишь у 0,6% выживших больных и в 71,4% у умерших больных. Развитие гиперкоагуляции сопряжено с риском развития тромботических осложнений. Для верификации диагноза ТЭЛА необходимо выполнение КТ с внутривенным контрастированием, для диагностики тромбоза глубоких вен (ТГВ) нижних конечностей – проведение УЗИ сосудов нижних конечностей.
При госпитализации пациентов с подозрением на COVID-19 или подтвержденным COVID-19 рекомендуется тесты для скрининга нарушений гемостаза: определение в крови уровня D-димера, протромбинового времени, фибриногена и развернутого анализа крови, включающего количество тромбоцитов.
Профилактику ТГВ нижних конечностей/ТЭЛА с использованием профилактических доз НМГ/НФГ целесообразно проводить больным со среднетяжёлой формой COVID-19, которые лечатся дома и имеют высокий риск венозных тромбоэмболических осложнений, низкий риск кровотечений и не получают антикоагулянтного лечения по другим показаниям. Это относится прежде всего к больным с сильно ограниченной подвижностью, ТГВ/ТЭЛА в анамнезе, активным злокачественным новообразованием, крупной операцией или травмой в предшествуюший месяц, носителям ряда тромбофилий (дефициты антитромбина, протеинов С или S, антифиосфолипидный синдром, фактор V Лейден, мутация гена протромбина G-20210A), а также при сочетании дополнительных факторов риска ТГВ/ТЭЛА (возраст старше 70 лет, сердечная/дыхательная недостаточность, ожирение, системное заболевание соединительной ткани, гормональная заместительная терапия/приём оральных контрацептивов). В амбулаторной практике может быть рекомендовано применение прямых пероральных антикоагулянтов: апиксабан по 2,5 мг 2 раза в сутки или ривароксабан 10 мг 1 раз в сутки (Приложение 6-1).

При этом следует уделять особое внимание наличию противопоказаний (прежде всего выраженная почечная недостаточность). Во время использования антикоагулянтов необходимо повторно оценивать риск и активно искать признаки кровотечений. 
Необходимо учитывать, что при амбулаторном лечении антикоагулянты в первичной профилактике ТГВ/ТЭЛА изучены недостаточно.
Назначение низкомолекулярных гепаринов (НМГ), как минимум, в профилактических дозах показано ВСЕМ госпитализированным пациентам и должно продолжаться как минимум до выписки. Нет доказанных преимуществ какого-либо одного НМГ по сравнению с другими. При недоступности НМГ или противопоказаниях к ним возможно использование нефракционированного гепарина (НФГ). Увеличение дозы гепарина до промежуточной или лечебной может быть рассмотрено у больных с высоким и крайне высоким уровнем D-димера, при наличии дополнительных факторов риска венозных тромбоэмболических осложнений, а также при тяжелых проявлениях COVID-19, лечении в блоке ОРИТ. У больных с ожирением (индекс массы тела > 30 кг/м2) следует рассмотреть увеличение профилактической дозы на 50%.
Дозы препаратов гепарина представлены в Приложении 6-2.

Продленная профилактика у больных с COVID-19 после выписки может быть рассмотрена при сохраняющемся повышенном риске венозных тромбоэмболических осложнений и низком риске кровотечений в случаях, когда не требуются лечебные дозы антикоагулянта по другим показаниям. В качестве антикоагулянтов для продленной профилактики венозных тромбоэмболических осложнений имеется доказательная база для профилактических доз эноксапарина и ривароксабан в дозе 10 мг 1 раз в сутки. Кандидатами для продленной профилактики ТГВ (вплоть до 45 дней после выписки) могут быть больные пожилого возраста, больные, лечившиеся в блоке интенсивной терапии, с активным злокачественным новообразованием, ТГВ/ТЭЛА в анамнезе, сохраняющимся выраженным ограничением подвижности, концентрацией D-димера в крови > 2 раз выше верхней границы нормы. 
При тромботических осложнениях следует использовать лечебные дозы НМГ/НФГ. Применение лечебных доз НМГ/НФГ может рассматриваться также у больных с клиническим подозрением на тромботические осложнения, когда нет возможности верифицировать диагноз. Лечение ТГВ/ТЭЛА, ассоциированных с COVID-19, антикоагулянтами следует продолжать не менее 3 месяцев; после выписки предпочтительно использовать прямые пероральные антикоагулянты, если к ним нет противопоказаний.
Список возможных к назначению антикоагулянтов представлен в Приложении 6-2.

У пациентов с иммунной тромбоцитопенией, вызванной гепарином, а также при исходно низком количестве тромбоцитов, для профилактики и лечения венозных тромбоэмболических осложнений рекомендуется использовать фондапаринукс натрия. Фондапаринукс натрия, в отличие препаратов НМГ/НФГ, лишен потенциально благоприятных плейотропных эффектов, однако, с другой стороны, он не вызывает гепарин-индуцированную тромбоцитопению. 
НМГ, фондапаринукс натрия не рекомендуется использовать у пациентов с выраженной почечной недостаточностью или быстро меняющейся функцией почек.
Противопоказания для использования антикоагулянтов – продолжающееся кровотечение, уровень тромбоцитов в крови ниже 25*109/л, выраженная почечная недостаточность (для НМГ и фондапаринукса натрия). Повышенное протромбиновое время и АЧТВ не относятся к противопоказаниям к назначению антикоагулянтов. Если антикоагулянты противопоказаны, следует использовать механические способы профилактики ТГВ нижних конечностей (предпочтительно перемежающуюся пневматическую компрессию).
Данных о применении прямых пероральных антикоагулянтов при COVID-19 нет. Пациентам, получающим пероральные антикоагулянты по другим показаниям, при не тяжелых проявлениях COVID‑19, их прием можно продолжить. При неприемлемых лекарственных взаимодействиях с препаратами для лечения COVID‑19 (прием лопиновира/ритонавира), а также при тяжелой форме COVID‑19 рекомендуется переход на лечебные дозы гепарина (предпочтительно НМГ).
Кратность определения D-димера, протромбинового времени, фибриногена и количества тромбоцитов зависит от тяжести COVID‑19 инфекции, важна динамика как в сторону повышения, так и понижения показателей. У госпитализированных больных при легком варианте течения 1 раз в 4‑5 дней, при средней тяжести 1 раз в два дня, при тяжелом – ежедневно. Внеочередной анализ вышеперечисленных показателей берется при усугублении тяжести по COVID‑19.
Для диагностики ДВС-синдрома рекомендуется использовать критерии Международного общества тромбоза и гемостаза (таблица 2). Диагноз ДВС‑синдрома устанавливается при наличии 5 баллов по этим критериям.
У пациентов с коагулопатией потребления при отсутствии кровотечений следует поддерживать количество тромбоцитов выше 20*109/л, плазменную концентрацию фибриногена – выше 2,0 г/л. У пациентов с кровотечениями следует поддерживать количество тромбоцитов выше 50*109/л, плазменную концентрацию фибриногена – выше 2,0 г/л, протромбиновое отношение < 1,5.
У больных в критическом состоянии, а также при использовании методов экстракорпоральной поддержки кровообращения, при отсутствии возможности мониторировать состояние системы гемостаза традиционными методами допустимо использовать глобальные тесты (тромбоэластография) при наличии опыта их применения и интерпретации.
Основными критериями эффективности упреждающей противовоспалительной терапии являются динамика клинического ответа: снижение уровня лихорадки, улучшение самочувствия, появление аппетита, уменьшение одышки, повышение SpО2. При этом эффект от блокаторов ИЛ-6 наступает в течение 12 ч (чаще используются 1-2 инъекции), лечения ГК – от 12 до 72 ч (курс 2-3 суток), терапии антикоагулянтами – от 120 ч (курс от 5 дней). Если эффект от упреждающей противовоспалительной терапии не получен, то необходимо предполагать другие причины ухудшения состояния (прогрессирование пневмонии, сепсис и др.).
При лечении COVID-19 необходимо обеспечивать достаточное поступление жидкости в организм. Восполнение суточной потребности в жидкости должно обеспечиваться преимущественно за счет пероральной регидратации. Суточная потребность в жидкости должна рассчитываться с учетом лихорадки, одышки, потерь жидкости при диарее, рвоте (в случае наличия у пациента таких симптомов). С целью профилактики отека легких пациентам следует ограничить объем вводимой жидкости, соблюдать нулевой или отрицательный гидробаланс. При выраженной интоксикации, а также при дискомфорте в животе, тошноте и/или рвоте показаны энтеросорбенты (диоксид кремния коллоидный, полиметилсилоксанаполигидрат и другие).
Пациентам в тяжелом состоянии (в ОРИТ) при наличии показаний проводится инфузионная терапия. Следует с осторожностью подходить к инфузионной терапии, поскольку избыточные трансфузии жидкостей могут ухудшить насыщение крови кислородом, особенно в условиях ограниченных возможностей ИВЛ, а также спровоцировать или усугубить проявления ОРДС. Объем инфузионной терапии должен составлять 10-15 мл/кг/сут.
При проведении инфузионной терапии важное значение имеет скорость введения жидкости: чем меньше скорость введения жидкости, тем безопаснее для пациента.
В условиях проведения инфузионной терапии врач оценивает суточный диурез, динамику артериального давления, изменения аускультативной картины в легких, гематокрита (не ниже 0.35/л). При снижении объема диуреза, повышении артериального давления, увеличения количества хрипов в легких, снижении гематокрита объем парентерально вводимой жидкости должен быть уменьшен.
Для снижения объема инфузионной терапии поддержание нутритивного статуса пациента при необходимости нужно проводить методом зондового питания с использованием стандартных и полуэлементарных смесей для энтерального питания. Питание должно быть частым и дробным для исключения переполнения желудка и уменьшения экскурсии легких.
С целью улучшения отхождения мокроты при продуктивном кашле назначают мукоактивные препараты (ацетилцистеин, амброксол, карбоцистеин). Бронхолитическая ингаляционная терапия с использованием сальбутамола, фенотерола, с применением комбинированных средств (ипратропия бромид+фенотерол) целесообразна при наличии бронхообструктивного синдрома.
Жаропонижающим препаратом первого выбора является парацетамол, который назначается по 500-1000 мг до 4 раз в день (не более 4 г в сутки).
Симптоматическое лечение включает:
• Купирование лихорадки (жаропонижающие препараты, например, парацетамол);
• Комплексную терапию ринита и/или ринофарингита (увлажняющие/ элиминационные препараты, назальные деконгестанты);
• Комплексную терапию бронхита (мукоактивные, бронхолитические и прочие средства).
Жаропонижающие назначают при t тела > 38,0-38,5 ºС. При плохой переносимости лихорадочного синдрома, головных болях, повышении артериального давления и выраженной тахикардии (особенно при наличии ишемических изменений или нарушениях ритма) жаропонижающие препараты используют и при более низких цифрах. Наиболее безопасным препаратом является парацетамол.
Для местного лечения ринита, фарингита, при заложенности и/или выделениях из носа начинают с солевых средств для местного применения на основе морской воды (изотонических, а при заложенности – гипертонических). В случае их неэффективности показаны назальные деконгенстанты. При неэффективности или выраженных симптомах могут быть использованы различные растворы с антисептическим действием.
Во время беременности (II и III триместры), в послеродовом и постабортном периоде возможно применение муколитических средств с помощью mesh-небулайзера (амброксол 2-3 мл с изотоническим раствором 2 мл 3 раза в день) и бронходилататоров (ипратропия бромид + фенотерол по 20 капель в 2-4 мл изотонического раствора 2 раза в день). Во время беременности (I, II и III триместры), в послеродовом и постабортном периоде в качестве бронходилататора также может применяться сальбутамол с помощью mesh-небулайзера (2,5-5 мг 2 раза в день).
Необходимым компонентом комплексной терапии является адекватная респираторная поддержка. Показатели сатурации кислорода должны определяться у всех беременных с клиникой острого респираторного заболевания и/или с пневмонией.
Показаниями для перевода в ОРИТ при коронавирусной инфекции являются быстропрогрессирующая ОДН (ЧД > 25 в 1 мин, SpO2 < 92%, а также другая органная недостаточность (2 и более балла по шкале SOFA).
У пациентов пожилого и старческого возраста делирий может быть первой манифестацией заболевания или развиться по мере его прогрессирования. Госпитализация пациента, помещение в блок интенсивной терапии и на ИВЛ повышают риск развития делирия. Развитие делирия, особенно гиперактивной формы, может представлять собой дополнительные трудности лечения пациентов.
Рекомендации:
1. Регулярный скрининг делирия с использованием рекомендованных инструментов у всех пациентов пожилого и старческого возраста, госпитализированных в связи с COVID-19.
2. Рекомендуется проводить профилактику делирия у всех пациентов пожилого и старческого возраста, госпитализированных в связи с COVID-19, путем коррекции его триггеров. Профилактические меры включают: регулярную ориентацию пациента в его личности, во времени и пространстве, профилактику запоров, лечение боли, лечение бактериальной пневмонии (высока вероятность ее присоединение у пациентов с COVID-19), адекватную оксигенотерапию, профилактику задержки мочи, а также пересмотр сопутствующей терапии для минимизации назначения препаратов, повышающих риск делирия.
3. При появлении поведенческих нарушений необходимо прежде всего оценить и провести коррекцию триггеров развития делирия (см. выше). При неэффективности этих мер и/или необходимости более быстрого контроля ситуации для снижения риска для пациента или окружающих может потребоваться более ранний, чем обычно, переход к фармакологическому лечению.
4. При назначении быстро действующих транквилизаторов необходимо мониторировать развитие побочных эффектов, состояние жизненно важных показателей (ЧДД, SрO2, АД, ЧСС), уровень гидратации и сознания, по крайней мере, каждый час до тех пор, пока не будет убежденности в их стабильности. Следует помнить о том, что бензодиазепины угнетают дыхание, а также не превышать максимальные дозы препаратов галоперидола (2 мг/сутки независимо от пути введения), рисперидона (1 мг/сутки в несколько приемов), лоразепама (2 мг/сутки независимо от пути введения).
У пациентов пожилого и старческого возраста COVID-19 повышает риск развития недостаточности питания. Повышение этого риска связано как с клиническими симптомами заболевания (снижение обоняния и вкуса, снижение аппетита, диарея, лихорадка, слабость), так и с социальными факторами (самоизоляция), которые в ряде случаев потенциируют предсуществующие риски. Пациенты старческого возраста с полиморбидностью в большей степени подвержены риску недостаточности питания и ассоциированной с ней саркопении, именно у этой группы прогноз при COVID-19 наиболее неблагоприятен. ИВЛ, особенно пролонгированная, является хорошо документированной причиной недостаточности питания с потерей мышечной массы и функции, что, в свою очередь, ассоциировано в дальнейшем со снижением качества жизни и утратой автономности после выписки из стационара. Адекватная оценка пищевого статуса, профилактика и коррекция недостаточности питания эффективно снижают риск осложнений и улучшают клинические исходы.
Рекомендуется:
1. У всех пациентов пожилого и старческого возраста, госпитализированным с COVID-19, проводить скрининг риска недостаточности питания с использованием валидированнных инструментов.
2. Для пациентов, которые по результатам скрининга относятся к категориям «риск недостаточности питания» или «недостаточность питания», необходимо проводить коррекцию с использованием продуктов перорального энтерального питания (ПЭП).
3. Рекомендуется рассчитывать энергетическую ценность рациона пациента пожилого и старческого возраста, ориентируясь на уровень 30 ккал на кг массы тела в сутки, суточный уровень потребления белка должен составлять не менее 1,0-1,2 г на кг массы тела в сутки (при тяжелом течении заболевания и диагностированной недостаточностью питания – до 2,0 г/кг массы тела в сутки).
4. Рекомендуется назначать препараты ПЭП, которые обеспечивают поступление в организм энергии не менее 400 ккал/сут и белка не менее 30 г/сут. При отсутствии противопоказаний для обеспечения оптимального функционирования желудочно-кишечного тракта предпочтительны продукты ПЭП, содержащие пищевые волокна.
5. В случаях, когда пероральное питание невозможно, рекомендуется без промедлений начинать зондовое энтеральное питание (ЗЭП).
6. При выписке из стационара пациентам с недостаточностью питания или риском ее развития рекомендуется применять ПЭП с целью оптимизации уровня потребления пищи и массы тела, а также с целью уменьшения риска снижения функциональных возможностей. Рекомендуется назначать ПЭП на срок не менее одного месяца и оценивать эффективность и ожидаемую пользу ПЭП один раз в месяц.
Антибактериальная терапия назначается при наличии убедительных признаков присоединения бактериальной инфекции (повышение прокальцитонина более 0,5 нг/мл, лейкоцитоз > 10*109/л, появление гнойной мокроты).
Выбор антибиотиков и способ их введения осуществляется на основании тяжести состояния пациента, анализе факторов риска встречи с резистентными микроорганизмами (наличие сопутствующих заболеваний, предшествующий прием антибиотиков и др.), результатов микробиологической диагностики. С целью уменьшения нагрузки на медицинский персонал целесообразно использовать пероральные формы антимикробных препаратов, ступенчатую терапию (амоксициллин/клавулановая кислота в/м, в/в – переход на прием амоксициллина/клавулановой кислоты per os, цефтриаксон, цефотаксим в/м, в/в с последующим переходом на цефдиторен per os).
Пациентам в тяжелом состоянии (ОРИТ) при наличии признаков бактериальной инфекции (повышение ПКТ более 0,5 нг/мл, появление гнойной мокроты) рекомендована комбинированная терапия: защищенные аминопенициллины (амоксициллин/клавулановая кислота, амоксициллин/сульбактам), цефалоспорины (цефтриаксон, цефотаксим цефтаролина фосамил,) в/в комбинации с азитромицином или кларитромицином в/в.
Альтернативой является применение цефалоспоринов третьего поколения (цефтриаксон, цефотаксим) в/в комбинации с респираторным фторхинолоном (левофлоксацин, моксифлоксацин) в/в. При совместном использовании фторхинолонов с препаратами группы 4-аминохинолонов (гидроксихлорохин) следует учитывать риск потенциирования кардиотоксического эффекта.
Пациентам с наличием факторов риска инфицирования Staphylococcus aureus (недавно перенесенные хирургические вмешательства, госпитализации или пребывание в доме престарелых, наличие постоянного внутривенного катетера, диализ) целесообразно эмпирическое назначение препаратов, обладающих антистафилококковой активностью (цефтаролина фосамил, линезолид, ванкомицин) в комбинации с респираторным фторхинолоном в/в.
Пациентам с факторами риска инфицирования P. aeruginosa (длительная терапия системными ГКС, муковисцидоз, вторичные бронхоэктазы, недавний прием системных антибиотиков) рекомендованы – комбинация β-лактамного антибиотика с антисинегнойной активностью (пиперациллин/тазобактам, меропенем, имипенем/циластатин, дорипенем) с ципрофлоксацином или левофлоксацином; альтернатива – комбинация β-лактамного препарата с антисинегнойной активностью с аминогликозидами II-III поколения и макролидами, либо респираторным фторхинолоном.
В случае клинической неэффективности или развития нозокомиальных осложнений выбор режима антимикробной терапии необходимо осуществлять на основании выявления факторов риска резистентных возбудителей, анализа предшествующей терапии, результатов микробиологической диагностики (пиперациллин/тазобактам, цефепим/сульбактам, меропенем, дорипенем, имипенем/циластатин, цефтолозан/тазобактам, цефтазидим/авибактам, тигециклин, азтреонам, амикацин, телаванцин и др.).
Особенности антибактериальной терапии у беременных, рожениц и родильниц
Начать лечение эмпирическими антибиотиками после постановки диагноза пневмонии в течение 4 ч, при тяжелой пневмонии – в течение 1 ч.
Пациенткам с тяжелым течением заболевания антибактериальные препараты вводятся внутривенно.
При вторичной вирусно-бактериальной пневмонии (наиболее вероятные возбудители – Streptococcus pneumoniae, Staphylococcus aureus и Haemophilus influenza) предпочтительнее использовать следующие схемы антибиотикотерапии:
• Цефалоспорин III поколения ± макролид;
• Защищенный аминопенициллин ± макролид;
При третичной бактериальной пневмонии (наиболее вероятные возбудители – метициллинрезистентные штаммы Staphylococcus aureus, Haemophilus influenza) обосновано назначение следующих препаратов (в различных комбинациях):
• Цефалоспорин IV поколения ± макролид;
• Карбапенемы;
• Ванкомицин;
• Линезолид.
К антибактериальным лекарственным средствам противопоказанным при беременности, относятся тетрациклины, фторхинолоны, сульфаниламиды.
Акушерская тактика определяется несколькими аспектами: тяжестью состояния пациентки, состоянием плода, сроком гестации. При средней степени тяжести и тяжелом течении заболевания до 12-й недели гестации в связи с высоким риском перинатальных осложнений, связанных как с воздействием вирусной инфекции, так и эмбриотоксичным действием лекарственных препаратов, возможно прерывание беременности после излечения инфекционного процесса. При отказе пациентки от прерывания беременности необходима биопсия ворсин хориона или плаценты до 12-14-й недель или амниоцентез с 16 недель гестации для выявления хромосомных аномалий плода, которые проводятся по желанию женщины.
Прерывание беременности и родоразрешение в разгар заболевания сопряжено с увеличением показателя материнской летальности и большим числом осложнений: утяжеление основного заболевания и вызванных им осложнений, развитие и прогрессирование дыхательной недостаточности, возникновение акушерских кровотечений, интранатальная гибель плода, послеродовые гнойно-септические осложнения. Однако при невозможности устранения гипоксии на фоне ИВЛ или при прогрессировании дыхательной недостаточности, развитии альвеолярного отека легких, а также при рефрактерном септическом шоке по жизненным показаниям в интересах матери и плода показано экстренное абдоминальное родоразрешение (кесарево сечение) с проведением всех необходимых мероприятий по профилактике коагулопатического и гипотонического акушерского кровотечения.
В сроке беременности до 20 недель экстренное кесарево сечение можно не проводить, так как беременная матка в этом сроке не влияет на сердечный выброс. В сроке беременности 20-23 недели экстренное кесарево сечение проводится для сохранения жизни матери, но не плода, а в сроке более 24 недель – для спасения жизни матери и плода.
В случае развития спонтанной родовой деятельности в разгар заболевания (пневмонии) роды предпочтительно вести через естественные родовые пути под мониторным контролем состояния матери и плода.
Предпочтительным методом обезболивания является регионарная аналгезия при отсутствии противопоказаний. Противовирусная, антибактериальная, детоксикационная терапия, респираторная поддержка проводятся по показаниям.
Во втором периоде для профилактики развития дыхательной и сердечно-сосудистой недостаточности следует ослабить потуги. С целью ускорения процесса родоразрешения при дистрессе плода, слабости родовой деятельности и/или ухудшении состояния женщины возможно применение вакуум-экстракции или акушерских щипцов.
Кесарево сечение выполняется по стандартным акушерским показаниям. Однако при невозможности устранения гипоксии на фоне ИВЛ или при прогрессировании дыхательной недостаточности, развитии альвеолярного отека легких, а также при рефрактерном септическом шоке по жизненным показаниям в интересах матери и плода показано экстренное абдоминальное родоразрешение (кесарево сечение) с проведением всех необходимых мероприятий по профилактике коагулопатического и гипотонического акушерского кровотечения. При тяжелой форме течения COVID-19 предпочтительным доступом является нижнесрединная лапаротомия.
Анестезиологическое обеспечение операции кесарева сечения при тяжелом течении заболевания: в отсутствии признаков выраженной полиорганной недостаточности (до 2 баллов по шкале SOFA) возможно применение регионарных методов обезболивания на фоне респираторной поддержки, при выраженной полиорганной недостаточности – тотальной внутривенной анестезии с ИВЛ.
Всем пациенткам, независимо от срока беременности, показана профилактика кровотечения.
Во всех случаях вопрос о времени и методе родоразрешения решается индивидуально.
Клиническими критериями выписки из стационара беременных и родильниц являются:
• Нормальная t тела в течение 3-х дней;
• Отсутствие симптомов поражения респираторного тракта;
• Восстановление нарушенных лабораторных показателей;
• Отсутствие акушерских осложнений (беременности, послеродового периода).
Прогноз для матери и плода зависит от триместра гестации, в котором возникло заболевание, наличия преморбидного фона (курение, ожирение, фоновые заболевания органов дыхательной системы и ЛОР-органов, сахарный диабет, ВИЧ-инфекция), степени тяжести инфекционного процесса, наличия осложнений и своевременности начала противовирусной терапии.
Маршрутизация новорожденных высокого риска по развитию COVID-19 основывается на выделении групп риска в зависимости от инфицирования матери.
Потенциально инфицированным SARS-CoV-2 считается ребенок:
• Рожденный от матери, у которой выявлен подтвержденный случай COVID-19 за 14 дней до родов;
• Рожденный от матери с подозрением на инфицирование SARS-CoV-2, в том числе находившейся на самоизоляции (из группы подлежащих карантину по контакту с инфицированным SARS-CoV-2);
• Новорожденный до 28 дней постнатального периода в случаях его контакта с инфицированными/потенциально инфицированными SARS-CoV-2 (включая членов семьи, опекунов, медицинский персонал и посетителей).
Инфицированным новорожденный считается при положительном результате исследования биоматериала на РНК SARS-CoV-2 МАНК вне зависимости от наличия или отсутствия клинической картины.
Для присутствия на родах и перемещения ребенка должна быть заранее выделенная врачебно-сестринская бригада для новорожденного, которая приглашается в родильный зал не ранее начала потужного периода или начала анестезии при кесаревом сечении, ожидает рождения ребенка на расстоянии не менее 2-х метров от роженицы. Использование СИЗ обязательно.
Число людей, оказывающих помощь в помещении, должно быть минимизировано, чтобы уменьшить контакт с больным.
Не рекомендовано отсроченное пережатие пуповины; не рекомендован контакт мать-ребенок; ребенок к груди не прикладывается для предотвращения постнатального инфицирования, максимально быстро выносится из родильного зала.
В зависимости от клинического состояния женщины возможно поддержание лактации для последующего грудного вскармливания ребенка после выздоровления матери.
Первичная и реанимационная помощь новорожденному оказывается в свободном родильном зале или в специально выделенном помещении с учетом минимизации применения технологий, способствующих образованию внешнего инфицированного аэрозоля (санация трахеи, вентиляция мешком Амбу, неинвазивное введение сурфактанта и другие).
Предметы диагностики и лечения (стетоскоп, термометр и др.) и средства ухода должны быть индивидуального использования для каждого ребенка, после его перевода должны быть обработаны в соответствии с правилами.
Врачи, медсестры и другой персонал, контактирующий с ребенком, должны находиться в СИЗ.
После рождения ребенок должен быть выведен из помещений, предназначенных для беременных, рожениц и родильниц с COVID-19 и изолирован в специально выделенном отделении (обычно отделение детской больницы). Транспортировка производится в транспортном кувезе, персонал использует СИЗ. Специально выделенный медицинский автотранспорт подлежит дезинфекции по правилам работы с особо опасными инфекциями.
У новорожденного ребенка берутся мазки из носа и ротоглотки на COVID-19 сразу после перемещения из родильного зала или сразу после установления постнатального контакта с COVID-19- позитивными людьми из его окружения. Далее исследование на РНК SARS-CoV-2 повторяется через 2-3 суток. Если оба результата исследования отрицательные, то ребенок считается неинфицированным SARS-CoV-2. Если ребенок по эпидемиологическим показаниям должен находиться на карантине, то контрольные исследования биологического материала из носа, ротоглотки, а также стула проводятся на 10-12-е сутки карантина с целью принятия решения о возможности его прекращения к 14 суткам. Если один из результатов исследования на РНК SARS-CoV-2 положительный, то ребенок считается инфицированным данным вирусом и дальнейшие контрольные исследования проводятся в соответствии с рекомендациями по ведению пациентов с COVID-19.
Вакцинация и неонатальный скрининг откладываются до установления SARS-CoV-2-отрицательного статуса.
При необходимости медицинская помощь новорожденному оказывается в соответствии с клиническими рекомендациями.
04.11.2020 | 17:40:06