Физиология плода. Функциональная система Мать-Плацента-Плод.
Раздел: Статьи
/
Акушерство и гинекология
/
Акушерство
/
Физиология плода. Функциональная система Мать-Плацента-Плод.
Содержание
Физиология плода
- Сердечно-сосудистая система плода
- Гемопоэз плода
- Кровообращение плода
- Иммунная система плода
- Дыхательная система плода
- Нервная система плода
- Нейроэндокринная система плода
- Выделительная система плода
- Желудочно-кишечный тракт плода
Функциональная система мать-плацента-плод
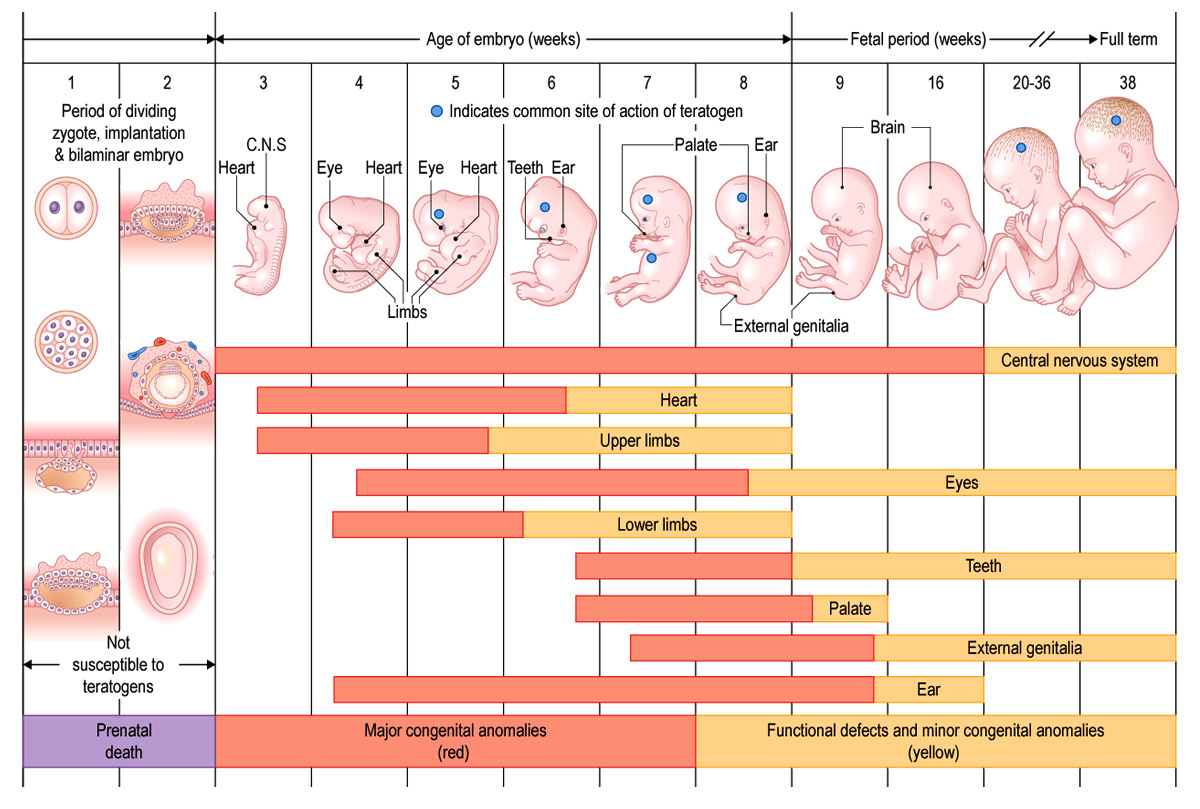
Во внутриутробном развитии человека условно выделяют два периода: эмбриональный (зародышевый) и фетальный (плодовый). К эмбриональному периоду относят первые 8 нед существования зародыша. В этот промежуток времени образуются зачатки всех важнейших органов и систем. Фетальный период начинается с 9-й недели беременности и заканчивается рождением плода. В этот период происходит развитие органов и систем, находившихся в зачаточном состоянии, совершается становление новых функциональных систем, обеспечивающих жизнедеятельность плода и новорожденного.
Развитие организма до рождения происходит чрезвычайно динамично. Темп роста плода значительно выше, чем организма в любые периоды его жизни после рождения. В течение короткого времени оплодотворенная яйцеклетка превращается в новорожденного, происходит генетически обусловленная строгая последовательность формирования органов и систем, которые проходят путь от начальной дифференциации до определенной стадии развития, обеспечивающей переход к внеутробному существованию. П.К. Анохин и его сотрудники создали теорию системогенеза на основании функциональных систем, необходимых для выживания новорожденных, но в которых во время внутриутробного развития нет жизненной необходимости. К таким системам относятся функциональная система дыхания, способность к акту сосания и т.д. Однако в эмбриогенезе происходит гетерохронное созревание функциональных систем плода не только в зависимости от их значения для выживания новорожденных, но и для выживания зародыша и плода на разных этапах внутриутробного развития, причем некоторые из них существуют только в период до рождения.
Сердечно-сосудистая система является первой системой, которая начинает функционировать у зародыша. Ее образование происходит в первые дни жизни зародыша: первые сокращения сердца и движения крови обнаруживаются уже в начале 4-й недели его развития. К концу 4-й недели можно различить основные отделы сердца, но оно действует еще как простая сократимая трубка с неразделенным потоком крови. С середины 6-й недели внутриутробной жизни начинается процесс развития внутрисердечных перегородок, который заканчивается к началу 8-й недели жизни: к этому времени сердце по своему строению оказывается близко к сформированному. Отверстие в межжелудочковой перегородке, образующееся в процессе ее развития, закрывается около 7-й недели жизни эмбриона, после чего сердце полностью разделяется на правую и левую половины. Остается открытым вплоть до рождения овальное отверстие в межпредсердной перегородке, клапан которого позволяет перемещаться крови в левое предсердие из правого, но не допускает движения крови в обратном направлении.
Образование кровеносных сосудов в теле зародыша начинается еще до появления закладки сердца, но позднее, чем это происходит в желточном мешке. Кровеносные сосуды желточного мешка формируются в конце 2-й недели, основные сосуды тела - к середине 3-й недели. Закладка сосудов в разных органах происходит автономно, в разное время, но в течение первых 4-5 нед.
На первых порах непосредственным регулятором работы сердца является небольшой сгусток своеобразной специфической ткани, закладывающейся в самом раннем онтогенезе, и сердце сокращается, еще не имея иннервации, с помощью местных механизмов. На границе 4-й и 5-й недель внутриматочной жизни доиннервационный период развития сердца заканчивается, к нему подрастают первые нервные волокна. Развитие иннервации сердца начинается с врастания в него ветвей блуждающих нервов при длине зародыша 7,5 мм. Позднее, в конце 7-й недели развития зародыша, длина которого составляет 17 мм, врастают симпатические волокна. К этому моменту заканчивается внутриорганное развитие сердца и происходит развитие проводящей системы миокарда. Полагают, что первым звеном иннервации сердца является афферентное звено. Устанавливается связь между сердцем и продолговатым мозгом, после чего начинается афферентная импульсация с сердца, способствующая развитию ядер блуждающего нерва и имеющая значение в развитии сердечно-сосудистого центра.
Постепенно созревает и система регуляции сосудистого русла плода с превалированием симпатического влияния над парасимпатическим.
Частота сердечных сокращений (ЧСС) изменяется по мере развития плода и становления нервной регуляции работы сердца. В ранние сроки I триместра беременности, особенно в течение первых 6 нед, частота сокращений сердца относительно невелика (90-128 в минуту), на 7-8-й неделе она возрастает до 177 в минуту, а к 12-15-й неделе устанавливается на уровне 155-147 в минуту. Затем частота сердцебиения несколько уменьшается.
Сердце плода в норме находится под влиянием повышенного тонуса симпатической нервной системы, что, как полагают, является механизмом приспособления к относительной гипоксемии. Однако при одновременном раздражении блуждающего и симпатического нервов превалирует влияние вагуса.
Деятельность сердечно-сосудистой системы зависит от дыхательной и общей двигательной активности плода. Шевеления и дыхательные движения стимулируют пупочно-плацентарный кровоток и тем самым увеличивают возможность получения плодом от матери кислорода и питательных веществ. При обобщенных движениях плода наблюдается тахикардия, свидетельствующая о том, что ЦНС воспринимает проприоцептивные импульсы и координирует в соответствии с ними сердечную деятельность. Эта реакция плода получила название моторно-кардиального рефлекса.
Гемопоэз. Начинается гемопоэз главным образом в желточном мешке. Первые примитивные эритроидные клетки образуются в стенке желточного мешка. У зародыша величиной 5-7 мм уже начинается печеночный период гемопоэза. Начиная с 5-го месяца, костный мозг принимает участие в этом процессе и на 7-м месяце беременности становится основным местом эри-тропоэза. Кроветворение в селезенке происходит между 3-м и 7-м месяцами беременности.
В периферической крови плода эритроциты появляются на 7-8-й неделе. В ранних стадиях развития кровь бедна форменными элементами; среди эритроцитов много ядросодержащих клеток с малым содержанием гемоглобина. С развитием плода количество эритроцитов и гемоглобина увеличивается. Фетальный гемоглобин отличается повышенной способностью поглощать кислород.
Кровообращение плода (рис. 1.1). У плода часть хорошо оксигенированной крови (pO2 = 3 мм рт.ст.) из плаценты поступает в печень и по печеночным венам - в нижнюю полую вену. Второй поток плацентарной крови минует печень и поступает в нижнюю полую вену через венозный проток, расположенный на задней поверхности печени: около 2/3 крови из нижней полой вены поступает в сердце по так называемому левому пути, то есть из правого предсердия через овальное отверстие в левое предсердие, а затем через левый желудочек в восходящую часть аорты.
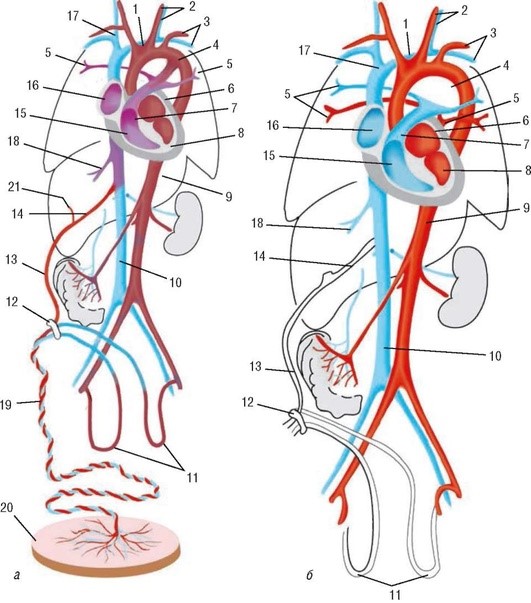
Рис. 1.1. Кровообращение плода (а) и новорожденного (б): а - схема плацентарного кровообращения у плода (кровь артериальная - красного цвета, кровь смешанная - лилового цвета, кровь венозная - синего цвета): 1 - дуга аорты; 2 - сонная артерия и вена; 3 - подключичная артерия и вена; 4 - боталлов проток; 5 - легочные сосуды; 6 - левое предсердие; 7 - легочная артерия; 8 - левый желудочек; 9 - нисходящий отдел аорты; 10 - нижняя полая вена; 11 - пупочные артерии; 12 - пупочное кольцо; 13 - пупочная вена; 14 - аранциев проток; 15 - правый желудочек; 16 - правое предсердие; 17 - верхняя полая вена; 18 - печеночная вена; 19 - артерии пуповины; 20 - плацента; 21 - венозный синус; б - схема легочного кровообращения у новорожденных (кровь артериальная - красного цвета, кровь венозная - синего цвета): 1 - дуга аорты; 2 - сонная артерия и вена; 3 - подключичная артерия и вена; 4 - остаток запустевшего боталлова протока; 5 - легочные сосуды; 6 - левое предсердие; 7 - легочная артерия; 8 - левый желудочек; 9 - нисходящий отдел аорты; 10 - нижняя полая вена; 11 - запустевшие пупочные артерии; 12 - пупочное кольцо; 13 - запустевшая пупочная вена; 14 - запустевший аранциев проток; 15 - правый желудочек; 16 - правое предсердие; 17 - верхняя полая вена; 18 - печеночная вена
Этой более оксигенированной кровью (pO2 = 25-28 мм рт.ст.) снабжаются коронарные сосуды сердца и сосуды, питающие мозг. Из верхней полой вены кровь поступает также в правое предсердие. Через овальное отверстие проходит около 3% этой крови, остальная часть смешивается с 2/3 количества оксигенированной крови из нижней полой вены, не прошедшей через овальное отверстие, и идет по так называемому правому пути - через правое сердце, артериальный проток и нисходящую аорту, из которой 40-50% крови поступает в плаценту (pO2 = 19-22 мм рт.ст.). Остальная часть крови снабжает нижнюю часть туловища. Через легкие проходит только часть крови, составляющая 5-10% общего сердечного выброса. Это связано с высоким сосудистым сопротивлением в этом органе, обусловленным небольшой величиной pO2 в крови, протекающей через легкие. В сосудах легких по мере прогрессирования беременности значительно больше развивается мышечный слой по сравнению с таковым в сосудах других областей.
Иммунная система. Клетки, способные реализовать специфические и неспецифические иммунные реакции, происходят из примитивных гемопоэтических стволовых клеток желточного мешка.
Первые лимфоидные клетки обнаружены в печени на 5-й неделе развития зародыша. На 6-7-й неделе образуется вилочковая железа. Гемопоэтические стволовые клетки мигрируют с кровью в железу. Они обнаруживаются в этом органе с 8-й по 9-ю неделю развития плода. В этот период вилочковая железа становится местом активного лимфопоэза. В вилочковой железе лимфоидные клетки постепенно созревают, становятся резистентными к глюкокортикоидам и приобретают иммунокомпетенцию. Эти клетки являются тимусзависимыми (Т-лимфоциты). Часть лимфоцитов затем мигрирует из вилочковой железы в периферические лимфатические структуры: в паракортикальные зоны лимфатических узлов и периартериолярные области селезенки. Эти клетки являются уже функционально активными. Вилочковая железа растет очень быстро, достигает максимальной величины перед родами или после них. Затем происходит инволюция железы, и ее функцию выполняют другие органы.
Лимфоидная ткань в селезенке появляется около 20-й недели. Максимальная лейкопоэтическая активность в этом органе отмечается на 5-м месяце внутриутробного развития.
Костный мозг начинает функционировать на 11-12-й неделе внутри-маточного развития. Относительно рано клетки приобретают способность синтезировать иммунологически активные белки. Несмотря на раннее становление биосинтеза ряда протеинов комплемента, их концентрация и биологическая активность в конце беременности не превышают 50% активности комплемента взрослого человека. Активный синтез некоторых классов иммуноглобулинов начинается также рано: IgM - на 10-11-й неделе, IgG - на 11-12-й неделе развития плода. Однако продукция их в течение беременности остается на низком уровне и увеличивается постнатально под влиянием стимуляции экзогенными антигенами. На 11-й неделе развития лимфоциты с мембранными поверхностными иммуноглобулинами (В-лимфоциты) G, М и А находятся в периферической крови, костном мозге, селезенке и печени, на 14-й неделе их количество становится таким же, как у взрослых. Низкий уровень синтеза иммуноглобулинов связан не с недостаточным количеством В-лимфоцитов, а, видимо, с ограниченной антигенной стимуляцией в течение внутриматочной жизни. Каждый иммуноглобулин имеет свои характерные черты. Обычно при иммунизации матери образуются глобулины типа G и М, А, которые свободно переходят через плаценту к плоду, причем в таком количестве, что их концентрация в сыворотке крови плода достигает концентрации в крови плода. Физиологическое значение передачи этих иммуноглобулинов от матери к плоду заключается в создании у плода и новорожденного пассивного иммунитета к микроорганизмам, против которых используется главным образом клеточный тип иммунитета. IgA считают «местным» АТ, важным для защиты слизистых оболочек дыхательного и желудочно-кишечного трактов. IgM представляет наибольший интерес, поскольку этот класс АТ доминирует в реакциях плода и новорожденного на антиген. Антигенами для них являются также АВ0- и Rh-агглютинины.
Дыхательная система. Функциональная система дыхания начинает формироваться очень рано. Около середины 4-й недели развития появляется первичный гортанно-трахейный вырост, на дистальном конце которого уже имеется пара утолщений, называемых легочными точками или первичными бронхиальными почками. К 4-й неделе формируются первичные правый и левый бронхи. На 5-й неделе происходит деление бронхов на ветви. Затем происходит быстрое дальнейшее деление бронхов, в результате которого образуется бронхиальное дерево легочной доли. К 6-му месяцу развития насчитывается примерно 17 порядков ветвей, а к моменту рождения их уже 27. Последние из этих ветвей известны как бронхиолы. В течение 6-го месяца внутриутробного развития образуются альвеолы. Цилиндрический эпителий альвеол начинает замещаться плоским, стенки альвеол истончаются. Одновременно наблюдается увеличение легочной капиллярной сети.
Легкие плода человека до 16-й недели беременности имеют железистую структуру. Они растянуты до функциональной остаточной емкости (ФОЕ) жидкостью, которая продуцируется легкими. Избыток этой жидкости заглатывается плодом и/или поступает в ОВ.
Дыхательные мышцы созревают также рано. С помощью ультразвуковых приборов дыхательные движения плода можно обнаружить уже с 11-й недели беременности. В норме дыхательные движения плода происходят при закрытой голосовой щели и околоплодная жидкость не поступает в легкие. Во время апноэ у плода жидкость в легких находится под положительным давлением около 1,5-3 мм рт.ст. по отношению к амниону. Дыхательные движения плода способствуют развитию его дыхательных мышц. Продукция жидкости легкими и дыхательные движения имеют значение в регуляции развития легких.
Одним из наиболее важных факторов, способствующих созреванию легких плода, является синтез и секреция поверхностно-активных липидов - сурфактантов. Сурфактанты регулируют поверхностное натяжение легких во время вдоха и выдоха и поддерживают их в расправленном состоянии. У плода в смыве из легких поверхностно-активный лецитин (основной компонент сурфактантов) обнаруживается на 22-24-й неделе. В 28 нед беременности он вырабатывается в достаточном количестве, чтобы легкие могли выполнять свою функцию. К 34-38-й неделе беременности его количество увеличивается до такой степени, что уже обеспечивается нормальная функция легких. В процессе созревания легких, в частности синтеза сурфактантов, большое значение имеют кортикостероиды. Под их влиянием увеличивается содержание сурфактантов в легких и в околоплодной жидкости. У плода выделяется больше кортикостероидов во время родов, чем в период, им предшествующий, что способствует ускоренному созреванию эпителия легких, продуцирующего сурфактанты.
Нервная система.
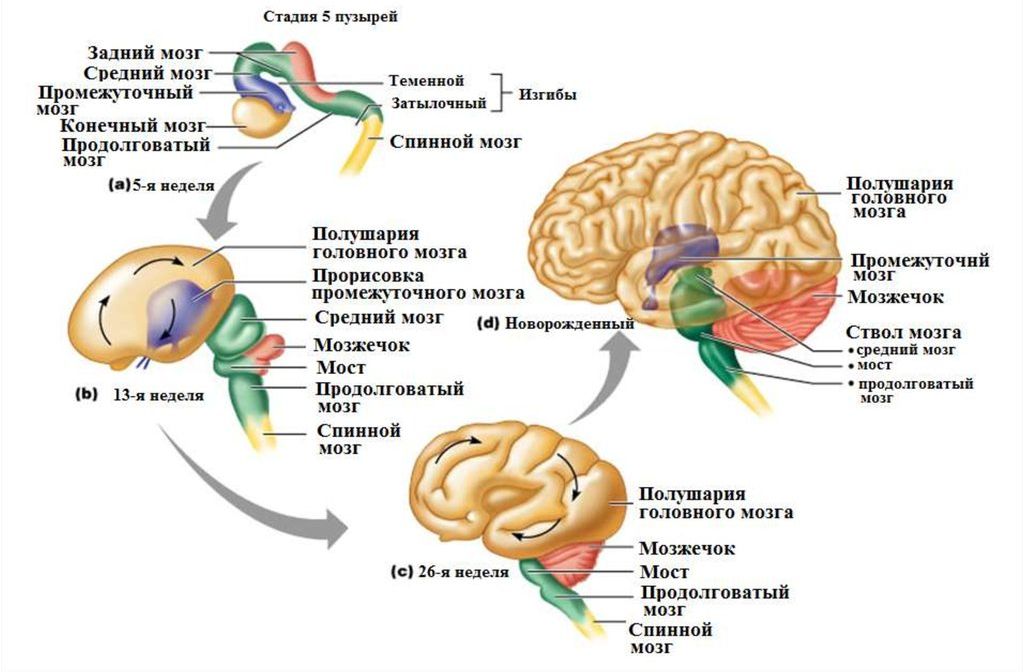
Развитие различных нервных структур головного мозга происходит в строго определенной генетически обусловленной последовательности. В их формировании так же, как и в формировании других органов и систем, наблюдаются периоды развития, которые характеризуются высоким темпом размножения клеток, синтеза белков и легкой повреждаемостью образующихся структур. Подобные периоды обозначают термином «спурт».
Формирование ЦНС начинается очень рано, развитие мозга плода происходит быстрее, чем всех остальных его органов. В стадии бластулы слой эктодермы вдавливается, образуя желобок. Его верхние края растут навстречу друг другу и образуют трубку. Ее части растут неравномерно, что приводит к образованию складок, изгибов, выростов, из которых впоследствии образуются различные части ЦНС. Из просвета нервной трубки формируются желудочки мозга и спинномозговой канал. Спурт образования нейронов относят к 10- 18-й неделе беременности, хотя развитие их продолжается и дальше. На 4-й неделе беременности имеются уже три первичных мозговых пузыря - передний, средний и задний мозг. Дальнейшее развитие мозга заключается в разделении этих трех его пузырей на пять отделов мозга, что происходит на 5-й неделе беременности. Передний мозг подразделяется на два отдела: конечный мозг (telencephalon), из которого затем развиваются большие полушария, и промежуточный мозг (diencephalon) - место развития таламуса и гипоталамуса .
Задний мозговой пузырь также делится на две части: продолговатый мозг (mуelencephalon) и задний мозг (metencephalon) - область развития мозжечка и моста. Средний мозговой пузырь остается неразделенным.
Полагают, что критический период созревания коры большого мозга приходится на 12-16-ю неделю беременности. Это время появления электрических сдвигов в коре и ее ответов на внешние раздражения.
В средней части крыши промежуточного мозга на 7-й неделе беременности появляется эпифиз в виде небольшого выпячивания. Зрительный бугор - это группа ядерных масс, развивающихся в боковых стенках промежуточного мозга. Развитие ядер зрительного бугра идет чрезвычайно быстро. Основные проводящие пути, входящие и выходящие из него, обнаруживаются уже на 7- 8-й неделе беременности.
Гипоталамус развивается из базальных пластинок и дна промежуточного мозга. С ним интимно связан гипофиз, нервная доля которого развивается из дна промежуточного мозга.
Развитие мозжечка начинается позже. Рост его зачатков происходит на 2-м месяце беременности. В течение 4-го и 5-го месяцев беременности поверхностные части мозжечка растут очень быстро, что приводит к развитию большого количества извилин и борозд. Рост мозжечка особенно интенсивен в последние 3 мес беременности.
Миелинизация ЦНС происходит только во второй половине беременности. Этот процесс начинается в продолговатом мозге и достигает полушарий к концу беременности. Афферентные пучки миелинизируются первыми, эфферентные нервы подвергаются этому процессу после рождения. Поскольку миелинизация распространяется от каудальной области по направлению к головному мозгу, рефлексы проявляются раньше на нижних конечностях, чем на верхних.
Спурты развития глии, дендритов и синапсов начинаются примерно с 25-й недели беременности и продолжаются после рождения.
Химический спурт мозга совершается после 32-й недели беременности (образование цереброзидов, ганглиозидов, плазмогенов, фосфолипидов, холестерола). Спурт продолжается и после рождения до 3-4-летнего возраста ребенка.
По мере функционального созревания различных отделов мозга изменяется поведение плода. В 7 нед беременности после региональной дифференциации мозга появляются первые рефлексы в ответ на тактильные раздражения кожи вокруг рта, где имеются чувствительные рецепторы. Спонтанные движения головы и туловища можно видеть у плода при сроке беременности 7,5 нед. Движения конечностей обнаруживаются на 10-й неделе беременности, а на 16-й неделе движения становятся координированными. Мигание (или закрывание глаз) при виброакустическом раздражении возникает у плода на 24-й неделе, глотательные движения появляются на 4-м месяце беременности.
Одним из показателей созревания ЦНС в период антенатального развития является становление цикла активность-покой. По мере формирования этого цикла у плода в разные сроки его развития изменяется и характер регуляции основных функций, в том числе сердечной деятельности, общей двигательной и дыхательной активности. К 28-й неделе беременности у плода уже можно выделить три функциональных состояния: активное, спокойное и промежуточное, временная организация которых в цикл активность-покой происходит к 32-й неделе беременности. Синхронно с фазами цикла изменяется выраженность вегетативных реакций плода (сердечной деятельности, двигательной и дыхательной активности, моторно-кардиального рефлекса). В период фазы покоя они угнетаются, в фазу активности - активируются.
Характер повреждения мозга плода во время его внутриматочной жизни зависит главным образом от вида стрессорного воздействия в критический период развития различных отделов и структур мозга. В противоположность другим органам, критический период развития которых завершается в первые 8 нед, созревание мозга продолжается до конца беременности, а такие отделы, как кора большого мозга, мозжечок, весьма ранимы в последние недели беременности.
Нейроэндокринная система. Функции нервной и эндокринной систем взаимосвязаны, имеются данные о сопряженном развитии элементов некоторых нейроэндокринных функциональных подсистем. Таким образом, развиваются гипоталамо-гипофизарные области и регулируемые ими эндокринные железы.
Гипоталамо-гипофизарная система начинает развиваться очень рано. Передняя доля гипофиза обнаруживается у эмбриона длиной 2-3 мм, а задняя - у эмбриона длиной 7 мм. Эти две части соединяются, когда эмбрион достигает 12 мм.
АКТГ в гипофизе плода обнаруживается в возрасте 9 нед. Созревание надпочечников и секреторная функция их коры обнаруживаются в первую половину пренатального развития. Надпочечники являются одним из самых больших органов плода. В 4 нед беременности их размер превосходит размер почек, но затем они уменьшаются, и ко времени рождения они уже равны 1/3 размеров почек. Три четверти надпочечников составляет фетальная часть коры, которая исчезает через месяц после рождения. В коре надпочечников содержатся ферменты, которые участвуют в синтезе и метаболизме стероидов.
Аденогипофиз плода выделяет также гонадотропные гормоны - ФСГ и ЛГ, которые важны для процесса полового диморфизма. Гипоталамические отделы мозга, гипофиз и половые железы формируются как система с обратной связью. После развития гонад содержание регулирующих их гипофизарных гормонов становится различным у мальчиков и девочек. У зародышей женского пола стимуляция секреции гипофизом гонадотропинов начинается на 2-3 нед раньше (на 3-м месяце развития), чем у зародышей мужского пола, и бывает более интенсивной. Половая дифференцировка по женскому типу не требует контроля со стороны гонад. Яичко очень рано становится активным эндокринным органом, который вызывает маскулинизацию организма. Образование фолликулов в яичниках плода происходит после 20-й недели. Гормонально-зависимая половая дифференцировка происходит в период с 16-й по 28-ю неделю внутриутробного развития, критический период развития половых центров - с 4-го по 7-й месяц. Половой диморфизм зависит от уровня половых гормонов в критические периоды его формирования.
Развитие щитовидной железы (ЩЖ) у плода начинается очень рано. На 4-й неделе ЩЖ уже может синтезировать тиреоглобулин. На 7-й неделе она занимает уже свое дефинитивное положение в организме плода. Тиреоидные фолликулы начинают образовываться около 6-й недели развития плода, а после 10-й недели уже может аккумулироваться йод. В ЩЖ на 12-й неделе внутриутробного развития образуются трийодтиронин и тироксин. ТТГ появляется в гипофизе у плода между 8-й и 12-й неделями беременности. Его интенсивное увеличение происходит между 19-й и 22-й неделями в период созревания гипоталамо-гипофизарной системы. Гипоталамо-гипофизарно-тиреоидная система плода функционирует более или менее автономно. Гормоны ЩЖ оказывают большое влияние на развитие мозга. При их отсутствии (или недостатке) задерживаются образование и созревание нейронов, синаптогенез, разрастание дендритов, уменьшается образование сосудов в коре большого мозга, нарушается миграция клеток. Большое значение для развития мозга имеет инсулин, стимулирующий его рост, способствующий переходу аминокислот в клетке.
Выделительная система. Основным экскреторным органом в период внутриутробного развития плода служит плацента. Однако почки плода являются одним из компонентов функциональной системы, обеспечивающей его водно-электролитный гомеостаз. Для нормального развития плода необходим интенсивный обмен между его телом, ОВ и материнским организмом. При этом большое значение имеет выделение плодом мочи, поступающей в ОВ. Обмен жидкости между матерью и плодом происходит со скоростью 3000-4000 мл/ч. От матери к плоду воды переходит в 500 раз больше, чем нужно для его роста. Очевидно, что это имеет значение для обменных процессов между матерью и плодом и для выполнения ОВ их защитной роли в развитии плода. Возврат воды от плода к матери также интенсивен - через хориоамнион она переходит со скоростью 250 мл/ч.
Постоянные почки (метанефрос) начинают формироваться на 5-й неделе развития плода. Из расширенных концов закладок метанефроса образуются последовательно ветвящиеся выросты. Из первых разрастаний образуются мочеточники, из последующих - лоханки, чашечки и прямые собирательные канальцы. Нефрогенез начинается на 7-й или 8-й неделе беременности и продолжается до 32-34-й недели. На 9-12-й неделе беременности уже имеются хорошо дифференцированные клубочки и проксимальные извитые канальцы. На 14-й неделе петля нефрона (Генле) становится функционально развитой. Не все нефроны созревают и функционируют одновременно: на 11-13-й неделе морфологически сформированы только 20% нефронов, 30% находятся в такой же стадии зрелости на 15-20-й неделе. Количество нефронов удваивается с 20-й недели (350 000) до 40-й недели (820 000) беременности. После рождения, хотя новые канальцы больше не образуются, почки продолжают расти, диаметр клубочков увеличивается.
Образование мочи у плода происходит в самые ранние сроки внутриутробного развития. Ее обнаруживают в мочевом пузыре уже на 20-й неделе развития плода. Постепенно диурез у плода возрастает, и к концу беременности количество мочи доходит до 660 мл/сут. Моча плода гипотонична за счет малого количества солей натрия. Относительно низкое осмотическое давление мочи плода способствует круговороту воды в системе плод - околоплодные воды - мать и поэтому является адекватным для периода внутриутробного развития. Одновременно с водой происходит обмен электролитов.
В обмене воды между телом плода и ОВ имеет значение заглатывание их плодом, что обнаруживается на 4-м месяце беременности. В более поздние сроки беременности плод заглатывает в час около 20 мл ОВ, или приблизительно 500 мл в сутки. Почкам плода еще не свойственна полноценная экскреторная функция, но им присущи процессы клубочковой фильтрации и канальцевой реабсорбции.
В почках плода синтезируются ренин, эритропоэтины, простагландины и, возможно, происходит гликонеогенез. Значение этих веществ выходит за пределы регуляции функции самих почек. Под влиянием ренина образуется ангиотензин, имеющий широкий спектр действия. Система ренин-ангио-тензин у плода уже функционирует. Почки плода обладают также свойством разрушать избыточное количество инсулина, накапливающегося в его организме при определенных условиях, например, при СД у матери.
Участие ЦНС плода в регуляции функции его выделительной системы показывает зависимость выделения мочи от фаз цикла активность-покой. Диурез у плода происходит в активную фазу этого цикла.
Желудочно-кишечный тракт. Начало образования желудка можно заметить уже в конце 4-й недели развития. К началу 9-10-й недели гестации сосудистая система печени принципиально сформирована. Печень плода находится на пути мощного потока крови, поступающего к сердцу по пупочной и воротной венам, и благодаря сильно развитой капиллярной сети ее паренхимы играет значительную роль в регуляции венозного возврата к сердцу и объема крови. Сосудистая система печени может функционировать в качестве временного депо крови, предотвращая перегрузку сердца плода. Правая доля печени получает венозную кровь в основном из системы портальной вены, левая доля - из пупочной вены.
У плода, как и у взрослого человека, пищевые вещества поступают сначала в печень. Однако у плода они попадают в воротное кровообращение не из кишечника, а из плаценты.
По мере прогрессирования беременности, с 20-й по 40-ю неделю, объем печени увеличивается почти в 17 раз. Темп прироста ее объема прогрессивно возрастает, особенно после 34-й недели беременности. Левая доля печени всегда относительно больше правой, что связано с особенностями ее кровоснабжения и присущей ей функцией депонирования крови у плода.
В середине беременности печень является основным источником гемо-поэза. Билирубин обнаруживается в АЖ на 12-й неделе беременности, и его концентрация достигает максимальных значений между 16-й и 30-й неделями беременности. Билирубин удаляется из ОВ через плаценту.
Гликоген определяется в печени впервые около 10-й недели беременности, затем по мере прогрессирования беременности количество его постоянно увеличивается. В последнем триместре содержание гликогена в печени возрастает очень резко, и его количество в 2 раза превосходит таковое у взрослого человека. Оно снижается до уровня взрослого (или несколько ниже) в течение нескольких часов после рождения.
На 15-й неделе беременности в печени появляются ферменты, участвующие в липидном обмене.
Поджелудочная железа появляется как вырост эндодермы двенадцатиперстной кишки. Из дорсальной панкреатической почки образуются тело и хвост железы. Вентральная панкреатическая почка располагается в углу, образованном двенадцатиперстной кишкой и дивертикулом печени. Из нее развиваются общий желчный проток и головка поджелудочной железы. Дорсальная и вентральная почки срастаются около 7-й недели развития эмбриона. Эндокринные клетки островков происходят из почкующихся и ветвящихся эпителиальных тяжей. Дифференциация клеток ацинусов происходит на 3-м месяце беременности, когда имеются уже панкреатические островки (Лангерганса). Дифференциация клеток островков на α- и β-клетки происходит у эмбриона, величина которого 130 мм. В конце беременности в поджелудочной железе 60% островков состоит из β-клеток и 30% - из α-клеток. Около 24-й недели беременности в железе отмечается уже протеолитическая активность, но липаза и амилаза на этой стадии отсутствуют. Липаза появляется с 13-14-й недели беременности.
Инсулин может быть получен из поджелудочной железы около 12-й недели гестации. Содержание инсулина в крови у плода сопоставимо с его содержанием в крови новорожденного. Инсулин из крови матери не проходит или почти не проходит через плаценту в кровь плода. В конце беременности плод реагирует на увеличение глюкозы в его крови усилением выработки инсулина, однако эта реакция выражена очень слабо. Она выражена значительнее у плодов и новорожденных, матери которых больны СД.
Инсулин является основным гормоном роста плода. Он также имеет большое значение в углеводном обмене, окислительном метаболизме, в регуляции перехода аминокислот в клетки.
В процессе эмбрио- и фетогенеза происходит развитие функциональных систем, обеспечивающих развитие плода на каждом этапе внутриутробного существования, а также создающих условия для выживания новорожденных.
Для каждой функциональной системы зародыша и плода важно не только ее созревание, но и развитие функций, сопряженных с другими функциональными системами. Для нормального развития ЦНС плода имеет значение афферентная импульсация от сердца, являющегося первым работающим органом у плода. Афферентная система сердца развивается раньше эфферентной. Процесс миелинизации в ЦНС начинается с афферентных нервов. После 7-й недели, когда появляются двигательные реакции плода, импульсация поступает с рецепторов скелетных мышц. После начала дыхательных движений (12-я неделя беременности) начинается импульсация в дыхательные центры. При недостаточной двигательной активности плода происходит недоразвитие его мышечной системы (или недоразвитие мышечной системы приводит к снижению двигательной активности), что сочетается с недостаточной импульсацией в ЦНС. Это приводит к замедлению развития центров, регулирующих деятельность мышц (в том числе дыхательных) и другие функции развивающегося плода. Функциональные системы, необходимые для жизни новорожденного (например, легочное дыхание, пищеварение), не только формируются до рождения, но и проходят периоды тренировки (дыхательные движения плода, заглатывание и переваривание АЖ). Тренируется и координация функций ЦНС - согласованность глотательных движений и дыхания, мышечной работы и сердечной деятельности. Отклонение от нормального темпа развития всех этих процессов приводит к нарушению развития плода и его адаптации к новым условиям жизни после рождения.
В образовании и интеграции функциональных систем, необходимых для приспособления плода к внешней среде, участвует не только плод, но и мать. Организм матери во время беременности приспосабливается к плоду, что отличает функциональную систему мать-плод от известных в биологии форм жизни двух организмов. Генетически запрограммирована строгая последовательность не только развития органов и систем плода, но и процессов адаптации к беременности материнского организма, которая происходит в полном соответствии с этапами внутриутробного развития.
Например, получение кислорода извне обеспечивается гемодинамической функциональной системой мать-плацента-плод, являющейся подсистемой общей функциональной системы мать-плод. Она развивается первой в самом раннем онтогенезе. В ней одновременно формируется фетоплацентарное и МПК.
В плаценте существуют два потока крови:
1) поток материнской крови, обусловленный главным образом системной гемодинамикой матери;
2) поток крови плода, зависящий от реакций его сердечно-сосудистой системы.
Поток материнской крови шунтируется сосудистым руслом миометрия. В конце беременности процент крови, поступающей к межворсинчатому пространству, колеблется между 60 и 90. Эти колебания кровотока зависят главным образом от тонуса миометрия. Вокруг артерий и вен в ворсинках развивается параваскулярная сеть, которую рассматривают как шунт, способный пропускать кровь в условиях, когда через обменную часть плаценты кровоток затруднен. Фетоплацентарное кровообращение и МПК сопряжены, интенсивность кровотока одинакова. В зависимости от изменений состояния активности матери и плода у каждого из них происходит перераспределение крови таким образом, что оксигенация плода остается в пределах нормы.
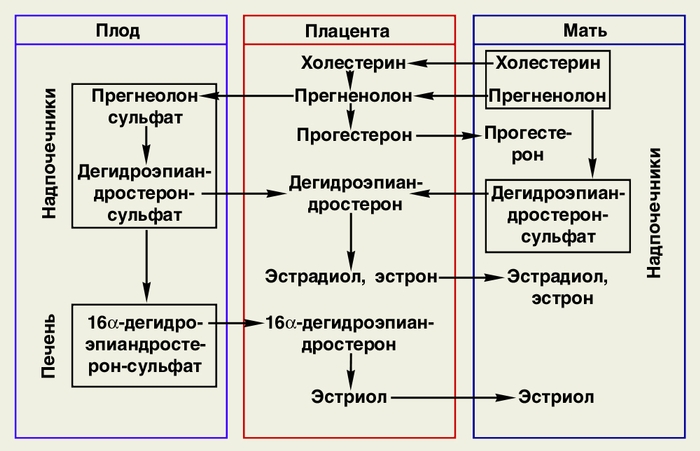
Своеобразно развитие эндокринной функциональной системы плод-плацента-мать, что особенно четко прослеживается на примере синтеза эстриола. Ферментные системы, необходимые для продукции эстрогенов, распределены между плодом (его надпочечниками и печенью), плацентой и надпочечниками матери. Первый этап в биосинтезе эстрогенов во время беременности (гидрок-силирование молекулы холестерина) происходит в плаценте. Образовавшийся прегненолон из плаценты поступает в надпочечники плода, превращаясь в них в дегидроэпиандростерон (ДГЭА). ДГЭА поступает с венозной кровью в плаценту, где под влиянием ферментных систем подвергается ароматизации и превращается в эстрон и Е2. После сложного гормонального обмена между организмом матери и плода они превращаются в эстриол (основной эстроген фетоплацентарного комплекса).
Рост плода является интегративным показателем его развития. Рост плода до рождения неравномерен. Он определяется двумя факторами: основным - генетически закодированным внутренним потенциалом роста и добавочным - состоянием матери и плаценты (интенсивность МПК). Рост плода происходит линейно, но темп его в разные триместры беременности различен. Инкремент роста (прирост на единицу массы) вначале очень интенсивен, на 10-й неделе беременности он равен 70% в неделю, затем уменьшается.
Абсолютное увеличение массы плода, определяющее возрастающее потребление им продуктов питания (измеренное в прибавке массы за неделю) и кислорода, ускоряется после 15-16-й недели с 10 до 85 г/нед. К 26-27-й и к 37-38-й неделе доходит до 200 г/нед, а затем темп прироста массы плода снижается и остается на более низком уровне до родов.
Минимальный прирост массы плода в конце беременности связан с развитием так называемой физиологической относительной плацентарной недостаточности (ПлН), возникающей в результате уменьшения интенсивности МПК из-за процессов «старения» плаценты. Рост плаценты к концу беременности замедляется значительно больше, чем рост плода. Специальные исследования показали, что при физиологически протекающей беременности интенсивность МПК после 36-й недели возрастает незначительно, а к концу беременности даже несколько уменьшается, что осложняет обменные процессы между матерью и плодом.
Отношение массы тела плода к его длине не остается постоянным, поскольку к 33-й неделе беременности в теле плода увеличивается содержание жира и воды.
У матерей высокого роста (164 см и выше) новорожденные весят на 250 г больше, чем у матерей меньшего роста (158 см и ниже). При первой беременности масса плода меньше, чем при повторной беременности, это различие определяется с 32-й недели. Разница равна 120 г к 36-й неделе и 200 г к 40-й неделе беременности. Мужской плод с 20-й недели растет быстрее женского. В 32 нед разница составляет 50 г, а на 40-42-й неделе она достигает 150 г.
Основной стимулятор роста плода - инсулин. Он усиливает липогенез, оказывает анаболическое влияние на белковый метаболизм. Гиперинсулинизм у плода является основной причиной увеличения его массы при СД у матери.
Для определения срока беременности по длине плода предлагались различные схемы. Наиболее распространена и удобна для запоминания схема Гаазе (Haase). В первые 5 мес беременности длина плода (в сантиметрах) соответствует числу месяцев, возведенному в квадрат, а начиная с 6-го месяца и до конца беременности - числу месяцев, умноженному на коэффициент 5. В табл. 1.1 представлены длина и масса плода в разные сроки беременности (в неделях).
Таблица 1.1. Длина и масса плода в зависимости от срока беременности
| Срок беременности, нед | Длина плода, см | Масса плода, г |
| 4 | 1 | - |
| 8 | 4 | - |
| 12 | 9 | 20 |
| 16 | 16 | 120 |
| 20 | 25 | 300 |
| 24 | 30 | 700 |
| 28 | 35 | 1000 |
| 32 | 40 | 1600 |
| 36 | 45 | 2500 |
| 40 | 50 | 3000-3500 |
Источник: Акушерство: учебник / Э. К. Айламазян [и др.]. - 10-е изд., перераб. и доп. - М.: ГЭОТАР-Медиа, 2019.
25.05.2020 | 22:09:16